WRAP UP SKENARIO 1 BLOK ENDOKRIN DAN METABOLISME DISUSUN OLEH: KELOMPOK A2 Ketua : Freza Farizan (1102013114) Sekretaris : Amorrita Puspita Ratu (1102013023) Anggota : 1. Adinda Amalia Sholeha (1102013007) 2. Airindya Bella Kusumaningtyas (1102013016) 3. Bendit Setiawan (1102013056) 4. Dinda Apriyanti (1102013086) 5. Elda Amelinda Hazima (1102013093) 6. Eli Susanti (1102013095) 7. Nurul Ula (1102012148) 1

Wrap Up Sk 1 Endokrin Pbl a2
Dec 11, 2015
PAKE BAIK BAIK
Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

WRAP UP SKENARIO 1BLOK ENDOKRIN DAN METABOLISME
DISUSUN OLEH:KELOMPOK A2
Ketua : Freza Farizan (1102013114)Sekretaris : Amorrita Puspita Ratu (1102013023)Anggota :
1. Adinda Amalia Sholeha (1102013007)2. Airindya Bella Kusumaningtyas (1102013016)3. Bendit Setiawan (1102013056)4. Dinda Apriyanti (1102013086)5. Elda Amelinda Hazima (1102013093)6. Eli Susanti (1102013095)7. Nurul Ula (1102012148)
FAKULTAS KEDOKTERAN UMUMUNIVERSITAS YARSI
2014/2015
1

SKENARIO 1
PENGLIHATAN TERGANGGU
Tn. A, 56 tahun, mengeluh penglihatan terganggu di kedua mata sejak 2 bulan yang lalu. Kadang-kadang terlihat bintik gelap dan lingkaran-lingkaran cahaya. Pasien sudah mengidap DM tipe 2 sejak 5 tahun. Saat ini telapak kaki terasa kesemutan dan nyeri bila berjalan. Tekanan darah 130/90 mmHg, berat badan 80 kg, tinggi badan 165 cm, dan indeks massa tubuh (IMT) 29,4 kg/m2, lingkar perut 108 cm. Kulit teraba kering dan pada pemeriksaan sensorik dengan monofilament Semmes Weinstein 10 gram sudah terdapat penurunan rasa nyeri. Pemeriksaan Ankle Brachial Index 0,9. Pada pemeriksaan funduskopi terdapat mikroaneurisma dan perdarahan dalam retina. Hasil laboratorium glukosa darah puasa 256 mg/dl, glukosa darah 2 jam setelah makan 345 mg/dl, HbA1c 10,2 g/dl, dan protein urin positif 3.
Dokter menyarankan untuk dilakukan pemeriksaan lebih lanjut untuk melihat komplikasi kronik mikroangiopati, makroangiopati, dan neuropati. Pasien juga diberikan edukasi perencanaan makan diet 1900 kalori yang halal dan baik sesuai ajaran Islam, jenis olahraga yang sesuai, dan pemberian insulin untuk mengontrol glukosa darahnya, serta efek samping yang dapat terjadi akibat pemberian obat.
2

KATA-KATA SULIT
1. Mikroaneurisma: pembengkakan pembuluh darah dan dapat terlihat titik kemerahan pada retina.
2. Mikroangiopati: mengecil dan menebalnya dinding pembuluh darah sehingga protein bocor.
3. Makroangiopati: akumulasi lipid dan gumpalan darah pada pembuluh darah besar.4. Neuropati: masalah saraf yang menyebabkan nyeri, mati rasa, kesemutan,
pembengkakan, kelemahan otot pada bagian tubuh yang berbeda.5. Funduskopi: tes untuk melihat dan menilai keadaan pada fundus okuli.6. Ankle Brachial Index: pemeriksaan non invasif pembuluh darah untuk mendeteksi
iskemia, penurunan perfusi perifer yang dapat menyebabkan angiopati dan neuropati diabetik.
7. Monofilament Semmes Weinstein: tes uji diabetik peripheral neuropati dengan memberikan tekanan pada daerah kaki.
PERTANYAAN & JAWABAN
1. Mengapa kulit kering? Karena pada keadaan glukosuria, glukosa keluar bersama air dan dapat menyebabkan dehidrasi dan akhirnya kulit menjadi kering.
2. Apa hubungan DM dengan obesitas? Banyak makan menyebabkan gula darah meningkat yang akan berujung pada obesitas dan DM.
3. Mengapa harus dilakukan diet kalori? Untuk mempertahankan kadar gula darah.4. Faktor risiko diabetes? Sindrom metabolik (obesitas, HDL rendah, trigliserida tinggi),
genetik, usia, RAS dan gaya hidup.5. Apa penyebab perdarahan pada retina? Mikroangiopati yang menyebabkan kebocoran
pembuluh darah di retina.6. Apa jenis olahraga yang sesuai untuk DM 2? Jalan-jalan kecil 30 menit, 3-4x seminggu.7. Apa penyebab telapak kaki kesemutan dan nyeri saat berjalan? Makroangiopati dan
mikroangiopati yang menyebabkan aliran darah tidak lancar.8. Apa efek samping pemberian insulin? Hipoglikemia.9. Bagaimana pencegahan dan tatalaksana DM 2? Pencegahan: olahraga dan diet teratur.
Tatalaksana: pemberian insulin.10. Bagaimana pandangan Islam terhadap pola makan yang baik dan benar? Makan sebelum
lapar dan berhenti sebelum kenyang.11. Apa perbedaan DM 1 dan 2? DM 1 disebabkan autoimun, DM 2 disebabkan oleh gaya
hidup yang buruk.
3

HIPOTESIS
Gaya hidup yang buruk seperti makan berlebihan dan tidak pernah olahraga dapat menyebabkan obesitas dan sindrom metabolik lain, seperti HDL rendah dan trigliserida tinggi. Keadaan ini dapat menimbulkan gejala-gejala seperti dehidrasi, kulit kering, makroangiopati, mikroangiopati, neuropati, kesemutan, muncul bintik hitam dimata, dan perdarahan di mata. Apabila dilakukan pemeriksaan seperti funduskopi, Ankle Brachial Index, Monofilament Semmes Weinstein, dapat didiagnosis penyakit ini adalah Diabetes Melitus Tipe 2. DM 2 ini dapat dilakukan tatalaksana seperti perubahan pola diet, olahraga teratur, dan pemberian insulin. Tapi pemberian insulin juga dapat menyebabkan efek samping seperti hipoglikemia.
4

SASARAN BELAJAR
LI 1. Memahami dan Menjelaskan Anatomi Pankreas
1.1 Makroskopik
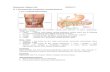
Pankreas merupakan organ yang memanjang, terletak di epigastrium, kuadran kiri atas. Srtukturnya lunak, berlobus, terletak pada dinding posterior abdomen dibelakang peritoneum menyilang planum transpyloricum.
Pankreas dibagi menjadi : Caput : bentuknya seperti cakram, terletak didalam bagian cekung abdomen. Sebagian
kaput meluas ke kiri belakang arteri dan vena mesentrika superior di sebut processus uncinatus.
Collum : bagian pankreas mengecil, menghubungkan kaput dan corpus. Terletak di depan pangkal vene porta hepatis dan tempat dipercabangkannya arteri mesentrika superior dari aorta.
Corpus : berjalan ke atas dan kiri, menyilang garis tengah pada potongan melintang sedikit berbentuk segitiga.
Cauda : berjalan ke depan menuju ligamentum lienorenale dan mengadakan hubungan dengan hilum renale.
Ductus pankreaticus Ductus pankreaticus dari cauda pankreas berjalan disepanjang kelenjar, menerima banyak
cabang dari perjalanannya. Bermuara ke pars descendens duodenum bersama ductus choledokus papila duodeni major. Kadang – kadang muaranya terpisah dengan ductus choledokus.
5

Ductus pankreaticus accesorius ( bila ada ), mengalirkan getah pankreas dari bagian atas caput keduodenum sedikit di atas muara ductus pankreaticus menuju papilla duodeni minor.
Perdarahan Arteri : arteri lienalis, arteri pancreaticiduodenalis superior dan inferiorVena : sesuai dengan arterinya mengalirkan darah ke sistim porta
PersarafanBerasal dari serabut – serabut saraf simpatis dan parasimpatis (vagus)
1.2 Mikroskopik
Pankreas adalah kelenjar campuran eksokrin-endokrin yang menghasilkan enzim pencernaan dan hormon. Sebagai kelenjar eksokrin pankreas membantu dan berperan penting dalam sistem pencernaan dengan mensekresikan enzim-enzim pankreas seperti amilase, lipase dan tripsin.
(Myriam Solar, Carina Cardalda, Isabelle Houbracken et al. Pancreatic Exocrine Duct Cells Give Rise to Insulin-Producing b Cells during Embryogenesis but Not after Birth. Developmental Cell Press. 2009;17:849)
Sebagai kelenjar endokrin, pankreas dikenal dengan produksi hormon-hormon insulin dan glukagon yang berperan dalam metabolisme glukosa. Fungsi endokrin pankreas dilakukan oleh pulau-pulau Langerhans yang tersebar di antara bagian eksokrin pankreas.
(Mescher, Anthony L. Histologi Dasar JUNQUEIRA Teks & Atlas Edisi 12. Jakarta: EGC, 2011)
Pankreas merupakan kelenjar yang penting dengan kedua fungsi eksokrin dan endokrin dengan jaringan ikat fibrosa tipis yang membungkus jaringan parenkimnya. Bagian eksokrin berbentuk seperti setandan buah anggur yang terdiri atas sel asinar pankreas yang disebut asinar, sel ini mensintesis dan menyekresikan enzim pencernaan ke dalam duodenum melalui sistem duktus. Sel asinar pankreas tampak berbentuk piramid dengan apikal sitoplasma yang mengandung granula zimogen dan nukleus yang menonjol yang terletak dekat ke basolateral membran sel. Bagian endokrin dari pankreas membentuk sekitar 1-2% dari total massa, dan bagian ini terdiri dari pulau (pulau kecil) pankreas yang disebut pulau langerhans yang tersebar yang mengandung sekelompok sel pemproduksi hormon yang berbeda.
6

(Wenyan Hu, Gang Zhao, Chunyou Wang, et al. Nonlinear Optical Microscopy for Histology of Fresh Normal and Cancerous Pancreatic Tissues. Plos One. 2012;7:3)
http://legacy.owensboro.kctcs.edu/gcaplan/anat2/notes/pancreas3.jpg
http://embryology.med.unsw.edu.au/embryology/images/e/ea/Pancreas_histology_002.jpg
7

http://www.proteinatlas.org/images_dictionary/pancreas__1__example_1__1_100_1.jpg
Sel asinar terwarnai jelas tersusun dalam lobulus dengan nukleus yang mencolok. Sel pulau terlihat menempel dengan sel asinar dan dikelilingi selaput halus.
Sel asinar dari asini memiliki bentuk piramid, dengan lumen yang sangat kecil. Sel ini memiliki nukleus yang bulat, dengan nukleus berada di dasar dengan tersebar dan terlihat jelas atau mencolok. Sebenarnya sel asinar terlihat letak dasarnya dengan nukleus bulat yang relatif dengan nukleolus yang besar.granula zymogen yang tebal tersebar di apikal sitoplasma, dasar sitoplasma dipenuhi oleh lamela dari retikulum endoplasma kasar yang tersebar dan mitokondria yang oval. Mitokondrianya memiliki matriks yang tebal dan krista yang padat. Aparatus golgi biasanya terletak di dekat granula zimogen.
(Azza A. Attia. Histological and Electron Microscopic Studies of the Effect of β-Carotene on the pancreas of streptozocin (STZ)-Induced Diabetic Rats. Pakistan Journal of Biological Sciences. 2009;12:303)
Pulau langerhans adalah gumpalan massa sel endokrin yang terpulas pucat dan terbenam dalam jaringan asinar eksokrin pankreas. Ada lima tipe sel yang ditemukan di pulau Langerhans, masing-masing memiliki kemampuan sekresi hormon yang berbeda-beda, yaitu:
1. Sel alpha, yaitu sel yang menghasilkan hormon glukagon. Sel ini merupakan sel terbanyak kedua yang ditemukan di pulau Langerhans setelah sel beta (20%).
2. Sel beta, yaitu sel yang meng hasil kan hormon insulin. Sel β terletak di dalam pulau Langerhans dan memenuhi sekitar 80% dari volume pulau Langerhans.
3. Sel delta, sel ini menghasilkan somatostatin.
4. Sel F, sel ini menghasilkan pancreatic polypeptide yangbelum diketahui jelas fungsinya.
8

5. Sel Gamma
Pulau langerhans sebagian besar disusun oleh sel beta, sel alpha dan sel delta dengan sedikit polipeptida pankreas (PP) dan sel epsilon. Di bagian kepala pankreas kaya akan sel PP. Bagian yang kaya akan sel PP berpengaruh untuk mengukur total massa pulau langerhans.
http://www.mc.vanderbilt.edu/root/sitebuilder/mcweb/images/gannonlab/MG2.jpg
http://o.quizlet.com/i/Tr06K_RdQy5Un4kjb9c4AA_m.jpg
Pulau langerhans mengandung dua jenis sel utama yaitu sel alfa () dan sel beta (β). Sedangkan Sel pendukungnya yaitu sel delta () dan sel yang sangat langka yaitu sel C. Sel memproduksi glukagon sampai dengan 20% di sel pulau dan memiliki karakteristik distribusi periferal. Sel β memproduksi insulin sekitar 70% dari sel pulau dan menempati bagian dalam pulau.
Sel alfa dan sel beta memiliki nukleus yang bulat, besar, mencolok dan bersifat basofil. Sitoplasmanya mengandung banyak granula sekresi dengan bagian tengah agak tebal dikelilingi oleh bagian yang lebih jernih. Mitokondria tersebar di seluruh sitoplasma, strukturnya halus dan
9

terlihat bulat atau plum filamen dengan matrik yang tebal. Badan golgi terlihat di beberapa sel di antara granula β.
Walaupun peran dari insulin (sekresi dari sel beta), glukagon (sekresi dari sel alpha), dan somatostatin (sekresi dari sel delta) sangat penting dalam homeostasis glukosa, fungsi tepat dari sel PP di pankreas masih belum diketahui. Pada manusia, efek sel PP adalah mencegah kontraksi kandung empedu dan enzim pankreas. Pada hewan, diperkirakan berpengaruh pada jumlah makanan yang dimakan, metabolisme energi, dan ekspresi ghrelin lambung dan peptida hipotalamus.
Pulau langerhans yang normal ditembus oleh sebuah jaringan kapiler dan diselubungi oleh kolagen tipis dan helaian glial yang memisahkan sel endokrin dari komponen eksokrin. Tetapi, tidak ada pola yang sama untuk setiap pulau di bawah mikroskop, hal ini disebabkan populasi pulau yang jarang.
Pulau langerhans tampak sebagai kelompok sel berbentuk bulat, pucat, dikelilingi simpai halus, tidak memiliki saluran, dengan banyak pembuluh darah untuk penyaluran hormon kelenjar pankreas. Simpai serat-serat retikulin halus mengelilingi setiap pulau langerhans dan memisahkannya dari eksokrin pankreas yang berdekatan. Sel-sel parenkim dan pembuluh darah di inervasi oleh serat saraf autonom. Kebanyakan pulau langerhans bergaris tengah 100-200 μm. Pulau langerhans merupakan kumpulan sel ovoid 76x 1/5 μm yang tersebar di seluruh pankreas. Semua sel dalam pulau berbentuk poligonal tak teratur, dengan inti bundar di tengah, mitokondria kecil berbentuk batang dan aparatus golgi.
(Xiaojun Wang, Mark C. Zielinski, Ryosuke Misawa, et al. Quantitative Analysis of Pancreatic Polypeptide Cell Distribution in the Human Pancreas. Plos One. 2013;8:4)
LI 2. Memahami dan Menjelaskan Fisiologi Insulin
10

A. Efek Insulin pada metabolisme Karbohidrat
Insulin Meningkatkan Metabolisme dan Ambilan Glukosa Otot
Selama hampir sepanjang hari, jaringan otot tak tergantung atas glukosa untuk energinya tetapi pada asam-asam lemak. Alasan utama hal ini adalah bahwa membrane otot normal yang dalam keadaan istirahat hampir tak permeable terhadap glukosa kecuali bila serat otot dirangsang oleh insulin. Dan diantara waktu makan, jumlah insulin yang disekresikan terlalu kecil untuk meningkatkan masuknya insulin dalam jumlah bermakna kedalam sel-sel otot. Tetapi, pada dua keadaan (selama kerja fisik sedang dan berat, dan selama beberapa jam setelah makan), otot menggunakan sejumlah besar glukosa untuk energinya.
Penyimpanan Glikogen di dalam Otot
Bila setelah makan otot tidak bekerja, dan walaupun glukosa yang ditranspor ke dalam otot jumlahnya banyak, sebagian besar glukosa sampai batas 2 hingga 3 persen kemudian akan disimpan dalam bentuk glikogen otot daripada digunakan untuk energi. Kemudian glikogen dapat digunakan untuk energi oleh otot. Glikogen otot berbeda dari glikogen hati karena ia tidak dapat dikonversi kembali menjadi glukosa dan dilepaskan ke dalam cairan tubuh. Alasan untuk ini adalah bahwa tidak terdapat glukosa fosfatase di dalam sel-sel otot.
Mekanisme insulin meningkatkan transport glukosa melalui membrane sel otot
Insulin meningkatkan transport glukosa ke dalam sel-sel otot dalam cara yang sungguh berbeda dari cara meningkatkan transport ke dalam sel-sel hati. Transpor ke dalam hati terutama akibat mekanisme penangkapan yang disebabkan oleh fosforilasi glukosa atas pengaruh glukokinase. Tetapi ini hanya merupakan factor kecil dalam efek insulin untuk memindahkan glukosa ke dalam sel-sel otot. Yang lebih penting, insulin langsung mempengaruhi membrane sel otot untuk mempermudah transport glukosa. Transpor glukosa melalui membrane sel tidak terjadi melawan perbedaan konsentrasi. Yaitu sekali konsentrasi glukosa di dalam sel meningkat setinggi konsentrasi glukosa di luar, tak ada glukosa tambahan yang akan ditranspor ke dalam sel. Sehingga, proses transpor bukan salah satu difusi yang dipermudah, yang secara sederhana berarti bahwa pengangkut mempermudah difusi glukosa melalui membrane tetapi tidak dapat memberikan energi bagi proses transport untuk menyebabkan pemindahan glukosa melawan perbedaan energi.
11

Kurangnya Efek insulin atas ambilan dan penggunaan glukosa oleh otak
Otak memang berbeda dari kebanyakan jaringan tubuh lainnya, pada mana insulin mempunyai sedikit atau tak berefek atas ambilan atau penggunaan glukosa. Namun, sel-sel otak permeable bagi glukosa tanpa diintermediasi oleh insulin.
Efek insulin dalam meningkatkan ambilan, penyimpanan, dan penggunaan glukosa oleh hati
Salah satu efek insulin yang terpenting adalah menyimpan sebagian besar glukosa yang telah diabsorpsi sesudah makan di dalam hati dalam bentuk glikogen. Kemudian diantara waktu makan, bila insulin tak tersedia dan konsentrasi glukosa darah mulai turun, maka glikogen hati dipecah kembali menjadi glukosa, yang dilepaskan kembali ke darah untuk menjaga konsentrasi glukosa darah agar tidak turun terlalu rendah. Mekanisme insulin menyebabkan ambilan dan penyimpanan glukosa di dalam hati meliputi beberapa langkah yang hampir serentak:
1. Insulin menghambat fosforilase, enzim yang menyebabkan glikogen hati dipecah menjadi glukosa
2. insulin meningkatkan ambilan glukosa dari darah oleh sel-sel hati. Ini terjadi dengan meningkatkan aktivitas enzim glukokinase, yaitu enzim yang menyebabkan fosforilasi awal glukosa setelah glukosa berdifusi ke dalam sel-sel hati. Sekali terfosforilasi, glukosa tertangkap di dalam sel-sel hati karena glukosa yang telah terfosforilasi tidak dapat berdifusi kembali melalui membrane sel.
3. Insulin juga meningkatkan aktivitas enzim yang meningkatkan sintesis glikogenEfek dari kerja diatas adalah meningkatkan jumlah glikogen di dalam hati. Glikogen
dapat meningkat sekitar 5-6% dari massa hati, yang hampir sama dengan penyimpanan 100g glikogen.
Pelepasan glikogen dari hati diantara waktu makan
Setelah makan berlalu dan kadar glukosa mulai turun sampai kadar rendah, sekarang terjadi beberapa kejadian yang menyebabkan hati melepaskan glukosa kembali ke dalam darah yang bersirkulasi.
1. Penurunan glukosa darah menyebabkan pancreas menurun sekresi insulinnya2. kemudian kurangnya insulin membalikan semua efek yang telah dijelaskan sebelumnnya
untuk penyimpanan glikogen3. kurangnya insulin juga mengaktivasi enzim fosforilase, yang menyebabkan pemecahan
glikogen menjadi glukosa fosfat4. Enzim glukosa fosfatase menyebabkan gugusan fosfat pecah dari glukosa dan ini
memungkinkan glukosa bebas berdifusi kembali ke darah.Hati mengambil glukosa dari darah bila glukosa berlebihan setelah makan dan
mengembalikannya ke dalam darah bila glukosa diperlukan diantara waktu makan.
Efek insulin lainnya atas metabolisme karbohidrat di dalam hati
12

Insulin juga meningkatkan konversi glukosa hati menjadi asam lemak dan asam lemak ini diangkut lagi ke dalam jaringan adipose serta disimpan sebagai lemak. Insulin juga menghambat glukoneogenesis. Ini terutama terjadi dengan menurunkan jumlah dan aktivitas enzim hati yang diperlukan untuk glukoneogenesis.
B. Efek Insulin pada Metabolisme Lemak
Efek Insulin dalam sintesis dan penyimpanan lemak
Beberapa faktor yang menyebabkan peningkatan sintesis asam lemak di dalam hati meliputi:
1. Insulin meningkatkan transport glukosa ke dalam sel-sel hati. Kemudian glukosa dipecah menjadi piruvat di dalam jalur glikolisis dan kemudian piruvat dikonversi menjadi Asetil CoA (substrat untuk sintesis asam lemak)
2. Kelebihan ion sitrat dan isositrat terbentuk oleh siklus asam sitrat bila glukosa dalam jumlah berlebihan digunakan untuk energi. Kemudian ion ini mempunyai efek langsung dalam mengaktivasi asetil CoA karboksilase, enzim yang diperlukan untuk memulai stadium pertama sintesis asam lemak.
3. Kemudian asam lemak ditransport dari hepar ke sel-sel adipose, untuk disimpan.
Efek insulin atas penyimpanan lemak di dalam sel-sel adipose
1. Insulin menghambat kerja lipase yang sensitive hormone. Karena lipase merupakan enzim yang menyebabkan hidrolisis trigliserida di dalam sel-sel lemak, sehingga pelepasan asam lemak ke dalam darah yang bersirkulasi dihambat.
2. Insulin meningkatkan transport ke dalam sel-sel lemak dalam jalan yang sama seperti meningkatkan transpor glukosa ke dalam sel-sel otot. Glukosa juga membentuk zat lain yang penting untuk penyimpanan lemak. Selama proses glikosis glukosa, sejumlah besar zat α-gliserofosfat terbentuk. Zat ini memberikan gliserol yang terikat dengan asam lemak untuk membentuk trigliserida, bentuk lemak yang disimpan di dalam sel-sel adipose.
Peningkatan katabolisme lemak karena defisiensi insulin
1. Lipolisis lemak yang disimpan dan pelepasan asam lemak bebas selama defisiensi insulinEfek yang terpenting adalah bahwa enzim lipase yang sensitive hormone di dalam
sel-sel lemakmenjadi sangat teraktivasi. Ini menyebabkan hidrolisis trigliserida yang disimpan, melepaskan sejumlah besar asam lemak dan gliserol ke dalam darah. Akibatnya, konsentrasi asam lemak bebas plasma meningkat dalam beberapa menit sampai beberapa jam. Kemudian asam lemak bebas ini menjadi substrat energi utama yang digunakan oleh semua jaringan tubuh di samping otak.
2. Defisiensi insulin meningkatkan konsentrasi fosfolipid dan kolesterol plasmaKelebihan asam lemak di plasma akibat defisiensi insulin juga memacu
pengubahan sejumlah asam lemak menjadi fosfolipid dan kolesterol di hati, yang merupakan dua zat utama yang dihasilkan dari metabolisme lemak. Kedua zat ini bersama dengan beberapa
13

trigliserida yang terbentuk di dalam hati, kemudian dikeluarkan ke dalam darah di dalam lipoprotein. Konsentrasi lipid yang tinggi, terutama konsentrasi kolesterol yang tinggi, menyebabkan cepatnya timbul aterosklerosis pada pasien dengan diabetes yang serius.
3. Pemakaian lemak yang berlebihan selama tidak ada insulin menyebabkan ketosis dan asidosis
Defisiensi insulin juga menyebabkan kelebihan pembentukan asam asetoasetat di dalam sel hati. Ini akibat cepatnya pemecahan asam lemak di dalam hati untuk membentuk asetil CoA dalam jumlah yang sangat banyak. Sebagian asetil CoA ini dapat digunakan untuk energi tetapi kelebihannya dikondensasi menjadi asam asetoasetat, yang sebaliknya akan dilepaskan ke dalam darah. Sejumlah asam asetoasetat juga dikonversi menjadi asam β-hidroksibutirat dan aseton. Kedua zat ini bersama dengan asma asetoasetat dinamai badan keton dan adanya dalam jumlah besar pada cairan tubuh dinamai ketosis.
C. Efek Insulin pada Metabolisme Protein dan Pertumbuhan
Insulin meningkatkan sintesis dan penyimpanan protein
1. Insulin merangsang pengangkutan sejumlah besar asam amino ke dalam selDiantara asam amino yang banyak diangkut adalah valin, leusin, isoleusin, tirosin, dan fenilalanin. Insulin bersama-sama dengan hormone pertumbuhan mempunyai kemampuan untuk meningkatkan ambilan asam amino ke dalam sel.
2. Insulin meningkatkan translasi RNA messengerDengan cara yang belum dpat dijelaskan, insulin dapat menyalakan mesin ribosom. Tanpa insulin, ribosom benar-benar berhenti bekerja.
3. Insulin meningkatkan kecepatan transkripsi rangkaian genetic DNA yang terpilihHal ini menyebabkan peningkatan jumlah RNA dan beberapa sintesis protein, terutama mengaktifkan sejumlah besar enzim untuk penyimpanan karbohidrat, lemak, dan protein.
4. Insulin menghambat proses katabolisme proteinHal ini akan mengurangi kecepatan pelepasan asam amino dari sel, khususnya dari sel-sel otot
5. Di dalam hati, insulin menekan kecepatan glukoneogenesisHal ini dilakukan dengan cara mengurangi aktivitas enzim yang memacu glukoneogenesis. Karena zat terbanyak yang digunakan untuk sintesis glukosa dengan proses glukoneogenesis adalah asam amino plasma, maka supresi glukoneogenesis ini menghemat asam amino dari cadangan protein tubuh.
Tidak adanya insulin menyebabkan berkurangnya protein dan peningkatan asam amino plasma
Bila tidak ada insulin, hampir seluruh proses penyimpanan protein menjadi terhenti sama sekali. Proses katabolisme protein akan meningkat, sintesis protein berhenti, dan sejumlah besar asam amino dibuang ke dalam plasma. Konsentrasi asam amino dalam plasma sangat meningkat, dan sebagian besar kelebihan asam amino akan langsung dipergunakan sebagai sumber enrgi
14

Gambar 1. Struktur Insulin
Sumber: http://diabetesmanager.pbworks.com/f/figure1a%20%26%20b.gif
atau menjadi substrat dalam proses glukoneogenesis. Pemecahan asam amino ini juga meningkatkan ekskresi ureum dalam urin.
Insulin dan hormone pertumbuhan berinteraksi secara sinergis untuk memacu pertumbuhan
LI 3. Memahami dan Menjelaskan Biokimia Insulin
STRUKTUR INSULIN
Insulin adalah monomer yang terdiri dari dua rantai polipeptida: rantai A memiliki 21 asam amino dan rantai B memiliki 30 asam amino (pada manusia). Dua jembatan disulfida (residu A7 ke B7, dan A20 ke B19) kovalen menambatkan rantai, dan rantai A mengandung jembatan disulfida internal (residu A6 ke A11). Terutama, posisi tiga ikatan disulfida ini tidak bervariasi dalam bentuk mamalia insulin.
SINTESIS INSULIN
Insulin adalah hormon yang secara eksklusif diproduksi oleh sel beta pankreas. Sel beta yang terletak di pankreas dalam kelompok yang dikenal sebagai pulau Langerhans. Insulin adalah protein kecil dan diproduksi sebagai bagian dari protein yang lebih besar untuk memastikan lipatan dengan benar. Dalam perakitan protein insulin, transkrip mRNA diterjemahkan menjadi protein aktif yang disebut preproinsulin.
Preproinsulin berisi urutan sinyal amino-terminal yang diperlukan agar hormon prekursor untuk melewati membran dari retikulum endoplasma (ER) untuk pengolahan pasca-translasi. Setelah
15

memasuki ER, urutan sinyal preproinsulin, sekarang tidak berguna, yang proteolitik dihapus untuk membentuk proinsulin. Setelah pembentukan pasca-translasi dari tiga ikatan disulfida penting terjadi, peptidases tertentu proinsulin membelah. Produk akhir dari biosintesis adalah insulin matang dan aktif. Akhirnya, insulin dikemas dan disimpan dalam butiran sekretori, yang menumpuk di sitoplasma, sampai dipicu untuk dikeluarkan.
SEKRESI INSULIN
Proses di mana insulin dilepaskan dari sel-sel beta, dalam menanggapi perubahan dalam konsentrasi glukosa darah, adalah mekanisme yang kompleks dan menarik yang menggambarkan sifat rumit dari regulasi insulin. Tipe 2 transporter glukosa (GLUT2) memediasi masuknya glukosa ke dalam sel beta. Sebagai bahan bakar baku untuk glikolisis, glukosa terfosforilasi oleh glukokinase enzim. Glukosa diubah menjadi efektif ini terjebak dalam sel-sel beta dan selanjutnya dimetabolisme untuk membuat ATP, molekul energi pusat.
Rasio ATP:ADP meningkat menyebabkan saluran jembatan kalium ATP dalam membran sel untuk menutup, mencegah ion kalium dari yang didorong melewati membran sel. Berikutnya kenaikan muatan positif di dalam sel, karena peningkatan konsentrasi ion kalium, menyebabkan depolarisasi sel. Efek bersih adalah aktivasi jembatan saluran kalsium tegangan, yang ion kalsium transportasi ke dalam sel. Peningkatan cepat konsentrasi kalsium intraseluler memicu ekspor butiran insulin dengan proses yang dikenal sebagai eksositosis. Hasil akhir adalah ekspor insulin dari sel beta dan difusi ke dalam pembuluh darah di dekatnya. Kapasitas vaskular luas sekitar pulau pankreas menjamin difusi cepat dari insulin (dan glukosa) antara sel-sel beta dan pembuluh darah.
RESEPTOR INSULIN
16

Reseptor insulin unik karena merupakan kompleks heterotetrameric terdiri dari dua ekstraseluler α-peptida yang disulfida terikat dua β-peptida transmembran. Kedua subunit α- dan β- dari kompleks reseptor berasal dari sebuah gen tunggal. Pengolahan reseptor ini mengingatkan pengolahan protein preproinsulin yang mengarah ke dua peptida (A dan B) disulfida terikat bersama untuk membentuk insulin bioaktif.
Gambar 3. Reseptor Insulin. Sumber: http://themedicalbiochemistrypage.org/images/insulin-receptor.png
AKTIVITAS INSULIN
Beberapa peran insulin Ketika insulin berikatan dengan reseptornya memicu autofosforilasi reseptor yang menghasilkan situs docking untuk protein substrat reseptor insulin (IRS-1-IRS4). Protein IRS pada gilirannya memicu aktivasi beragam protein sinyal pentransduksi. Hasil akhir aktivasi reseptor insulin bervariasi dan dalam banyak kasus sel jenis tertentu tetap mencakup perubahan dalam metabolisme, fluks ion, translokasi protein, tingkat transkripsi, dan sifat pertumbuhan sel responsif.
PDE3B = phosphodiesterase 3B (juga disebut adiposit cAMP fosfodiesterase), GS = glikogen sintase, HSL = hormon lipase sensitif, ACC = asetil-CoA karboksilase, liase ACL = ATP-sitrat.
17

Gambar 4. Aktivitas Insulin. Sumber: http://themedicalbiochemistrypage.org/images/insulin-receptor-signaling.png
LI 4. Memahami dan Menjelaskan Diabetes Melitus
4.1 Definisi
Diabetes mellitus (DM) adalah suatu penyakit atau gangguan metabolisme kronis dengan multi etiologi yang ditandai dengan tingginya kadar gula darah disertai dengan gangguan metabolisme karbohidrat, lipid dan protein sebagai akibat insufisiensi fungsi insulin (Ditjen Bina Farmasi dan Alkes, 2005).
4.2 Epidemiologi
Diabetes Mellitus telah dikategorikan sebagai penyakit global oleh Organisasi Kesehatan Dunia atau World Health Organization(WHO). Jumlah penderita DM ini meningkat di setiap negara. Berdasarkan data dari WHO (2006), diperkirakan terdapat 171 juta orang di dunia menderita diabetes pada tahun 2000 dan diprediksi akan meningkat menjadi 366 juta penderita pada tahun 2030. Sekitar 4,8 juta orang di dunia telah meninggal akibat DM. Setengah dari penderita DM ini tidak terdiagnosis.
Sepuluh besar negara dengan prevalensi DM tertinggi di dunia pada tahun 2000 adalah India, Cina, Amerika, Indonesia, Jepang, Pakistan, Rusia, Brazil, Italia, dan Bangladesh. Pada tahun 2030 India, Cina, dan Amerika diprediksikan tetap menduduki posisi tiga teratas negara dengan prevalensi DM tertinggi. Sementara, Indonesia diprediksikan akan tetap berada dalam sepuluh besar negara dengan prevalensi DM tertinggi pada tahun 2030 (Wild, Roglic, Green, et al, 2004)
Indonesia menduduki posisi keempat dunia setelah India, Cina, dan Amerika dalam prevalensi DM. Pada tahun 2000 masyarakat Indonesia yang menderita DM adalah sebesar 8,4 juta jiwa dan diprediksi akan meningkat pada tahun 2030 menjadi 21,3 juta jiwa. Data ini menunjukkan bahwa angka kejadian DM tidak hanya tinggi di negara maju tetapi juga di negara berkembang, seperti Indonesia. Berdasarkan hasil Riset Kesehatan Dasar (RISKESDAS) pada
18

tahun 2007 menunjukkan bahwa secara nasional, prevalensi DM berdasarkan diagnosis oleh tenaga kesehatan dan adanya gejala adalah sebesar 1,1%. Sedangkan prevalensi berdasarkan hasil pengukuran kadar gula darah pada penduduk umur lebih dari lima belas tahun di daerah perkotaan adalah sebesar 5,7% (Depkes, 2008).
4.3 Etiologi
DM TIPE 1
Etiologi DM tipe 1 diakibatkan oleh kerusakan sel beta pankreas karena paparan agen infeksi atau lingkungan, yaitu racun, virus (rubella kongenital, mumps, coxsackievirus dan cytomegalovirus) dan makanan (gula, kopi, kedelai, gandum dan susu sapi).
Beberapa teori ilmiah yang menjelaskan penyebab diabetes mellitus tipe 1 sebagai berikut:
1. Hipotesis sinar matahari
Teori yang paling terakhir adalah "hipotesis sinar matahari," yang menyatakan bahwa waktu yang lama dihabiskan dalam ruangan, dimana akan mengurangi paparan sinar matahari kepada anak-anak, yang akan mengakibatkan berkurangnya kadar vitamin D. Bukti menyebutkan bahwa vitamin D memainkan peran integral dalam sensitivitas dan sekresi insulin. Berkurangnya kadar vitamin D, dan jarang terpapar dengan sinar matahari, dimana masing-masing telah dikaitkan dengan peningkatan risiko diabetes mellitus tipe 1.
2. Hipotesis higiene "Hipotesis kebersihan"
Teori ini menyatakan bahwa kurangnya paparan dengan prevalensi patogen, dimana kita menjaga anak-anak kita terlalu bersih, dapat menyebabkan hipersensitivitas autoimun, yaitu kehancuran sel beta yang memproduksi insulin di dalam tubuh oleh leukosit. Dalam penelitian lain, peneliti telah menemukan bahwa lebih banyak eksposur untuk mikroba dan virus kepada anak-anak, semakin kecil kemungkinan mereka menderita penyakit reaksi hipersensitif seperti alergi. Penelitian yang berkelanjutan menunjukkan bahwa "pelatihan" dari sistem kekebalan tubuh mungkin berlaku untuk pencegahan tipe 1 diabetes. Kukrija dan Maclaren menunjukkan bahwa pencegahan diabetes tipe 1 mungkin yang akan datang melalui penggunaan imunostimulasi, yakni memaparkankan anak-anak kepada bakteri dan virus yang ada di dunia, tetapi yang tidak menyebabkan efek samping imunosupresi.
3. Hipotesis Susu Sapi
Teori ini menjelaskan bahwa eksposur terhadap susu sapi dalam susu formula pada 6 bulan pertama pada bayi dapat menyebabkan kekacauan pada sistem kekebalan tubuh dan meningkatkan risiko untuk mengembangkan diabetes mellitus tipe 1 di kemudian hari. Dimana protein susu sapi hampir identik dengan protein pada permukaan sel beta pankreasyang memproduksi insulin, sehingga mereka yang rentan dan peka terhadap susu sapi maka akan dire
19

spon oleh leukosit, dan selanjutnya akan menyerang sel sendiri yang menyebabkan kerusakan sel beta pankreas sehingga terjadi dibetes mellitus tipe 1. Peningkatan pemberian ASI di 1980 tidak menyebabkan penurunan terjadinya diabetes tipe 1, tetapi terjadi peningkatan dua kali lipat diabetes mellitus tipe 1. Namun, kejadian diabetes tipe 1 lebih rendah pada bayi yang diberi ASI selama 3 bulan.
4. Hipotesis POP
Hipotesis ini menjelaskan bahwa eksposur terhadap polutan organik yang persisten (POP) meningkatkan risiko kedua jenis diabetes. Publikasi jurnal oleh Institut Nasional Ilmu Kesehatan Lingkungan menunjukkan peningkatan yang signifikan secara statistik dalam tingkat rawat inap untuk diabetes dari populasi yang berada di tempat Kode ZIP yang mengandung limbah beracun.
5. Hipotesis Akselerator
Sebuah teori yang menunjukkan bahwa tipe 1 diabetes merupakan bagian sederhana dari kontinum yang sama dari tipe 2, tetapi muncul lebih dulu. Hipotesis akselerator menyatakan bahwa peningkatan berat dan tinggi anak-anak pada abad terakhir ini telah "dipercepat", sehingga kecenderungan mereka untuk mengembangkan tipe 1 dengan menyebabkan sel beta di pankreas di bawah tekanan untuk produksi insulin. Beberapa kelompok mendukung teori ini, tetapi hipotesis ini belum merata diterima oleh profesional diabetes.
Faktor yang mempengaruhi DM TIPE 1:
Faktor genetik Penderita diabetes tidak mewarisi diabetes tipe I itu sendiri; tetapimewarisi suatu predisposisi atau kecenderungan genetik ke arah terjadinyaDM tipe I. Kecenderungan genetik ini ditemukan pada individu yangmemiliki tipe antigen HLA.
Faktor-faktor imunologiAdanya respons otoimun yang merupakan respons abnormal dimanaantibodi terarah pada jaringan normal tubuh dengan cara bereaksi terhadap jaringan tersebut yang dianggapnya seolah-olah sebagai jaringan asing.Yaitu otoantibodi terhadap sel-sel pulau Langerhans dan insulin endogen.
Faktor lingkunganVirus atau toksin tertentu dapat memicu proses otoimun yangmenimbulkan destruksi selbeta.
DM TIPE 2
Faktor risiko diabetes tipe 2 terbagi atas:
Faktor risiko yang tidak dapat diubah seperti ras, etnik, riwayat keluarga dengan diabetes, usia > 45 tahun, riwayat melahirkan bayi dengan berat badan lahir lebih dari 4 kg, riwayat pernah menderita DM Gestasional dan riwayat berat badan lahir rendah < 2,5 kg.
Faktor risiko yang dapat diperbaiki seperti berat badan lebih (indeks massa tubuh > 23kg/m2, kurang aktivitas fisik, hipertensi(>140/90 mmHg), dislipidemia (HDL <35 mg/dl dan atau trigliserida > 250 mg/dl dan diet tinggi gula rendah serat.
20

Faktor risiko lain yang terkait dengan risiko diabetes seperti penderita sindrom ovarium poli-kistik, atau keadaan klinis lain yang terkait dengan resitensi insulin, sindrom metabolik, riwayat toleransi glukosa terganggu (IGT)/glukosa darah puasa terganggu (IFG) dan riwayat penyakit kardiovascular (stroke, penyempitan pembuluh darah koroner jantung, pembuluh darah arteri kaki).
a. Genetik atau Faktor Keturunan
DM cenderung diturunkan atau diwariskan, dan tidak ditularkan. Faktor genetis memberi peluang besar bagi timbulnya penyakit DM. Anggota keluarga penderita DM memiliki kemungkinan lebih besar menderita DM dibandingkan dengan anggota keluarga yang tidak menderita DM. Apabila ada orangtua atau saudara kandung yang menderita DM, maka seseorang tersebut memiliki resiko 40 % menderita DM. DM Tipe 1 lebih banyak dikaitkan dengan faktor keturunan dibandingkan dengan DM Tipe 2. Sekitar 50 % pasien DM Tipe 1 mempunyai orang tua yang juga menderita DM, dan lebih dari sepertiga pasien mempunyai saudara yang juga menderita DM. Pada penderita DM Tipe 2 hanya sekitar 3-5 % yang mempunyai orangtua menderita DM juga.
Pada DM tipe 1, seorang anak memiliki kemungkinan 1:7 untuk menderita DM bila salah satu orang tua anak tersebut menderita DM pada usia < 40 tahun dan 1:13 bila salah satu orang tua anak tersebut menderita DM pada usia ≥ 40 tahun. Namun bila kedua orang tuanya menderita DM tipe 1, maka kemungkinan menderita DM adalah 1:2.
a. Usia
DM dapat terjadi pada semua kelompok umur, terutama ≥ 40 tahun karena resiko terkena DM akan meningkat dengan bertambahnya usia dan manusia akan mengalami penurunan fisiologis yang akan berakibat menurunnya fungsi endokrin pankreas untuk memproduksi insulin. DM tipe 1 biasanya terjadi pada usia muda yaitu pada usia <40 tahun, sedangkan DM tipe 2 biasanya terjadi pada usia ≥ 40 tahun. Di negara-negara barat ditemukan 1 dari 8 orang penderita DM berusia di atas 65 tahun, dan 1 dari penderita berusia di atas 85 tahun.
Menurut penelitian Handayani di RS Dr. Sardjito Yogyakarta (2005) penderita DM Tipe 1 mengalami peningkatan jumlah kasusnya pada umur < 40 tahun (2,7%), dan jumlah kasus yang paling banyak terjadi pada umur 61-70 tahun (48 %). Menurut hasil penelitian Renova di RS. Santa Elisabeth tahun 2007 terdapat 239 orang (96%) pasien DM berusia ≥ 40 tahun dan 10 orang (4%) yang berusia < 40 tahun.
c. Jenis Kelamin
Perempuan memiliki resiko lebih besar untuk menderita Diabetes Mellitus, berhubungan dengan paritas dan kehamilan, dimana keduanya adalah faktor resiko untuk terjadinya penyakit DM. Dalam penelitian Martono dengan desain cross sectional di Jawa Barat tahun 1999 ditemukan bahwa penderita DM lebih banyak pada perempuan (63%) dibandingkan laki-laki
21

(37%). Demikian pula pada penelitian Media tahun 1998 di seluruh rumah sakit di Kota Bogor, proporsi pasien DM lebih tinggi pada perempuan (61,8%) dibandingkan pasien laki-laki (38,2%)
d. Pola Makan dan Kegemukan (Obesitas)
Perkembangan pola makan yang salah arah saat ini mempercepat peningkatan jumlah penderita DM di Indonesia. Makin banyak penduduk yang kurang menyediakan makanan yang berserat di rumah. Makanan yang kaya kolesterol, lemak, dan natrium (antara lain dalam garam dan penyedap rasa) muncul sebagai tren menu harian, yang ditambah dengan meningkatnya konsumsi minuman yang kaya gula.
Kegemukan adalah faktor resiko yang paling penting untuk diperhatikan, sebab meningkatnya angka kejadian DM Tipe 2 berkaitan dengan obesitas. Delapan dari sepuluh penderita DM Tipe 2 adalah orang-orang yang memiliki kelebihan berat badan. Konsumsi kalori lebih dari yang dibutuhkan tubuh menyebabkan kalori ekstra akan disimpan dalam bentuk lemak. Lemak ini akan memblokir kerja insulin sehingga glukosa tidak dapat diangkut ke dalam sel dan menumpuk dalam peredaran darah. Seseorang dengan IMT (Indeks Massa Tubuh) 30 kg/m2 akan 30 kali lebih mudah terkena DM dari pada seseorang dengan IMT normal (22 Kg/m2). Bila IMT ≥ 35 kg/m2, kemungkinan mengidap DM menjadi 90 kali lipat. Melakukan aktivitas fisik seperti olahraga secara teratur dapat membuang kelebihan kalori sehingga dapat mencegah terjadinya kegemukan dan kemungkinan untuk menderita DM. Pada saat tubuh melakukan aktivitas/gerakan, maka sejumlah gula akan dibakar untuk dijadikan tenaga gerak. Sehingga sejumlah gula dalam tubuh akan berkurang dan kebutuhan akan hormon insulin juga akan berkurang. Pada orang yang jarang berolah raga zat makanan yang masuk ke dalam tubuh tidak dibakar, tetapi hanya akan ditimbun dalam tubuh sebagai lemak dan gula. Proses perubahan zat makanan dan lemak menjadi gula memerlukan hormon insulin. Namun jika hormon insulin kurang mencukupi, maka akan timbul gejala DM.
(Tjokroprawiro, Askandar. 2003. Diabetes Mellitus - Klasifikasi, Diagnosis dan Dasar-dasar Terapi. Jakarta : PT Garamedia Pustaka Utama)
(Price, Sylvia A. 2005. Patofisiologi: Konsep Klinis Proses-Proses Penyakit. Jakarta: EGC)
4.4 Klasifikasi
Menurut American Diabetes Association (ADA,2013), klasifikasi diabetes meliputi empat kelas klinis :
Diabetes Mellitus tipe 1 Hasil dari kehancuran sel β pankreas, biasanya menyebabkan defisiensi insulin yang absolut. Proses destruksi ini dapat terjadi karena proses imunologik maupun idiopatik
Diabetes Mellitus tipe 2Hasil dari gangguan sekresi insulin yang progresif yang menjadi latar belakang terjadinya resistensi insulin
22

Diabetes tipe spesifik lainMisalnya : gangguan genetik pada fungsi sel β, gangguan genetik pada kerja insulin, penyakit eksokrin pankreas (seperti cystic fibrosis), dan yang dipicu oleh obat atau bahan kimia (seperti dalam pengobatan HIV/AIDS atau setelah transplantasi organ).
Gestational Diabetes MellitusPada beberapa pasien tidak dapat dengan jelas diklasifikasikan sebagai diabetes tipe 1 atau tipe 2. Presentasi klinis dan perkembangan penyakit bervariasi jauh dari kedua jenis diabetes. Kadang-kadang, pasien yang dinyatakan memilki diabetes tipe 2 dapat hadir dengan ketoasidosis. Demikian pula, pasien dengan tipe 1 diabetes mungkin memiliki onset terlambat dan memperlambat perkembangan penyakit walaupun memilki fitur penyakit autoimun. Kesulitan seperti itu pada diagnosis mungkin terjadi pada anak-anak, remaja, dan dewasa. Diagnosis yang benar dapat menjadi lebih jelas dari waktu ke waktu.
Karakteristik Diabetes tipe I Diabetes tipe IIKadar Sekresi Insulin Tidak ada/hampir ada Mungkin normal atau di atas
normalUsia Awitan Tipikal Anak DewasaPersentase Pengidap 10%-20% 80%-90%Defek Mendasar Kerusakan sel β Berkurangnya kepekaan sel
sasaran insulinTerapi Penyuntikan insulin,
pengaturan diet, olahragaKontrol diet dan penurunan berat, olahraga, kadang obat hipoglikemik oral
4.5 Patofisiologi
Diabetes Melitus tipe 1
Pada pulau Langerhans kelenjar pankreas terdapat beberapa tipe sel, yaitu sel β, sel α dan sel σ. Sel-sel β memproduksi insulin, sel-sel α memproduksi glukagon, sedangkan sel-sel σ memproduksi hormon somastatin. Namun demikian serangan autoimun secara selektif menghancurkan sel-sel β. Destruksi otoimun dari sel-sel β pulau Langerhans kelenjar pankreas langsung mengakibatkan defesiensi sekresi insulin. Defesiensi insulin inilah yang menyebabkan gangguan metabolisme yang menyertai DM Tipe 1. Selain defesiensi insulin, fungsi sel-sel α kelenjar pankreas pada penderita DM tipe 1 juga menjadi tidak normal. Pada penderita DM tipe 1 ditemukan sekresi glukagon yang berlebihan oleh sel-sel α pulau Langerhans. Secara normal, hiperglikemia akan menurunkan sekresi glukagon, tapi hal ini tidak terjadi pada penderita DM Universitas Sumatera Utara tipe 1, sekresi glukagon akan tetap tinggi walaupun dalam keadaan hiperglikemia, hal ini memperparah kondisi hiperglikemia. Salah satu manifestasi dari keadaan ini adalah cepatnya penderita DM tipe 1 mengalami ketoasidosis diabetik apabila tidak mendapatkan terapi insulin.
(http://repository.usu.ac.id/bitstream/123456789/35195/4/Chapter%20II.pdf)
23

Diabetes Melitus tipe 2
Diabetes tipe 2 adalah multifaktorial kompleks prototipikal penyakit. Faktor lingkungan, seperti gaya hidup menetap dan kebiasaan diet, tegas berperan, seperti yang dijelaskan dalam pembahasan berikutnya dari asosiasi dengan obesitas.
Faktor genetik juga terlibat dalam patogenesis, seperti dibuktikan dengan tingkat konkordansi penyakit dari 35% sampai 60% pada kembar monozigot dibandingkan dengan hampir setengah di dizigotik kembar. Konkordansi seperti ini bahkan lebih besar dari pada tipe 1 diabetes, menunjukkan mungkin komponen genetik yang lebih besar pada diabetes tipe 2. Bukti tambahan untuk genetic dasar telah muncul dari genomewide skala besar baru-baru ini studi asosiasi, yang telah mengidentifikasi lebih dari lokus selusin kerentanan disebut "diabetogenic" gen. Tidak seperti diabetes tipe 1, namun, penyakit ini tidak terkait dengan gen yang terlibat dalam toleransi kekebalan tubuh dan regulasi (misalnya, HLA, CTLA4), dan bukti secara autoimun adalah kurang. Kedua cacat metabolik yang menjadi ciri tipe 2 diabetes (1) penurunan kemampuan jaringan perifer untuk merespon insulin (resistensi insulin) dan (2) disfungsi sel beta yang dimanifestasikan sebagai sekresi insulin yang tidak memadai di wajah resistensi insulin
24

dan hiperglikemia (Gbr. 19-23).Resistensi insulin mendahului perkembangan hiperglikemia dan biasanya disertai dengan sel beta kompensasi hyperfunction dan hiperinsulinemia pada tahap awal dari evolusi diabetes.
Resistensi Insulin
Resistensi insulin didefinisikan sebagai kegagalan jaringan target untuk merespon secara normal terhadap insulin. Hal ini menyebabkan penyerapan penurunan glukosa dalam otot, mengurangi glikolisis dan oksidasi asam lemak di hati, dan ketidakmampuan untuk menekan glukoneogenesis hepatik. Berbagai cacat fungsional telah dilaporkan dalam jalur sinyal insulin dalam keadaan resistensi insulin (misalnya, mengurangi aktivasi tergantung fosforilasi reseptor insulin dan komponen hilir), yang melemahkan sinyal transduksi. Beberapa faktor bermain sebagai peran penting dalam pengembangan insulin daya tahan obesitas.
Obesitas dan Insulin Resistance
25

Hubungan obesitas dengan diabetes tipe 2 telah diakui selama beberapa dekade, dengan obesitas viseral yang umum di sebagian besar pasien yang terkena. Resistensi insulin hadir bahkan dengan obesitas sederhana tanpa ditemani oleh hiperglikemia, menunjukkan kelainan mendasar dari sinyal insulin dalam keadaan kelebihan lemak. Bahkan, sindrom metabolik jangka telah diterapkan pada konstelasi temuan didominasi oleh obesitas viseral, yang disertai dengan resistensi insulin, intoleransi glukosa, dan faktor risiko kardiovaskular seperti hipertensi dan abnormal profil lipid. Dengan tidak adanya penurunan berat badan dan gaya hidup modifikasi, orang dengan sindrom metabolik memiliki risiko yang signifikan untuk pengembangan frank diabetes tipe 2, menggarisbawahi pentingnya obesitas pada patogenesis penyakit ini. Risiko diabetes meningkat sebagai indeks massa tubuh (ukuran kandungan lemak tubuh) meningkat, menunjukkan hubungan dosis-respons antara lemak tubuh dan resistensi insulin. Meskipun banyak rincian yang disebut adipo-insulin sumbu tetap harus dijelaskan, pengakuan dari beberapa jalur yang diduga mengarah ke resistensi insulin telah meningkat secara substansial
Peran asam lemak bebas yang berlebih (FFA): studi cross-sectional telah menunjukkan korelasi terbalik antara FFA plasma puasa dan sensitivitas insulin. Tingkat trigliserida intraseluler sering nyata meningkat pada jaringan otot dan hati pada orang gemuk,
26

mungkin karena kelebihan beredar FFA disimpan dalam organ-organ ini. Trigliserida intraseluler dan produk metabolisme asam lemak berpotensi menghambat sinyal insulin dan hasilnya dalam keadaan resistensi insulin yang diperoleh. Efek lipotoxic dari FFA dimediasi melalui penurunan aktivitas dari protein insulin-sinyal kunci.
Peran peradangan: Selama beberapa tahun terakhir, peradangan telah muncul sebagai pemain utama dalam patogenesis diabetes tipe 2. Sekarang diketahui bahwa permisif lingkungan inflamasi (dimediasi tidak oleh proses autoimun seperti pada diabetes tipe 1 melainkan oleh sitokin proinflamasi yang disekresikan dalam menanggapi kelebihan gizi seperti FFA) hasil di kedua perangkat resistensi insulin dan sel beta disfungsi (lihat nanti). FFA kelebihan dalam makrofag dan sel-sel beta dapat melibatkan inflammasome, kompleks sitoplasma multiprotein yang mengarah ke sekresi sitokin interleukin IL-1β (Bab 2). IL-1β, pada gilirannya, memediasi sekresi sitokin pro-inflamasi tambahan dari makrofag, pulau, dan sel-sel lain yang dilepaskan ke dalam sirkulasi dan bertindak di situs utama aksi insulin untuk mempromosikan resistensi insulin. Dengan demikian, kelebihan FFA dapat menghambat sinyal insulin langsung dalam jaringan perifer, serta secara tidak langsung melalui pelepasan sitokin proinflamasi. Tidak mengherankan, sekarang ada beberapa uji coba yang sedang berlangsung antagonis sitokin (terutama dari IL-1β) pada pasien dengan diabetes tipe 2.
Peran adipokines: Jaringan adiposa bukan hanya depot penyimpanan pasif untuk lemak; dapat beroperasi sebagai organ endokrin fungsional, melepaskan disebut adipokines dalam menanggapi rangsangan ekstraseluler atau perubahan status metabolik. Dengan demikian, adiposit juga melepaskan IL-1β dan sitokin proinflamasi lainnya ke dalam sirkulasi dalam menanggapi FFA berlebihan, yang mempromosikan resistensi insulin perifer. Sebaliknya, adiponektin adalah adipokine dengan aktivitas kepekaan insulin, yang mungkin bertindak dengan meredam respon inflamasi.
Peroxisome proliferator-diaktifkan reseptor-γ (PPAR): PPAR merupakan faktor reseptor dan transkripsi nuklir dinyatakan dalam jaringan adiposa dan memainkan peran mani dalam diferensiasi adiposit. Sebuah kelas obat antidiabetes dikenal sebagai thiazolidinediones bertindak sebagai ligan agonis untuk PPAR? Dan meningkatkan sensitivitas insulin. Aktivasi PPAR mempromosikan sekresi adipokines antihyperglycemic seperti adiponektin, dan menggeser FFA depositionof terhadap jaringan adiposa dan jauh dari hati dan otot rangka.
Disfungsi sel beta pada diabetes tipe 2 mencerminkan ketidakmampuan sel-sel ini untuk menyesuaikan diri dengan tuntutan jangka panjang resistensi insulin perifer dan sekresi insulin meningkat. Dalam keadaan resistensi insulin, sekresi insulin awalnya lebih tinggi untuk setiap tingkat glukosa dibandingkan kontrol. Negara hyperinsulinemic ini adalah kompensasi untuk resistensi perifer dan sering dapat mempertahankan glukosa plasma normal untuk tahun.
Akhirnya, bagaimanapun, kompensasi sel beta menjadi tidak memadai, dan ada perkembangan hiperglikemia, yang disertai dengan kerugian mutlak dalam massa sel beta.
27

Mekanisme molekuler yang mendasari disfungsi sel beta pada diabetes tipe 2 yang multifaktorial dan dalam banyak kasus tumpang tindih dengan orang-orang yang terlibat dalam resistensi insulin. Dengan demikian, kelebihan gizi seperti lemak dan glukosa dapat mempromosikan sekresi sitokin pro-inflamasi dari sel beta, yang mengarah ke perekrutan sel mononuklear (makrofag dan sel T) ke dalam pulau, sehingga produksi sitokin lebih lokal.
Konsekuensi dari mikro inflamasi yang abnormal ini disfungsi beta sel dan, pada akhirnya, kematian sel beta. Penggantian amiloid dari pulau merupakan temuan karakteristik pada orang dengan diabetes tipe lama 2 dan hadir di lebih dari 90% dari pulau diabetes diperiksa (lihat nanti). The islet amyloid polypetide (IAPP), juga dikenal sebagai amylin, disekresikan oleh sel-sel beta dalam hubungannya dengan insulin, dan hasil agregasi normal di amiloid. IAPP juga terlibat inflammasome dan mempromosikan sekresi IL-1β, sehingga mempertahankan serangan peradangan pada sel beta yang masih hidup bahkan akhir penyakit.
4.6 Manifestasi Klinik
Manifestasi Klinik DM:
o Poliuriao Polidipsiao Polifagiao Penurunan berat badano Lemaho Kesemutano Gatalo Mata kaburo Disfungsi ereksi pada priao Pruritus vulvae pada wanita.
4.7 Diagnosis dan Diagnosis Banding
DIAGNOSIS
ANAMNESIS
Identitas penderitaMeliputi nama, umur, jenis kelamin, agama, pendidikan, pekerjaan,alamat, status perkawinan, suku bangsa, nomor register, tanggal masukrumah sakit dan diagnosa medis. Keluhan UtamaAdanya rasa kesemutan pada kaki / tungkai bawah, rasa raba yang menurun, adanya luka yang tidak sembuh – sembuh dan berbau, adanya nyeri pada luka. Riwayat kesehatan sekarang
28

Berisi tentang kapan terjadinya luka, penyebab terjadinya luka serta upaya yang telah dilakukan oleh penderita untuk mengatasinya. Riwayat kesehatan dahuluAdanya riwayat penyakit DM atau penyakit – penyakit lain yang ada kaitannya dengan defisiensi insulin misalnya penyakit pankreas. Adanya riwayat penyakit jantung, obesitas, maupun arterosklerosis, tindakan medis yang pernah di dapat maupun obat-obatan yang biasa digunakan oleh penderita. Riwayat kesehatan keluargaDari genogram keluarga biasanya terdapat salah satu anggota keluarga yang juga menderita DM atau penyakit keturunan yang dapatmenyebabkan terjadinya defisiensi insulin misal hipertensi, jantung. Riwayat psikososialMeliputi informasi mengenai prilaku, perasaan dan emosi yang dialami penderita sehubungan dengan penyakitnya serta tanggapan keluargaterhadap penyakit penderita.
PEMERIKSAAN FISIK
Status kesehatan umumMeliputi keadaan penderita, kesadaran, suara bicara, tinggi badan, berat badan dan tanda – tanda vital. Kepala dan leherKaji bentuk kepala, keadaan rambut, adakah pembesaran pada leher, telinga kadang-kadang berdenging, adakah gangguan pendengaran, lidah sering terasa tebal, ludah menjadi lebih kental, gigi mudah goyah, gusi mudah bengkak dan berdarah, apakah penglihatan kabur / ganda, diplopia, lensa mata keruh. Sistem integumenTurgor kulit menurun, adanya luka atau warna kehitaman bekas luka, kelembaban dan shu kulit di daerah sekitar ulkus dan gangren, kemerahan pada kulit sekitar luka, tekstur rambut dan kuku. Sistem pernafasanAdakah sesak nafas, batuk, sputum, nyeri dada. Pada penderita DM mudah terjadi infeksi. Sistem kardiovaskulerPerfusi jaringan menurun, nadi perifer lemah atau berkurang, takikardi/bradikardi, hipertensi/hipotensi, aritmia, kardiomegalis. Sistem gastrointestinalTerdapat polifagi, polidipsi, mual, muntah, diare, konstipasi, dehidrase, perubahan berat badan, peningkatan lingkar abdomen, obesitas. Sistem urinaryPoliuri, retensio urine, inkontinensia urine, rasa panas atau sakit saat berkemih. Sistem muskuloskeletalPenyebaran lemak, penyebaran masa otot, perubahn tinggi badan, cepat lelah, lemah dan nyeri, adanya gangren di ekstrimitas.
29

Sistem neurologisTerjadi penurunan sensoris, parasthesia, anastesia, letargi, mengantuk, reflek lambat, kacau mental, disorientasi.
PEMERIKSAAN PENUNJANG
Tes HbA1C
Tes HbA1C digunakan untuk mendeteksi diabetes tipe 2 dan pradiabetes tetapi tidak dianjurkan untuk diagnosis diabetes tipe 1 atau diabetes gestasional. Tes HbA1C adalah tes darah yang mencerminkan rata-rata kadar glukosa darah seseorang selama 3 bulan terakhir dan tidak menunjukkan fluktuasi harian. Tes A1C lebih nyaman bagi pasien dibandingkan dengan tes glukosa tradisional karena tidak memerlukan puasa dan dapat dilakukan setiap saat sepanjang hari. Hasil uji HbA1C dilaporkan sebagai persentase. Semakin tinggi persentase, kadar glukosa darah seseorang lebih tinggi telah. Tingkat HbA1C normal adalah di bawah 5,7 persen.
Sebuah hasil HbA1C dari 5,7-6,4 persen menunjukkan pradiabetes. Orang yang didiagnosis dengan pradiabetes dapat diuji ulang dalam 1 tahun. Orang dengan HbA1C di bawah 5,7 persen maystill beresiko untuk diabetes, tergantung pada ada karakteristik lain yang menempatkan mereka pada resiko, juga dikenal sebagai faktor risiko. Orang dengan HbA1C di atas 6,0 persen harus dipertimbangkan pada risiko yang sangat tinggi mengembangkan diabetes. Sebuah level 6,5 persen atau di atas berarti seseorang memiliki diabetes.
Hasil abnormal. Tes HbA1C dapat diandalkan untuk mendiagnosis atau memantau diabetes pada orang dengan kondisi tertentu diketahui mengganggu hasil. Interferensi harus dicurigai saat hasil A1C tampak sangat berbeda dari hasil tes glukosa darah. Orang-orang dari Afrika, Mediterania, atau keturunan Asia Tenggara atau orang-orang dengan anggota keluarga dengan anemia sel sabit atau talasemia yang sangat beresiko gangguan.
Namun, tidak semua dari tes HbA1C tidak dapat diandalkan untuk orang dengan penyakit ini. Hasil tes HbA1C False positif juga dapat terjadi pada orang dengan masalah lain yang mempengaruhi darah atau hemoglobin mereka seperti penyakit ginjal kronis, penyakit hati, atau anemia.
Perubahan Pengujian Diagnostik
Di masa lalu, tes HbA1C digunakan untuk memantau kadar glukosa darah tetapi tidak untuk diagnosis. Tes HbA1C sekarang telah dibakukan, dan pada tahun 2009, komite ahli internasional direkomendasikan digunakan untuk diagnosis diabetes tipe 2 dan prediabetes.
Tes Glukosa Plasma Puasa
The FPG tes digunakan untuk mendeteksi diabetes dan pradiabetes. The FPG tes telah tes yang paling umum digunakan untuk mendiagnosis diabetes karena lebih mudah daripada TTGO dan
30

lebih murah. The FPG Uji ini mengukur glukosa darah pada orang yang telah berpuasa selama minimal 8 jam dan paling dapat diandalkan ketika diberikan di pagi hari.
Orang dengan kadar glukosa puasa 100 sampai 125 mg / dL memiliki gangguan glukosa puasa (IFG), atau pradiabetes. Tingkat dari 126 mg / dL atau di atas, dikonfirmasi dengan mengulang uji pada hari lain, berarti seseorang memiliki diabetes.
Tes Toleransi Glukosa Oral
The OGTT dapat digunakan untuk mendiagnosa diabetes, pradiabetes, dan diabetes gestasional. Penelitian telah menunjukkan bahwa OGTT lebih sensitif dibandingkan tes FPG, tetapi kurang nyaman untuk mengelola. Ketika digunakan untuk menguji untuk diabetes atau pradiabetes, OGTT mengukur glukosa darah setelah seseorang berpuasa selama minimal 8 jam dan 2 jam setelah orang minum cairan yang mengandung 75 gram glukosa dilarutkan dalam air.
Jika kadar gula darah 2 jam antara 140 dan 199 mg / dL, orang tersebut memiliki jenis pradiabetes disebut gangguan toleransi glukosa (IGT). Jika dikonfirmasi oleh tes kedua, tingkat glukosa 2 jam dari 200 mg / dL atau di atas berarti seseorang memiliki diabetes.
Tes Glukosa Darah Sewaktu
Tes darah, glukosa plasma acak (RPG) tes, kadang-kadang digunakan untuk mendiagnosa diabetes selama pemeriksaan kesehatan secara teratur. Jika RPG mengukur 200 mikrogram per desiliter atau di atas, dan orang tersebut juga menunjukkan gejala diabetes, maka dokter bisa mendiagnosa diabetes.
DIAGNOSIS BANDING
1. Cystic Fibrosis2. Diabetic Ketoasidosis3. Drug-induced glucose intolerance4. Gestasional Diabetics5. Glucose intolerance6. Pankreatitis
4.8 Penatalaksanaan
Tatalaksana Farmakologis
Insulin
Insulin adalah hormon yang dihasilkan dari sel β pankreas dalam merespon glukosa. Insulin merupakan polipeptida yang terdiri dari 51 asam amino tersusun dalam 2 rantai, rantai A terdiri dari 21 asam amino dan rantai B terdiri dari 30 asam amino. Insulin mempunyai peran yang
31

sangat penting dan luas dalam pengendalian metabolisme, efek kerja insulin adalah membantu transport glukosa dari darah ke dalam sel. Macam-macam sediaan insulin:
1. Insulin kerja singkat Sediaan ini terdiri dari insulin tunggal biasa, mulai kerjanya baru sesudah setengah jam (injeksi subkutan), contoh: Actrapid, Velosulin, Humulin Regular.
2. Insulin kerja panjang (long-acting) Sediaan insulin ini bekerja dengan cara mempersulit daya larutnya di cairan jaringan dan menghambat resorpsinya dari tempat injeksi ke dalam darah. Metoda yang digunakan adalah mencampurkan insulin dengan protein atau seng atau mengubah bentuk fisiknya, contoh: Monotard Human.
3. Insulin kerja sedang (medium-acting) Sediaan insulin ini jangka waktu efeknya dapat divariasikan dengan mencampurkan beberapa bentuk insulin dengan lama kerja berlainan, contoh: Mixtard 30 HM (Tjay dan Rahardja, 2002).
Secara keseluruhan sebanyak 20-25% pasien DM tipe 2 kemudian akan memerlukan insulin untuk mengendalikan kadar glukosa darahnya. Untuk pasien yang sudah tidak dapat dikendalikan kadar glukosa darahnya dengan kombinasi metformin dan sulfonilurea, langkah selanjutnya yang mungkin diberikan adalah insulin (Waspadji, 2010).
Obat Antidiabetik Oral
1. GOLONGAN SULFONILUREA
MEKANISME KERJA.
Golongan obat ini sering disebut sebagai insulin secretstogues, kerjanya merangsang sekresi insulin dari granul sel-sel β Langerhans pancreas. Rangsangannya melalui interaksinya dengan ATP-sensitive K channel pada membrane sel-sel β yang menimbulkan depolarisasi membrane dan keadaan ini akan membuka kanal Ca. dengan terbukanya kanal Ca maka ion Ca++ akan masuk sel-sel β, merangsang granula yang berisi insulin dan akan terjadi sekresi insulin dengan jumlah yang ekuivalen dengan peptida C. kecuali itu sulfonylurea dapat mengurangi klirens insulin di hepar. Pada penggunaan jangka panjang atau dosis yang besar dapat menyebabkan hipoglikemia.
FARMAKOKINETIK.
Berbagai sulfonylurea mempunyai sifat kinetic berbeda, tetapi absorpsi melalui saluran cerna cukup efektif. Makanan dan keadaan hiperglikemia dapat mengurangi absorpsi. Untuk mencapai kadar optimal di plasma, sulfonylurea dengan masa paruh pendek akan lebih efektif bila diminum 30 menit sebelum makan. Dalam plasma sekitar 90%-99% terikat protein plasma terutama albumin; ikatan ini paling kecil untuk klorpropamid dan paling besar untuk gliburid.
Masa paruh dan metabolisme sulfonylurea generasi I sangat bervariasi. Masa paruh asetoheksamin pendek tetapi metabolit aktifnya, 1-hidroksiheksamid masa paruhnya lebih
32

panjang, sekitar 4-5 jam, sama dengan tolbutamid dan tolazamid. Sebaiknya sediaaan ini diberikan dengan dosis terbagi. Sekitar 10% dari metabolitnya diekskresi melalui empedu dan keluar bersama tinja.
1. Klorpropamid dalam darah terikat albumin, masa paruhnya panjang, 24-48 jam, efeknya masih terlihat beberapa hari setelah obet dihentikan. Metabolismenya di hepar tidak lengkap, 20% diekskresi utuh di urin.
2. Mula kerja tolbutamid cepat, masa paruhnya sekitar 4-7 jam. Dalam darah sekitar 91-96% tolbutamid terikat protein plasma, dan di hepar di ubah menjadi karboksitolbutamid. Ekskresinya melalui ginjal.
3. Tolazamid, absorpsinya lebih lambat dari yang lain; efeknya pada glukosa darah belum nyata untuk beberapa jam setelah obat diberikan. Masa paruh sekitar 7 jam, di hepar di ubah menjadi p-karboksitolazamid, 4-hidroksimetitolazamid dan senyawa lain, yang diantaranya memiliki sifat hipoglikemik cukup kuat.
4. Sulfonilurea generasi II, umumnya potensi hipoglikemiknya hampir 100 kali lebih besar dari generasi I. Meski masa paruhnya pendek, hanya sekitar 3-5 jam, efek hipoglikemiknya berlangsung 12-24 jam, sering cukup diberikan 1 kali sehari. Alasan mengapa masa paruh yang pendek ini, memberikan efek hipoglikemik panjang, belum diketahui.
5. Glibizid, absorpsinya lengkap, masa paruhnya 3-4 jam. Dalam darah 98% terikat protein plasma, potensinya 100 kali lebih kuat dari tolbutamid, tetapi efek hipoglikemik maksimalnya mirip dengan sulfonilurea lain, metabolismenya di hepar, menjadi metabolit yang tidak aktif, sekitar 10% diekskresi melalui ginjal dalam keadaan utuh.
6. Gliburid (glibenklamid) potensinya 200 x lebih kuat dari tolbutamid, masa paruhnya sekitar 4 jam. Metabolismrnya di ahepar, pada pemberian dosis tunggal hanya 25% metabolitnya diekskresi melalui urun, sisanya melalui empedu. Pada penggunaan dapat terjadi kegagalan primer dan sekunder, dengan seluruh kegagalan kira-kira 21% selama 1,5 tahun.
Karena semua sulfonilurea di metabolisme di hepar dan diekskresi melalui ginjal, sediaan ini tidak boleh diberikan pada pasien gangguan fungsi hepar atau ginjal yang berat.
EFEK SAMPING.
Insidens efek samping generasi I sekitar 4%, insidensnya lebih rendah lagi untuk generasi II. Hipoglikemia, bahkan sampai koma tentu dapat timbul.reaksi ini lebih sering terjadi pada pasien usia lanjut dengan gangguan fungsi hepar atau ginjal, terutama yang menggunakan sediaan dengan masa kerja panjang.
Efek samping lain, reaksi alergi jarang sekali terjadi, mual, muntah, diare, gejala hematologi, susunan saraf pusat, mata dan sebagainya.
Gangguan saluran cerna ini dapat berkurang dengan mengurangi dosis, menelan obat bersama makanan atau membagi obat dalam beberapa dosis. Gejala sususnan saraf pusat berupa vertigo, bingung, atraksia dan sebagainya. Gejala hematologik al. Leukopenia dan agranulositosis. Efek
33

samping lain gejala hipotiroidisme, ikterus obstruktuf, yang bersifat sementara dan lebih sering timbul akibat klorpropamid (0,4%). Berkuarngnya toleransi terhadap alkohol juga telah dilaporkan pada pemakaian tolbutamid dan klorpropamid.
Hipoglikemia dapat terjadi pada pasien yang tidak mendapat dosis tepat, tidak makan cukup atau dengan gangguan fungsi hepar dan/atau ginjal. Kecenderungan hipoglikemia pada orang tua disebabkan oleh mekanisme kompensasi berkurang dan asupan makanan yang cenderung kurang. Selain itu, hipoglikemia tidak mudah dikenali pada orang tua karena timbul perlahan tanpa tanda akut (akibat tidak ada refleks simpatis) dan dapat menimbulkan disfungsi otak sampai koma. Penurunan kecepatan ekskresi klo, propamid dapat meningkatkan hipoglikemia.
INDIKASI.
Memilih sulfonilurea yang tepat untuk pasien tertentu sangat penting untuk suksesnya terapi. Yang menentukan bukanlah umur pasien waktu terapi dimulai, tetapi usia pasien waktu penyakit DM mulai timbul. Pada umumnya hasil yang baik diperoleh pada pasien yang diabetesnya mulai timbul pada usia diatas 40 tahun. Sebelum menentukan keharusan penggunaan sulfonilurea, selalu harus dipertimbangkan kemungkinan mengatasi hiperglikemia dengan hanya mengatur diet serta mengurangi berat badan pasien.
Kegagalan pasien dengan salah satu derivat sulfonilurea, mungkin juga disebabkan oleh perubahan farmakokinetik obat, misal penghancuran yang terlalu cepat. Obat hasil terapi yang baik tidak dapat dipertahankan dengan dosis 0.5 g klorpropamid, 0.75 g tolazamid, sebaiknya dosis jangan ditambah lagi.
Selama terapi, pemeriksaan fisik dan laboratorium harus tetap dilakukan secara teratur. Pada keadaan yang gawat seperti stres, komplikasi, infeksi dan pembedahan, insulin tetap merupakan terapi standar.
2. MEGLITINID
Repaglinid dan nateglinid
Merupakan golongan meglitinid, mekanisme kerjanya sama dengan sulfonilurea tetapi struktur kimianya sangat berbeda. Golongan ADO ini merangsang insulin dengan menutup kanal K yang ATP-independent di sel β pankreas.
Pada pemberian oral absorpsinya cepat dan kadar puncaknya dicapai dalam waktu 1 jam. Masa paruhnya 1 jam, karena harus diberikan beberapa kali sehari, sebelum makan. Metabolisme utamanya di hepar dan metabolitnya tidak aktif. Sekitar 10% dimetabolisme di ginjal. Pada pasien dengan gangguan fungsi hepar atau ginjal harus diberikan secara berhati-hati. Efek samping utamanya hipoglikemia dan gangguan saluran cerna. Reaksi alergi juga pernah dilaporkan.
34

3. BIGUANID
Sebenarnya dikenal 3 golongan ADO dari golongan biguanid : fenformin, buformin, dan metformin, tetapi yang pertama telah ditarik dari peredaran karena sering menyebabkan asidosis laktat. Sekarang yang banyak digunakan adalah metformin.
MEKANISME KERJA.
Biguanid tidak menyebabkan rangsangan sekresi insulin dan umumnya tidak menyebabkan hipoglikemia. Metformin menurunkan produksi glukosa dihepar dan menungkatkan sensitivitas jaringan otot dan adiposa terhadap insulin. Efek ini terjadi karena adanya aktivasi kinase di sel (AMP-activated protein kinase). Meski masih kontroversial, adanya penurunan produksi glukosa hepar, banyak data yang menunjukkan bahwa efeknya terjadi akibat penurunan glukoneogenesis. Preparat ini tidak mempunyai efek yang berarti pada sekresi glukagon, kortisol, hormon pertumbuhan, dan somatostatin.
Biguanid tidak merangsang ataupun menghambat perubahan glukosa menjadi lemak. Pada pasien diabetes yang gemuk, biguanid dapat menurunkan berat badan dengan mekanisme yang belum jelas pula; pada orang nondiabetik yang gemuk tidak timbul penurunan berat badan dan kadar glukosa darah.
Metformin oral akan mengalami absorpsi di intestin, dalam darah tidak terikat protein plasma, ekskresinya melalui urin dalam keadaan utuh. Masa paruhnya sekitar 2 jam.
Dosis awal 2 x 500 mg, umumnya dosis pemeliharaan (maintenance dose) 3 x 500 mg, dosis maksimal 2,5 g. Obat diminum pada waktu makan. Pasien DM yang tidak memberikan respon dengan sulfonilurea dapat diatasi dengan metformin, atau dapat pula diberikan sebagai terapi kombinasi dengan insulin atau sulfonylurea.
EFEK SAMPING.
Hampir 20% pasien dengan metformin mengalami : mual; muntah, diare serta kecap logam (metalic taste); tetapi dengan menurunkan dosis keluhan-keluhan tersebut segera hilang. Pada beberapa pasien yang mutlak bergantung insulin eksogen, kadang-kadang biguanid menimbulkan ketosis yang tidak disertai dengan hiperglikemia (starvation ketosis). Hal ini harus dibedakan dengan ketosis karena defisiensi insulin.
Pada pasien dengan gangguan fungsi ginjal atau sistem kardiovaskular, pemberian biguanid dapat menimbulkan peningkatan kadar asam laktat dalam darah, sehingga hal ini dapat mengganggu keseimbangan elektrolit dalam cairan tubuh.
INDIKASI.
Sediaan biguanid tidak dapat menggantikan fungsi insulin endogen, dan digunakan pada terapi diabetes dewasa.
35

Dari berbagai derivat biguanid, data fenformin yang paling banyak terkumpul tetapi sediaan ini kini dilarang dipasarkan di Indonesia karena bahaya asidosis laktat yang mungkin ditimbulkannya. Di Eropa fenformin digantikan dengan metformin yang kerjanya serupa fenformin tetapi diduga lebih sedikit menyebabkan asidosis laktat. Dosis metformin ialah 1-3 gram sehari dibagi dalam 2 atau 3 kali pemberian.
KONTRA INDIKASI.
Biguanid tidak boleh diberikan pada kehamilan, pasien penyakit hepar berat, penyakit ginjal dengan uremia dan penyakit jantung kongestif dan penyakit paru dengan hipoksia kronik. Pada pasien yang akan diberi zat kontras intravena atau yang akan di operasi, pemberian obat ini sebaiknya dihentikan dahulu. Setelah lebih dari 48 jam, biguanid baru boleh diberikan dengan catatan fungsi ginjal harus tetap normal. Hal ini untuk mencegah terbentuknya laktat yang berlebihan dan dapat berakhir fatal akibat asidosis laktat. Insidens asidosis akibat metformin kurang dari 0.1 kasus per 1000 patient-years, dan mortalitasnyalebih rendah lagi.
4. GOLONGAN TIAZOLIDINEDION
MEKANISME KERJA.
Tiazolidinedion merupakan agonist potent dan selektif PPARγ, mengaktifkan PPARγ membentuk kompleks PPARγ-RXR dan terbentuklah GLUT baru. Di jaringan adiposa PPARγ mengurangi keluarnya asam lemak menuju ke otot, dan karenanya dapat mengurangi resistensi insulin. Pendapat lain, aktivasi hormon adiposit dan adipokin, yang nampaknya adalah adiponektin. Senyawa ini dapat meningkatkan sensitivitas insulin melalui peningkatan AMP kinase yang merangsang transport glukosa ke sel dan meningkatkan oksidasi asam lemak. Jadi agar obat dapat bekerja harus tersedia insulin.
Selain itu glitazon juga menurunkan produksi glukosa hepar, menurunkan asam lemak bebas di plasma dan remodeling jaringan adipose.
Pioglitazon dan rosiglitazon dapat menurunkan HBA1c (1,0-1,5%) dan berkecenderungan meningkatkan HDL, sedang efeknya pada trigliserid dan LDL bervariasi.
Pada pemberian oral absorpsi tidak dipengaruhi makanan, berlangsung ± 2 jam.metabolismenya di hepar, oleh sitokrom P-450 rosiglitazon dimetabolisme oleh isozim 2C8, sedangkan pioglitazon oleh 2C8 & 3A4. meski demikian, penggunaan rosiglitazon 4 mg 2 x sehari bersama nifedipin atau kontrasepsi oral (etinil estradiol + noretindron) yang juga dimetabolisme isozim 3A4 tidak menujukkan efek klinik negatif yang berarti.
Ekskresinya melalui ginjal, keduanyadapat diberikan pada insufisiensi renal, tetapi dikontraindikasikan pada gangguan fungsi hepar (ALT>2,5 x nilai normal). Meski laporan hepatotoksik baru ada pada troglitazon, FDA menganjurkan agar pada awal dan setiap 2 bulan sekali selama 12 bulan pertama penggunaan kedua preparat diatas dianjurkan pemeriksaan tes
36

fungsi hepar. Penelitian population pharmacokinetic, menunjukkan bahwa usia tidak mempengaruhi kinetiknya.
Glitazon digunakan untuk DM tipe 2 yang tidak memberi respons dengan diet & latihan fisik, sebagai monoterapi atau ditambahkan pada mereka yang tidak memberi respons pada obat hipoglikemik lain (sulfonilurea, metformin) atau insulin.
Dosis awal rosiglitazon 4 mg, bila dalam 3-4 minggu kontrol glisemia belum adekuat, dosis ditingkatkan 8mg/hari, sedangkan pioglitazon dosis awal 15-30mg bila kontrol glisemia belum adekuat, dosis dapat ditingkatkan sampai 45 mg. Efek klinis maksimalnya tercapai setelah penggunaan 6-12 minggu.
EFEK SAMPING.
Efek samping antara lain, peningkatan berat badan, edema, menambah volume plasma dan memperburuk gagal jantung kongestif. Edema sering terjadi pada penggunaannya bersama insulin. Kecuali penyakit hepar, tidak dianjurkan pada gagal jantung kelas 3 dan 4 menurut klasifikasi New York Heart Association. Hipoglikemia pada penggunaan monoterapi jarang terjadi.
5. PENGHAMBAT ENZIM α-GLIKOSIDASE
MEKANISME KERJA.
Obat golongan ini dapat memperlambat absorpsi polisakarida (starch), dekstrin, dan disakarida di intestin. Dengan menghambat kerja enzim α-glikosidase di brush border intestin, dapat mencegah peningkatan glukosa plasma pada orang normal dan pasien DM.
Karena kerjanya tidak mempengaruhi sekresi insulin, maka tidak akan menyebabkan efek samping hipoglikemia. Akarbose dapat digunakan sebagai monoterapi pada DM usia lanjut atau DM yang glukosa postprandialnya sangat tinggi. Di klinik sering digunakan bersama antidiabetik oral lain dan/atau insulin.Obat ini diberikan pada waktu mulai makan; dan absorpsi buruk.
Akarbose merupakan oligosakarida yang berasal dari mikroba, dan miglitol suatu derivat deseksi nojirimisin, secara kompetitif juga menghambat glukoamilase dan sukrase, tetapi efeknya pada α-amilase pankreas lemah. Kedua preparat dapat menurunkan glukosa plasma postprandial pada DM tipe 1 & 2, dan pada DM tipe 2 dengan hiperglisemia yang hebat dapat menurunkan HbA1c secara bermakna. Pada pasien DM dengan hiperglisemia ringan sampai sedang, hanya dapat mengatasi hiperglisemia sekitar 30%-50% dibandingkan antidiabetik oral lainnya (dinilai dengan pemeriksaan HbA1c).
EFEK SAMPING.
Efek samping yang bersifat dose-dependent antara lain: malabsorpsi, flatulen, diare, dan abdominal bloating. Untuk mengurangi efek samping ini sebaiknya dosis dititrasi, mulai dosis
37

awal 25 mg pada saat mulai makan untuk selama 4-8 minggu sampai dosis maksimal 75mg setiap tepat sebelum makan. Dosis yang lebih kecil dapat diberikan dengan makanan kecil (snack).
Akarbose paling efektif bila diberikan bersama makanan yang berserat, mengandung polisakarida, dengan sedikit kandungan glukosa dan sukrosa. Bila akarbose diberikan bersama insulin, atau dengan golongan sulfonilurea, dan menimbulkan hipoglikemia, pemberian glukosa akan lebih baik daripada pemberian sukrose, polisakarida atau maltosa.
OBAT HIPERGLIKEMIK
1. GLUKAGON
MEKANISME KERJA.
Glukagon menyebabkan glikogenolisis di hepar dengan jalan merangsang enzim adenilsiklase dalam pembentukan siklik AMP, kemudian siklik AMP ini mengaktifkan fosforilase, suatu enzim penting untuk glikogenolisis. Efek glukagon ini hanya terbatas pada hepar saja dan tidak dapat dihambat dengan pemberian adrenoreseptor β.
Glukagon juga meningkatkan glukoneogenesis. Efek ini mungkin sekali disebabkan oleh menyusutnya simpanan glikogen dalam hepar, karena dengan berkurangnya glikogen dalam hepar proses deaminasi dan transaminasi menjadi lebih aktif. Dengan meningkatnya proses tersebut maka pembentukan kalori juga makin besar. Ternyata efek kalorigenik glukagon hanya dapat timbul bila ada tiroksin dan adrenokortikosteroid.
Sekresi glukagon pankreas meninggi dalam keadaan hipoglikemia dan menurun dalam keadaan hiperglikemia. Sebagian besar glukagon endigen mengalami metabolisme di hati.
INDIKASI.
Glukagon terutama digunakan pada pengobatan hipoglikemia yang ditimbulkan oleh insulin. Hormon tersebut dapat diberikan secara IV, IM atau SK dengan dosis 1 mg. Bila dalam 20 menit setelah pemberian glukagon SK pasien koma hipoglikemik tetapi tidak sadar, maka glukosa IV harus segera diberikan karena mungkin sekali glikogen dalam hepar telah habis atau telah terjadi kerusakan otak yang menetap. Glukagon HCl tersedia dalam ampul berisi bubuk 1 dan 10mg.
2. DIAZOKSID
Obat ini memperlihatkan efek hiperglikemia bila diberikan oral dan efek antihipertensi bila diberikan IV. Sediaan ini meningkatkan kadar glukosa sesuai besarnya dosis dengan menghambat langsung sekresi insulin; mungkin juga dengan menghambat penggunaan glukosa dan perifer dan merangsang langsung sekresi insulin; mungkin juga dengan menghambat penggunaan glukosa di perifer dan merangsang pembentukan glukosa dalam hepar. Diazoksid digunakan pada hiperinsulinisme misalnya pada insulinoma atau hipoglikemia yang sensitif
38

terhadap leusin. Diazoksid 90% terikat plasma protein dalam darah. Masa paruh bentuk oral 24-36 jam, tetapi mungkin memanjang pada takar lajak atau pada apsien dengan kerusakan dengan kerusakan fungsi ginjal. Karena masa paruh yang panjang, diperlukan pengamatan jangka panjang. Takar lajak dapat menyebabkan hiperglikemia berat, kadang-kadang disertai ketoasidosis atau koma hiperosmolar tanpa ketosis.
Meskipun diazoksid termasuk golongan tiazid, obat ini meretensi air dan natrium. Diuretik tiazid meninggikan efek hiperglikemi dan hiperurisemi obat ini. Diazoksid oral menimbulkan potensiasi efek obat antihipertensi lain, meskipun bila obat ini digunakan sendiri efeknya tidak kuat. Efek hiperglikemi diazoksid dilawan oleh obat penghambat adrenoreseptor β. Diazoksid dapat menimbulkan iritasi saluran cerna, trombositopeni dan netropeni. Diazoksid bersifat teratogenik pada hewan (kelainan kardiovaskular dan tulang), juga menyebabkan degenerasi sel β pankreas fetus sehingga obat ini tidak boleh diberikan pada wanita hamil. Dosis pada orang dewasa adalah 3-8 mg/kgBB/hari, sedangkan pada anak kecil 8-15 mg/kgBB/hari. Obat ini diberikan dalam dosis terbagi 2-3 x sehari.
TERAPI INSULIN
KLASIFIKASI INSULIN
Jenis sediaan Bufer Mula kerja Puncak (jam)
Masa kerja (jam)
Kombinasi dengan (jam)
Kerja cepat Regular solube (kristal) Lispro
-Fosfat
0,1-0,70,25
1,5-40,5-1,5
5-82-5
Semua jenis
LenteKerja sedang NPH (isophan) Lente
FosfatAsetat
1-21-2
6-126-12
18-2418-24
RegularSenilente
Kerja panjang Protamin zinc Ultralente Glargin
Fosfat asetat-
4-64-62-5
14-2016-185-24
24-3620-3618-24
Regular
INDIKASI dan TUJUAN.
Insulin subkutan terutama diberikan pada DM tipe 1, DM tipe 2 yang tidak dapat diatasi hanya dengan diet dan atau antidiabetik oral, pasien DM pasca pankreaktomi atau DM dengan kehamilan, DM dengan ketoasidosis, koma nonketosis, atau komplikasi lain, sebelum tindakan operasi (DM tipe 1 dan 2). Tujuan pemberian insulin pada semua keadaan tersebut bukan saja untuk menormalkan glukosa darah tetapi juga memperbaiki semua aspek metabolisme, dan yang terakhir inilah umumnya yang suka dicapai.
39

Keadaan mendekati normoglisemia dicapai pada DM dengan multipel dosis harian insulin atau dengan infusion pump therapy, yang tujuannya mencapai glukosa darah puasa antara 90-120 mg/dL (5-6,7 mM), glukosa 2 jam postprandial kurang dari 150 mg/dL (8,3 mM). Pada pasien yang kurang disiplin atau kurang patuh terhadap terapi, mungkin perlu dicapai nilai glukosa darah puasa yang lebih tinggi (140 mg/dL atau 7,8 mM) dan postprandial 200 sampai 250 mg/dL atau11,1-13,9 mM.
EFEK SAMPING.
Hipoglikemia, merupakan efek samping paling sering terjadi dan terjadi akibat dosis insulin yang terlalu besar, tidak tepatnya waktu makan dengan waktu tercapainya kadar puncak insulin, atau karena adanya faktor yang dapat meningkatkan sensitivitas terhadap insulin, misal insufisiensi adrenal atau pituitary, ataupun akibat kerja fisik yang berlebihan.
Reaksi alergi dan resistensi, kadang-kadang reaksi ini terjadi akibat adanya bekuan atau terjadinya denaturasi preparat insulin, atau kontaminan, atau akibat pasien sensitif terhadap senyawa yang ditambahkan pada proses formulasi preparat insulin (misal: Zn2+, protamin, fenol,dll). Reaksi alergi lokal sering terjadi akibat IgE atau resistensi akibat timbulnya antibodi IgG.
Lipoartrofi dan lipohipertrofi. Lipoartrofi jaringan lemak subkutan ditempat suntikan dapat timbul akibat variant respon imun terhadap insulin; sedangkan lipohipertrofi dimana terjadi penumpukan lemak subkutan terjadi akibat efek lipogenik insulin yang kadarnya tinggi pada daerah tempat suntikan. Hal ini diduga akibat adanya kontaminan dalam preparat insulin, dan reaksi lebih jarang terjadi pada penggunaan insulin, dan reaksi lebih jarang terjadi pada penggunaan insulin yang lebih murni. Pada kenyataannya lipohipertrofi lebih sering terjadi dengan human insulin apabila pasien yang menyuntikan sendiri pada tempat yang sama. Hal ini dapat disebabkan karena terjadinya absorpsi insulin yang kurang baik atau tidak teratur.
Tatalaksana Non-Farmakologis
Pengaturan diet
Diet yang baik merupakan kunci keberhasilan penatalaksanaan diabetes. Diet yang dianjurkan adalah makanan dengan komposisi yang seimbang dalam hal karbohidrat, protein dan lemak. Tujuan pengobatan diet pada diabetes adalah: a. Mencapai dan kemudian mempertahankan kadar glukosa darah mendekati kadar normal. b. Mencapai dan mempertahankan lipid mendekati kadar yang optimal. c. Mencegah komplikasi akut dan kronik. d. Meningkatkan kualitas hidup. Terapi nutrisi direkomendasikan untuk semua pasien diabetes mellitus, yang terpenting dari semua terapi nutrisi adalah pencapian hasil metabolis yang optimal dan pencegahan serta perawatan komplikasi.
40

Untuk pasien DM tipe 1, perhatian utamanya pada regulasi administrasi insulin dengan diet seimbang untuk mencapai dan memelihara berat badan yang sehat. Penurunan berat badan telah dibuktikan dapat mengurangi resistensi insulin dan memperbaiki respon sel-sel β terhadap stimulus glukosa.
Olah raga
Berolah secara teratur dapat menurunkan dan menjaga kadar gula darah tetap normal. Prinsipya, tidak perlu olah raga berat, olah raga ringan asal dilakukan secara teratur akan sangat bagus pengaruhnya bagi kesehatan. Beberapa contoh olah raga yang disarankan, antara lain jalan atau lari pagi, bersepeda, berenang, dan lain sebagainya. Olah raga akan memperbanyak jumlah dan juga meningkatkan penggunaan glukosa (Ditjen Bina Farmasi dan Alkes, 2005).
(http://repository.usu.ac.id/bitstream/123456789/35195/4/Chapter%20II.pdf)
4.9 Pencegahan
Usaha pencegahan pada penyakit DM terdiri dari: pencegahan primordial yaitu pencegahan kepada orang-orang yang masih sehat agar tidak memilki faktor resiko untuk terjadinya DM, pencegahan primer yaitu pencegahan kepada mereka yang belum terkena DM namun memiliki faktor resiko yang tinggi dan berpotensi untuk terjadinya DM agar tidak timbul penyakit DM, pencegahan sekunder yaitu mencegah agar tidak terjadi komplikasi walaupun sudah terjadi penyakit, dan pencegahan tersier yaitu usaha mencegah agar tidak terjadi kecacatan lebih lanjut walaupun sudah terjadi komplikasi.
1. Pencegahan Primordial
Pencegahan primordial dilakukan dalam mencegah munculnya faktor predisposisi/resiko terhadap penyakit DM. Sasaran dari pencegahan primordial adalah orang-orang yang masih sehat dan belum memiliki resiko yang tinggi agar tidak memiliki faktor resiko yang tinggi untuk penyakit DM. Edukasi sangat penting peranannya dalam upaya pencegahan primordial. Tindakan yang perlu dilakukan seperti penyuluhan mengenai pengaturan gaya hidup, pentingnya kegiatan jasmani teratur, pola makan sehat, menjaga badan agar tidak terlalu gemuk dan menghindari obat yang bersifat diabetagenik.
2. Pencegahan Primer
Sasaran dari pencegahan primer adalah orang-orang yang termasuk kelompok resiko tinggi, yakni mereka yang belum terkena DM, tetapi berpotensi untuk mendapatkan penyakit DM. pada pencegahan primer ini harus mengenal faktor-faktor yang berpengaruh terhadap terjadinya DM dan upaya untuk mengeliminasi faktor-faktor tersebut
Pada pengelolaan DM, penyuluhan menjadi sangat penting fungsinya untuk mencapai tujuan tersebut. Materi penyuluhan dapat berupa : apa itu DM, faktor-faktor yang berpengaruh terhadap
41

timbulnya DM, usaha untuk mengurangi faktor-faktor tersebut, penatalaksanaan DM, obat-obat untuk mengontrol gula darah, perencanaan makan, mengurangi kegemukan, dan meningkatkan kegiatan jasmani.
a. Penyuluhan
Edukasi DM adalah pendidikan dan latihan mengenai pengetahuan mengenai DM. Disamping kepada pasien DM, edukasi juga diberikan kepada anggota keluarganya, kelompok masyarakat beresiko tinggi dan pihak-pihak perencana kebijakan kesehatan. Berbagai materi yang perlu diberikan kepada pasien DM adalah definisi penyakit DM, faktor-faktor yang berpengaruh pada timbulnya DM dan upaya-upaya menekan DM, pengelolaan DM secara umum, pencegahan dan pengenalan komplikasi DM, serta pemeliharaan kaki.
b. Latihan Jasmani
Latihan jasmani yang teratur (3-4 kali seminggu selama kurang lebih 30 menit) memegang peran penting dalam pencegahan primer terutama pada DM Tipe 2. Orang yang tidak berolah raga memerlukan insulin 2 kali lebih banyak untuk menurunkan kadar glukosa dalam darahnya dibandingkan orang yang berolah raga. Manfaat latihan jasmani yang teratur pada penderita DM antara lain:
Memperbaiki metabolisme yaitu menormalkan kadar glukosa darah dan lipid darah Meningkatkan kerja insulin dan meningkatkan jumlah pengangkut glukosa Membantu menurunkan berat badan Meningkatkan kesegaran jasmani dan rasa percaya diri Mengurangi resiko penyakit kardiovaskular
Laihan jasmani yang dimaksud dapat berupa jalan, bersepeda santai, jogging, dan berenang. Latihan jasmani sebaiknya disesuaikan dengan umur dan status kesegaran jasmani.
c. Perencanaan Pola Makan
Perencanaan pola makan yang baik dan sehat merupakan kunci sukses manajemen DM. Seluruh penderita harus melakukan diet dengan pembatasan kalori, terlebih untuk penderita dengan kondisi kegemukan. Menu dan jumlah kalori yang tepat umumnya dihitung berdasarkan kondisi individu pasien.
Perencanaan makan merupakan salah satu pilar pengelolaan DM, meski sampai saat ini tidak ada satupun perencanaan makan yang sesuai untuk semua pasien, namun ada standar yang dianjurkan yaitu makanan dengan komposisi yang seimbang dalam karbohidrat, protein, dan lemak sesuai dengan kecukupan gizi baik sebagai berikut:
Karbohidrat = 60-70 %, Protein = 10-15 %, dan Lemak = 20-25 %.
42

Jumlah asupan kolesterol perhari disarankan < 300 mg/hari dan diusahakan lemak berasal dari sumber asam lemak tidak jenuh dan membatasi PUFA (Poly Unsaturated Fatty Acid) dan asam lemak jenuh. Jumlah kalori disesuaikan dengan pertumbuhan, status gizi, umur, ada tidaknya stress akut dan kegiatan jasmani.
3. Pencegahan Sekunder
Pencegahan sekunder adalah upaya untuk mencegah atau menghambat timbulnya komplikasi dengan tindakan-tindakan seperti tes penyaringan yang ditujukan untuk pendeteksian dini DM serta penanganan segera dan efektif. Tujuan utama kegiatan-kegiatan pencegahan sekunder adalah untuk mengidentifikasi orang-orang tanpa gejala yang telah sakit atau penderita yang beresiko tinggi untuk mengembangkan atau memperparah penyakit.
Memberikan pengobatan penyakit sejak awal sedapat mungkin dilakukan untuk mencegah kemungkinan terjadinya komplikasi menahun. Edukasi dan pengelolaan DM memegang peran penting untuk meningkatkan kepatuhan pasien berobat.
a. Diagnosis Dini Diabetes Mellitus
Dalam menetapkan diagnosis DM bagi pasien biasanya dilakukan dengan pemeriksaan kadar glukosa darahnya. Pemeriksaan kadar glukosa dalam darah pasien yang umum dilakukan adalah :
Pemeriksaan kadar glukosa darah setelah puasa.
Kadar glukosa darah normal setelah puasa berkisar antara 70-110 mg/dl. Seseorang didiagnosa DM bila kadar glukosa darah pada pemeriksaan darah arteri lebih dari 126 mg/dl dan lebih dari 140 mg/dl jika darah yang diperiksa diambil dari pembuluh vena.
Pemeriksaan kadar glukosa darah sewaktu.
Jika kadar glukosa darah berkisar antara 110-199 mg/dl, maka harus dilakukan test lanjut. Pasien didiagnosis DM bila kadar glukosa darah pada pemeriksaan darah arteri ataupun vena lebih dari 200 mg/dl.16
Test Toleransi Glukosa Oral (TTGO).
Test ini merupakan test yang lebih lanjut dalam pendiagnosaan DM. Pemeriksaan dilakukan berturut-turut dengan nilai normalnya : 0,5 jam < 115 mg/dl, 1 jam < 200 mg/dl, dan 2 jam < 140 mg/dl.
Selain pemeriksaan kadar gula darah, dapat juga dilakukan pemeriksaan HbA1C atau glycosylated haemoglobin. Glycosylated haemoglobin adalah protein yang terbentuk dari perpaduan antara gula dan haemoglobin dalam sel darah merah.18 Nilai yang dianjurkan oleh PERKENI untuk HbA1C normal (terkontrol) 4 % - 5,9 %.17 Semakin tinggi kadar HbA1C maka
43

semakin tinggi pula resiko timbulnya komplikasi. Oleh karena itu pada penderita DM kadar HbA1C ditargetkan kurang dari 7 %.
Ketika kadar glukosa dalam darah tidak terkontrol (kadar gula darah tinggi) maka gula darah akan berikatan dengan hemoglobin (terglikasi). Oleh karena itu, rata-rata kadar gula darah dapat ditentukan dengan cara mengukur kadar HbA1C. bila kadar gula darah tinggi dalam beberapa minggu maka kadar HbA1C akan tinggi juga. Ikatan HbA1C yang terbentuk bersifat stabil dan dapat bertahan hingga 2-3 bulan (sesuai dengan umur eritrosit). Kadar HbA1C akan menggambarkan rata-rata kadar gula darah dalam jangka waktu 2-3 bulan sebelum pemeriksaan.19 Jadi walaupun pada saat pemeriksaan kadar gula darah pada saat puasa dan 2 jam sesudah makan baik, namun kadar HbA1C tinggi, berarti kadar glukosa darah tetap tidak terkontrol dengan baik.
b. Pengobatan Segera
Intervensi fakmakologik ditambahkan jika sasaran glukosa darah belum tercapai dengan pengaturan makanan dan latihan jasmani. Dalam pengobatan ada 2 macam obat yang diberikan yaitu pemberian secara oral atau disebut juga Obat Hipoglikemik Oral (OHO) dan pemberian secara injeksi yaitu insulin. OHO dibagi menjadi 3 golongan yaitu : pemicu sekresi insulin (Sulfonilurea dan Glinid), penambah sensitivitas terhadap insulin (Metformin dan Tiazolidindion), penambah absobsi glukosa (penghambat glukosidase alfa).
Selain 2 macam pengobatan tersebut, dapat juga dilakukan dengan terapi kombinasi yaitu dengan memberikan kombinasi dua atau tiga kelompok OHO jika dengan OHO tunggal sasaran kadar glukosa darah belum tercapai. Dapat juga menggunakan kombinasi kombinasi OHO dengan insulin apabila ada kegagalan pemakaian OHO baik tunggal maupun kombinasi.
4. Pencegahan Tersier
Pencegahan tersier adalah semua upaya untuk mencegah kecacatan akibat komplikasi. Kegiatan yang dilakukan antara lain mencegah perubahan dari komplikasi menjadi kecatatan tubuh dan melakukan rehabilitasi sedini mungkin bagi penderita yang mengalami kecacatan. Sebagai contoh, acetosal dosis rendah (80-325 mg) dapat dianjurkan untuk diberikan secara rutin bagi pasien DM yang sudah mempunyai penyakit makroangiopati.
Dalam upaya ini diperlukan kerjasama yang baik antara pasien pasien dengan dokter mapupun antara dokter ahli diabetes dengan dokter-dokter yang terkait dengan komplikasinya. Penyuluhan juga sangat dibutuhkan untuk meningkatkan motivasi pasien untuk mengendalikan penyakit DM. Dalam penyuluhan ini yang perlu disuluhkan mengenai:
Maksud, tujuan, dan cara pengobatan komplikasi kronik diabetes Upaya rehabilitasi yang dapat dilakukan Kesabaran dan ketakwaan untuk dapat menerima dan memanfaatkan keadaan hidup dengan
komplikasi kronik.
44

Pelayanan kesehatan yang holistik dan terintegrasi antar disiplin terkait juga sangat diperlukan, terutama di rumah sakit rujukan, baik dengan para ahli sesama disiplin ilmu seperti konsultan penyakit jantung dan ginjal, maupun para ahli disiplin lain seperti dari bagian mata, bedah ortopedi, bedah vaskuler, radiologi, rehabilitasi, medis, gizi, pediatri dan sebagainya.
4.10 Komplikasi
A. Komplikasi Akut Diabetes Mellitus
Komplikasi yang akut akibat DM terjadi secara mendadak. Keluhan dan gejalanya terjadi dengan cepat dan biasanya berat. Komplikasi akut umumnya timbul akibat glukosa darah yang terlalu rendah (hipoglikemia) atau terlalu tinggi (hiperglikemia).
a. Hipoglikemia
Kadar glukosa darah yang terlalu rendah sampai di bawah 60 mg/dl disebut hipoglikemia. Hipoglikemia dapat terjadi pada penderita DM yang diobati dengan suntikan insulin ataupun minum tablet anti-diabetes, tetapi tidak makan dan olah raganya melebihi biasanya.37 Bisa juga terjadi pada alkoholik, adanya tumor yang mensekresi glukagon, malnutrisi, dan yang jarang terjadi pada sepsis. Hipoglikemia dapat juga terjadi tanpa gejala awal pada sebagian pasien DM yang juga menderita hipertensi, khususnya di malam hari atau saat menggunakan obat bloker beta (obat hipertensi).
Keluhan dan gejala hipoglikemia dapat bervariasi, tergantung pada sejauh mana glukosa turun. Keluhan hipoglikemia pada dasarnya dapat dibagi dalam dua kategori besar, yaitu :
Keluhan akibat otak tidak mendapat cukup kalori sehingga menggangu fungsi intelektual, antara lain sakit kepala, kurang konsentrasi, mata kabur, capek, bingung, kejang, dan koma.
Keluhan akibat efek samping hormon lain (adrenalin) yang berusaha menaikkan kadar glukosa darah, yaitu pucat, berkeringat, nadi berdenyut cepat, berdebar, cemas, serta rasa lapar.
Pada awalnya ketika glukosa darah berada pada tingkat 40-50 mg/dl, pasien DM mengalami gemetaran, keringat dingin, mata kabur, lemah, lapar, pusing, sakit kepala, tegang, mual, jantung berdebar, dan kulit dingin. Pada saat glukosa darah di bawah 40 mg/dl, pasien akan merasa mengantuk, sukar bicara seperti orang mabuk, dan bingung. Dan pada saat glukosa di bawah 20 mg/dl keluhan atau gejala yang terjadi adalah kejang, tidak sadarkan diri (koma hipoglikemia), dan bisa menyebabkan kematian.
a. Diabetic Ketoacidosis (DKA)
Ketoasidosis Diabetik (KAD) adalah gawat darurat akibat hiperglikemia dimana terbentuk banyak asam dalam darah. Hal ini terjadi akibat sel otot tidak mampu lagi membentuk energi sehingga dalam keadaan darurat ini tubuh akan memecah lemak dan terbentuklah asam yang bersifat racun dalam peredaran darah yang disebut keton. Keadaan ini terjadi akibat suntikan
45

insulin berhenti atau kurang, atau mungkin karena lupa menyuntik atau tidak menaikkan dosis padahal ada makanan ekstra yang menyebabkan glukosa darah naik.20,37 Biasanya paling sering ditemukan pada penderita DM Tipe 1, namun pada penderita DM Tipe 2 pada keadaan tertentu seperti stress, infeksi, kelainan vaskuler ataupun stress emosional juga beresiko mendapatkan KAD.
Keluhan dan gejala KAD timbul akibat adanya keton yang meningkat dalam darah. Keluhan dan gejala tersebut berupa nafas yang cepat dan dalam, nafas bau keton atau aseton, nafsu makan turun, mual, muntah, demam, nyeri perut, berat badan turun, capek, lemah, bingung, mengantuk, dan kesadaran menurun sampai koma.35 Hasil pengamatan di bagian Ilmu Penyakit Dalam FKUI/RSCM tahun 1990, terdapat 152 pasien DM yang dirawat dengan CFR sebesar 24,9 % dari 15 kasus KAD. Hiperglikemik menuju glukosuria, berkurangnya volume cairan, dan tachycardia. Hipotensi dapat terjadi karena kekurangan volume cairan dengan kombinasi dengan peripheral vasodilatasi.
Pada keadaan lapar, asil-KoA dan glukagon akan menghambat Asetil-KoA Karboksilase yang berfungsi sebagai enzim dalam mengkatalis pembentukan Malonil-KoA dari Asetil-KoA. Dimana Malonil-KoA berfungsi sebagai penghambat suatu enzim di membran mitokondria yaitu Karnitin Palmitoil-Transferase I yang memiliki fungsi sebagai enzim yang membantu masuknya Asil-KoA masuk ke mitokondria untuk di ubah dalam proses ketogenesis menjadi badan keton dan CO2. Tapi pada orang DM, maka akan terus dihasilkan badan keton dan CO2 berlebih sehingga pH tubuh meningkat dan memicu jantung untuk terus bekerja bersama paru-paru dan ginjal untuk menyeimbangkan pH tubuh mengakibatkan tachycardia.
b. Hiperosmolar Non-Ketotik
Hiperosmolar Non-Ketotik adalah suatu keadaan dimana kadar glukosa darah sangat tinggi sehingga darah menjadi sangat “kental”, kadar glukosa darah DM bisa sampai di atas 600 mg/dl. Glukosa ini akan menarik air keluar sel dan selanjutnya keluar dari tubuh melalui kencing. Maka, timbullah kekurangan cairan tubuh atau dehidrasi.
Gejala Hiperosmolar Non-Ketotik mirip dengan ketoasidosis. Perbedaannya, pada Hiperosmolar Non-Ketotik tidak dijumpai nafas yang cepat dan dalam serta berbau keton. Gejala yang ditimbulkan adalah rasa sangat haus, banyak kencing, lemah, kaki dan tungkai kram, bingung, nadi berdenyut cepat, kejang dan koma.
B. Komplikasi Kronik Diabetes Mellitus
Pembagian komplikasi kronik DM :
Teori pertama bahwa peningkatan glukosa di intraselular menunju perubahan kenaikan produk akhir glikosilasi (AGEs) melalui protein intra- dan ekstraselular glikosilasi non enzimatik. Dimana glikosilasi nonenzimatik menghasilkan interaksi glukosa dengan gugus amino protein. Dimana AGEs telah menunjukkan cross-link protein, peningkatan atherosklerosis, disfungsi
46

glomerulus, berkurangnya sintesis nitrit oxide, menginduksi disfungsi endotel, dan perubahan struktur ECM.
Teori kedua berdasarkan pengamatan bahwa hyperglikemi meningkatkan metabolisme glukosa melalui jalur sorbitol. Glukosa intraselular dimetabolisme oleh phosphorilasi dan subsequent glikolisis, tapi ketika meningkat, beberapa glukosa diubah menjadi sorbitol oleh enzim aldose reduktase. Peningkatan konsentrasi sorbitol merubah pontensial redox, meningkatkan osmolalitas selular, generate reactive oxygen species, dan menuju ke slular disfungsi.
Teori ketiga bahwa hiperglikemik meningkatkan pembentukan diacylglicerol menuju pengaktifan protein kinase C (PKC). Diantara rekasi lainnya, PKC merubah transkripsi gen untuk fibronektin, kolagen tipe IV, protein kontraktile, dan protein ECM di sel endotelial dan neuron.
Teori keempat bahwa hiperglikemik meningkatkkan perubahan pada jalur hexosamine, yang menghasilkan fruktosa 6-fosfat, suatu substrat untuk O-linked glycosylation dan proteoglycan production. Jalur hexosamine mungkin merubah fungsi oleh protein glikosilasi seperti sintesis endotelial nitrik okside atau oleh perubahan dalam ekspresi gen transforming growth factor β (TGF-β) atau plasminogen activator inhibitor-1 (PAI-1).
a. Microvascular
1)Komplikasi ophthalmologi DM
DM dapat mengakibatkan kebutaan diantara umur 20-74 tahun. Kebutaan merupakan hasil progesive utama dari diabetes retinopathy dan macular edema. Tahap diabetes retinopathy sendiri ada 2, nonproliferative diabetic retinopathy dan proliferative diabetic retinopathy.
Nonproliferative diabetic retinopathy biasanya muncul pada akhir dekade awal atau awal dari dekade kedua dari penyakit DM itu sendiri dan ditandai dengan retinal vescular microaneurysms, blot hemorrhages, dan cotton wool spots. Nonproliferative diabetic retinopathy sedang dikarakteristikkan dengan perubahan venous vessel caliber, intraretinal microvascular abnormalities, dan beberapa microaneurysms dan hemorrhages. Patofisiologinya termasuk kehilangan retinal pericytes, peningkatan permeabilitas vaskular retina, perubahan aliran darah retina, dan keabnormalan microvascular retinal, semuanya menuju pada retinal iskemia. Keberadaan neovaskularisasi dalam respon pada retinal hypoxia adalah sebagai tanda proliferative diabetic retinopathy.
2)Komplikasi ginjal DM
Nephropathy dikarakteristikkan oleh glomerular hyperperfusi dan renal hypertrophy terjadi pada tahun pertama setelah serangan DM dan menyebabkan peningkatan GFR. Selama lima tahun pertama DM, penebalan basal membran glomerulus mengakibatkan glomerulus hypertrophy dan
47

GFR kembali ke normal. Setelah 5-10 tahun kemudian, microalbumin mulai diekskresikan oleh ginjal sebagai tanda ketidakmampuan ginjal untuk menyeimbangkan kompensasinya kembali.
Patogenesis nephropathy berhubungan dengan kronik hiperglikemi sebagai efek perkembangan dari soluble faktor (GF, angiotensin II, endothelin, AGEs), perubahan hemodinamic pada sirkulasi ginjal, dan perubahan struktur dari dlomerulus.
3)Neuropathy dan DM
Mungkin ditunjukkan dengan polyneuropathy, mononeuropathy, dan/atau autonomic neuropathy. Berhubungan dengan menghilangnya serabut saraf bermielin atau tidak bermielin karena ischemic.
a) Polyneuropathy
Akibat dari hilangnya sensori distal bisa mengakibatkan hyperestesi, parestesi, dan disestesi. Gejalanya berupa sensai mati rasa, kesemutan, panas, atau terbakar yang dimulai di daerah kaki dan menyebar secara proksimal.
b) Mononeuropathy
Hadir dengan rasa sakit dan melemahnya motorik pada distribusi suatu saraf tunggal. Diperkirakan akibat suatu kelainan vaskularisasi, tapi masih belum pasti patogenesisnya. Biasa mempengaruhi kranial nerve terutama kranial nerve III, IV, VI, atau VII.
c) Autonomic neuropathy
Tanda dari autonomic neuropathy adalah perkembangan cholinergic, noradrenergic, dan peptidergic. Juga dapat merusak perkembangan banyak sistem di tubuh, seperti cardiovascular, gastrointestinal, genitourinary, sudomotor, dan sistem metabolik. Pada cardiovascular mengakibatkan tachycardia dan orthostatic hypotension. Pada gastrointestinal mengakibatkan gastroparesis dan kelainan pengosongan bladder serta usus. Sedangkan pada genitourinary mengakibatkan kegagalan mempertahankan BAK dan disfungsi seksual.
b. Makrovaskular
Insidensi penyakit cardiovascular meningkat pada seseorang dengan DM. pasien DM tipe 2 tanpa MI memiliki resiko arteri koroner yang sama dengan seseorang nondiabetes yang memiliki MI.
Meskipun telah dilakukan control terhadap semua faktor resiko cardiovaskular, DM tipe 2 meningkatkan angka kematian cardiovascular hingga 2 kali pada pria dan 4 kali pada wanita. Faktor resiko penyakit makro vascular pada seseorang yang mengidap diabetes, diantaranya dislipidemia, hipertensi, obesitas.
1)Penyakit Jantung
48

DM merusak dinding pembuluh darah yang menyebabkan penumpukan lemak di dinding yang rusak dan menyempitkan pembuluh darah. Jika pembuluh darah koroner menyempit, otot jantung akan kekurangan oksigen dan makanan akibat suplai darah yang kurang. Selain menyebabkan suplai darah ke otot jantung, penyempitan pembuluh darah juga mengakibatkan tekanan darah meningkat, sehingga dapat mengakibatkan kematian mendadak.
2)Hipertensi
Penderita DM cenderung terkena hipertensi dua kali lipat dibanding orang yang tidak menderita DM. Hipertensi bisa merusak pembuluh darah. Hipertensi dapat memicu terjadinya serangan jantung, retinopati, kerusakan ginjal, atau stroke. Antara 35-75% komplikasi DM disebabkan oleh hipertensi. Faktor-faktor yang dapat mengakibatkan hipertensi pada penderita DM adalah nefropati, obesitas, dan pengapuran atau pengapuran atau penebalan dinding pembuluh darah
4.11 Prognosis
Rencana perawatan Anda mungkin memerlukan penyesuaian dari waktu ke waktu. Resistensi insulin meningkat dengan usia. Dan sel-sel yang memproduksi insulin di pankreas dapat aus karena pankreas mencoba untuk bersaing dengan kebutuhan tambahan tubuh insulin. Setelah beberapa tahun pertama, sebagian besar orang dengan diabetes tipe 2 membutuhkan lebih dari satu obat untuk menjaga gula darah mereka terkontrol.
Prognosis pada orang dengan diabetes tipe 2 bervariasi. Hal ini tergantung pada seberapa baik seseorang memodifikasi risiko nya komplikasi. Serangan jantung, stroke dan penyakit ginjal dapat menyebabkan kematian dini. Cacat karena kebutaan, amputasi, penyakit jantung, stroke dan kerusakan saraf dapat terjadi. Beberapa orang dengan diabetes tipe 2 menjadi tergantung pada perawatan dialisis karena gagal ginjal.
LI 4. Memahami dan Menjelaskan Perencanaan Diet Diabetes Melitus
Terapi gizi medis merupakan salah satu terapi non farmakologis yang sangat direkomendasikan bagi pasien ddiabetes, Terapi gizi medis ini pada pronsipnya adalah melakukan pengaturan pola makan yang didasarkan pada stasus gizi medis diabetesi dan melakukan modifikasi diet berdasarkan kebutuhan individual. Beberapa manfaat yang telah
49

terbukti dari terapi gizi medis ini antara lain: Menurunkan berat badan, Menurunkan tekanan sistolik dan diastolik, Menurunkan kadar glukosa darah, Memperbaiki profil lipid, Meningkatkan sensitivitas reseptor insulin, Memperbaiki sistem koagulsi darah.
Tujuan Terapi Gizi Medis
Tujuan terapi gizi medis ini adlah untuk mencapai dan mempertahankan:
o Kadar glukosa darah mendekati normalo Glukosa puasa berkisar 90-130 mg/dl.o Glukosa darah 2 jam setelah makan <180 mg/dl.o Kadar A1c <7%.o Tekanan darah <130/80 mmHg.o Profil Lipido Kolesterol LDL<100 mg/dlo Kolesterol HDL >40 mg/dl.o Trigliserida < 150 mg/dl.o Beran badan senormal mungkin.
Jenis Bahan Makanan
KARBOHIDRAT
Sebagai sumber energi, KH yang diberikan diabetisi tidak boleh lebih dar 55-65% dari total kebutuhan energi sehari, atau tidak boleh lebih dari 70% jika dikombinasikan dengan pemberian asam lemak tidak jenuh rantai tunggal (MUFA: monounsaturated fatty acids). Pada setiap gram karbohidrat terdapat kandungan energi sebesar 4kilokalori.
Rekomendasi karbohidrat :
o Kandungan total kalori pada makanan yang mengandung KH, lebih ditentukan oleh jumlahnya dibandungkan dengan jenis KH itu sendiri.
o Dari total kebutuhan kalori perhari, 60-70% diantaranya berasal dari sumber KH.o Jika ditambah MUFA sebagai sumber energi, maka jumlah KH maksimal 70% dari total
kebutuhan kalori perhari.o Julah serat 25-50 gram per hari.o Jumlah sukrosa sebagai sumber energi tidak perlu dibatasi, namun jangan sampai lebih dari
total kebutuhan kalori perhari.o Sebagai pemanis dapat digunakan pmanis non kalori seperti sakarin, aspartame, acesulfame,
dan sukralosa.o Penggunaan alkohol harus dibatasi tidak boleh lebih dar10 gram/hari.o Fruktosa tidak boleh lebih dari 60 gram/hari.o Makanan yang mengandung sukrosa tidak perlu dibatasi.
PROTEIN
50

Jumlah kebutuhan protein yang direkomendasikan sekitar 10-15% dari total kalori perhari. Pada penderita kelainan ginjal dimana diperlukan pembatasan asupan protein sampai 40 gram perhari, maka perlu ditambahkan suplementasi asam amino esensial. Protein mengandung energi sebesar 2 kilokalori/gram.
Rekomendasi pemberian protein:
o Kebutuhan protein 15-20% dari total kebutuhan energi perhari.o Pada keadaan kadar glukosa yang terkontrol, asupan protein tidak akan mempengaruhi
konsentrasi glukosa darah.o Pada keadaan glukosa tidak terkontrol, pemberian protein sekitar 0,8-1,0 mg/kg BB/hari.o Pada gangguan fungsi ginjal, asupan protein diturunkan sampai 0,85 gram/KgBB/hari dan
tidak kurang dari 40gram.o Jika terdapat komplikasi kardiovaskular, maka sumber protein nabati lebih dianjurkan
dibanding protein hewani.
LEMAK
Lemak memiliki kandungan energi sebesar 9 kilokalori/gram. Bahan makanan ini sangat penting untuk membawa vitamin yang larut dalam lemak seperti vitami A, D, E, K. Berdasarkan rantai karbonnya , lemak dibedakan menjadi lemak jenuh dan tidak jenuh. Pembatasan asupan lemak jenuh dan kolestrol sangat disarankan pada diabetisi karena terbukti dapat memperbaiki profil lipid tidak normal bagi pasien diabetes. Asam lemak tidak jenuh rantai tunggal (monounsaturated fatty acid : MUFA), merupakan salah satu asam lemak yang dapat memperbaiki glukosa darah dan profil lipid. Pemberian MUFA pada diet diabetisi, dapat menurunkan kadar trigliserida, kolestrol total, kolestrol VLDL, dan meningkatkan kadar kolestrol HDL. Sedangkan asam lemak tidak jenuh rantai panjang (polyunsaturated fatty acid= PUFA) dapat melindungi jantung, menurunkan kadar trigliserida, memperbaiki agregasi trombosit. PUFA mengandung asam lemak omega 3 yang dapat menurunkan sintesis VLDL di dalam hati dan eningkatkan aktivitas enzyme lipoprotein lipase yang dapat menurunkan kadar VLDL di jarngan perifer. Sehingga dapat menurunkan kadar kolestrol LDL.
Rekomendasi Pemberian Lemak:
o Batasi konsumsi makanan yang mengandung lemak jenuh, jumlah maksimal 10% dari total kebutuhan kalori per hari.
o Jika kadar kolestrol LDL ≥ 100 mg/dl, asupan asam lemak jenuh diturunkan sampai maksimal 7% dari total kalori perhari.
o Konsumsi kolestrol maksimal 300mg/hari, jika ada kolestrol LDL ≥ 100 mg/dl, maka maksimal kolestrol yang dapat dikonsumsi 200 mg per hari.
o Batasi asam lemak bentuk trans.o Konsumsi ikan seminggu 2-3 kali untuk mencukupi kebutuhan asam lemak tidak jenuh rantai
panjang.o Asupan asam lemak tidak jenuh rantai panjang maksimal 10% dari asupan kalori perhari.
51

Penghitungan Jumlah Kalori
Perhitungan julah kalori ditentukan oleh stasus gizi, umur, ada tidaknya stress akut, dan kegiatan jasmani. Penetuan stasu s gizi dapat dipakai indeks massa tubuh (IMT) atau rumus Brocca.
Penentuan stasus gizi berdasarkan IMT
IMT dihitung berdasarkan pembagian berat badan (dalam kilogram) dibagi dengat tinggi badan (dalam meter) kuadrat.
o Berat badan kurang <18,5 o Berat badan normal 18,5-22,9o Berat badan lebih ≥ 23,0o Dengan resiko 23-24.9o Obes I 25-29,9o Obes II ≥ 30Penentuan stasus gizi berdasarkan rumus Brocca
Pertama-tama dilakukan perhitungan berat badan idaman berdasarkan rumus:
berat badan idaman (BBI kg) = (TB cm - 100) -10%.
Penetuan stasus gizi dihitung dari : (BB aktual : BB idaman) x 100%
o Berat badan kurang BB <90% BBIo Berat badan normal BB 90-110% BBIo Berat badan lebih BB 110-120% BBIo Gemuk BB>120% BBI
Untuk kepentingan praktis dalam praktek digunakan rumus Brocca.
Penentuan kebutuhan kalori perhari:
1. Kebutuhan basal:
o Laki-laki : BB idaman (Kg) x 30 kaloro Wanita : BB idaman (Kg) x 25 kalori
2. Koreksi atau penyesuaian:
o Umur diatas 40 tahun : -5%o Aktivitas ringan : +10%o Aktifitas sedang : +20%o Aktifitas berat : +30%o Berat badan gemuk : -20%o Berat badan lebih : -10%o Berat badan kurus : +10%
52

3. Stress metabolik : +10-30%
4. Kehamilan trimester I dan II : +300 kalori
5. Kehamilan trimester II dan menyusui : +500 kalori
Makanan tersebut dibagi dalam 3 porsi besar untuk makan pagi (20%), makan siang (25%), serta 2-3 porsi ringan (10-15%) di antara makan besar. Pengaturan makan ini tidak berbeda dengan orang normal, kecuali dengan pengaturan jadwal makan dan jumlah kalori. Usahakan untuk merubah pola makan ini secara bertahap sesuai kondisi dan kebiasaan penderita
LI 5. Memahami dan Menjelaskan Pandangan Islam terhadap Pola Makan yang Baik dan Benar
A. Hadis Tentang Tata Cara Makan di Meja Makan , : , �د�ي� ي �ت� وكان وسلم عليه الله صلى النبي ح�ج�ر� في غ!الم�ا !نت! ك قال سلمة ابي عمربن عن
)" , , , " : , مسلم رواه �ك �ي ل م�م.ا !ل� وك �ك �ن �م�ي �ي ب !ل� وك الله م0 س� غ!الم! � يا فقال الص.ح�ف�ة� في �ط�يش! توالبيهقى ) والطبراني
Dari umar bin abi salamah ia berkata: “Sewaktu aku kecil pada masa nabi SAW. tanganku selalu bergerak kesana kemari dalam piring makan, karena itu Nabi berkata: hai Anak sebutlah nama Allah, makanlah dengan tangan kanan engkau, dan makanlah yang ada di sekitarmu”. ( HR. Muslim, thabrani dan baihaqi )[1]
B. Perintah Makan Menggunakan Tangan Kanan
" : ر�ب� ش� �ذ�ا و�ا �ه� �ن �م�ي �ي ب !ل� �ك �ا �ي ف�ل !م� �ح�د!ك ا �ل� �ك ا �ذ�ا ا قال وسلم عليه الله صلى النبي عن هريرة ابي عنالسنان ( في والنسائ مسلم رواه �ه� م�ال �ش� ب ب! ر� �ش� و�ي �ه� م�ال �ش� ب !ل! �ك �ا ي �ط�ان� ي الش. �ن. ف�ا �ه� �ن �م�ي �ي ب ب! ر� �ش� �ي ف�ل
الكبرى)Dari abi hurairah ra dari Nabi SAW bersabda: “ jika salah seorang dari kalian makan,
makanlah dengan menggunakan tangan kanan dan jika minum, minumlah juga dengan tangan kanannya. Sesungguhnya syaitan itu makan dengan tangan kirinya dan juga minum dengan tangan kirinya. ( HR. Muslim dan Nasa’i di dalam sunan Kubro) [2]
C. Perintah Makan, Minum, dan Berpakaian Tanpa Berlebihan
و� , : � !وا ب ر� و�ش� !و�ا !ا ك قال انه وسلم عليه الله صلى النبي عن جده عن ابيه عن شعيب بن عمرو عن( االيمان ( شعب في البيهقى رواه Iة� �ل ي م�خ� و�ال� Iس�ر�ف �ر� غ�ي ف�ي � �ص�د.ق!وا و�ت و�ا �س! �ب ال
Dari umar bin syu’aib dari ayahnya dari kakeknya dari Nabi SAW, sesungguhnya Nabi Bersabda: makanlah, minumlah, berpakaianlah dan shodaqohlah tanpa berlebihan dan sikap sombong.( HR. Baihaqi pada bab iman)[3]
D. Membagi Perut Menjadi 3 Bagian
: ا Lر ش� و�ع�اء� Nد�م�ي� ا �ء� م�ال م�ا قال وسلم عليه الله صلى الله س!ول� ر� �ن. ا كرب معدي بن المقدام عن , �ه ب ا ر� ل�ش� Pل!ث! وث �ط�ع�ام�ه ل Pل!ث! ف�ث �ف�اع�ال �لة� ا �مح� ال �ان� ك �ن� ف�ا �ه! �ب ص!ل !ق�م�ن� ي Pم�ة� !ق�ي ل �د�م� ا �ن� اب �ح�س�ب� ب �ه� �ط�ن ب م�ن�
�ف�س�ه �ن ل Pل!ث! حبان( ) وث وابن الترمذى رواه
53

Dari miqdam bin ma’dikariba sesungguhnya Rasulullah SAW bersabda:“Tidaklah seorang anak Adam mengisi sesuatu yang lebih buruk dari perutnya sendiri , cukuplah bagi anak adam beberapa suap yang dapat menegakkan tulang punggungnya, jikapun ingin berbuat lebih, maka sepertiga untuk makanan dan sepertiga untuk minum dan sepertiga lagi untuk nafasnya. ( HR. Tirmidzi dan Ibnu Hibban)
DAFTAR PUSTAKA
Dorland, W. A. Newman. 2006. Kamus Kedokteran Dorland, Edisi 29. Jakarta: EGC
Eroschenko Victor P.(2003). Atlas Histologi di Fiore dengan Korelasi Fungsional. Jakarta.EGCGandasoebrata R . 2010 . Penuntun Laboratorium Klinik. Cetakan keenambelas . Jakarta : Dian
RakyatGuyton, AC. & Hall, JE. 2007. Buku Ajar Fisiologi Kedokteran, Edisi 11. Jakarta: EGC
Idrus, Alwi dkk. 2014. Buku Ajar Ilmu Penyakit Dalam,Jilid II Edisi VI. Jakarta: Interna Publishing.
Price, Sylvia A. 2005. Patofisiologi: Konsep Klinis Proses-proses Penyakit, Volume 2 Edisi 6. Jakarta: EGC
Putz, Reinhard & Reinhard Pabst. 2006. Atlas Anatomi Manusia Sobotta, Jilid 2 Edisi 22. Jakarta: EGC
Robbins, Stanley L. 2007. Buku Ajar Patologi Robbins, Volume 2 Edisi 7. Jakarta: EGC
Sherwood, Lauralee. (2011). Fisiologi Manusia : dari sel ke sistem. Ed. 6. Jakarta : EGC.
Snell, Richard.S.(1992). Anatomi Klinik untuk Mahasiswa Kedokteran, edisi 6. Jakarta : EGC
54
Related Documents