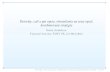
Heterocyklické deriváty triterpenů s cytotoxickou aktivitou M. Vlk a , J. Šarek b , M. Mayordomo Martínez a , M. Hajdúch c a T. Elbert d a Katedra jaderné chemie, Fakulta jaderná a fyzikálně inženýrská, ČVUT, Břehová 7, 128 43 Praha; e-mail: [email protected] b Katedra organické chemie, Přírodovědecká fakulta, Univerzita Palackého v Olomouci, Třída 17. listopadu 12, 772 00 Olomouc c Lab. experiment. medicíny, Dětská a Onkologická klinika, LF UP a FN Olomouc, Puškinova 6, 775 20 Olomouc d Laboratoř radioizotopů, Ústav organické chemie a biochemie, AV ČR, Flemingovo nám. 2, 166 10 Praha 6 Heterocyklické deriváty odvozené od lupanových, oleananových a taraxastanových skeletálních typů za- ujímají popřední místa v žebříčku zájmu výzkumu farmaceutických firem a vědeckých pracovišť díky roz- ličným biologickým aktivitám, jimiž disponuji. 1 V přírodě byly některé z těchto triterpenoidních derivátů, obsahujících přikondenzované heterocy- klické jádro na isoprenoidním skeletu, identifikovány a izolovány z živých organizmů. 2 V rámci dřívějšího výzkumu byly připraveny heterocyklické deriváty s pyrazinovým motivem, při- kondenzováním heterocyklických jader v poloze 2,3 lupanového a oleananového skeletu (funkcionalizace kruhu A). 3 Dříve byly rovněž připraveny deriváty s přikondenzovaným pyrazinovým cyklem jádrem ke kruhu E v polohách 21,22 lupanového skeletu, ovšem tyto sloučeniny nevykázaly cytotoxické aktivity. 3 Tato práce se zabývá syntézou pyrazinových derivátů odvozených od kyseliny ursonové (15), hetero- betulonové (22), moronové (28) a dále heterobetulinu (21) a moradiolu (27). Výše uvedené kyseliny, rovněž jako příslušné dioly, patří mezi deriváty taraxastanového, oleananového a ursanového skeletálního typu a byly již dříve popsány. V posledních letech však jejich výzkum nabývá na významu hlavně díky jejich an- tivirotickým a cytotoxickým účinkům. 4, 5, 6 V návrhu syntetických prací byly stanoveny jako cílové sloučeniny deriváty 18 - 20, 24 - 26, 30 - 32, 34 a 35. Nejprve byly syntetizovány výchozí sloučeniny 21, 23, 27 a 29 modifikací postupů již dříve v literatuře popsaných. 6 Prezentované výchozí sloučeniny 21 a 27 jsou výsledkem několikastupňové syntézy vycházející z betulinu (1). Heterobetulin (21) a moradiol (27) byly izolovány chromatograficky a dále jednotlivě oxido- vány na příslušné kyseliny 23 a 29 pomocí Jonesova činidla. Z reakční směsi byly izolovány rovněž chro- matografickou cestou a následně krystalovány. Kyselina ursonová (15) byla získána jemnou oxidací kyseliny ursolové (14) dichromanem sodným. Su- rová kyselina byla dále krystalována. Kondenzační reakce byly provedeny podle známého postupu, reakcí ethylendiaminu v bazickém prostředí morfolinu se sírou. Tímto postupem byly připraveny pyrazinové de- riváty 18, 19, 24, 25, 30 a 31; jejich methyl estery 20, 26 a 32 byly připraveny následnou methylací diazo- methanem. Sloučeniny s přikondenzovaným pětičlenným heterocyklickým jádrem byly připraveny kondenzační re- akcí bromallobetulonu s thiomočovinou v morfolinu. Takto byl získán aminothiazol 34, který byl po chro- matografické separaci dále diazotován na bromthiazolalon 35. Struktury všech připravených sloučenin byly jednoznačně potvrzeny spektrálními daty. Reference: 1. Dzubak P. et al.: Nat. Prod. Rep., 2006, 23, 394-411. 2. Pettit , G. R. et al.: J. Am. Chem. Soc. 1988, 110, 2006-2007. 3. Urban M. et al.: J. Nat. Prod., 2007, 70, 526-532. 4. Lobo-Echeverri T. et al.: J. Nat Prod., 2005, 68, 577-580. 5. Zhang P. et al: Tetrahedron., 2009, 65, 4304-4309. 6. Bradbury B. J., Huang M.: Substituted taraxastanes useful for treating viral infections. PCT Int. Patent Appl. WO 2007098247, 23 August 2007. 7. Krasutsky P. A. et al.: Nat. Prod. Rep., 2006, 23, 919-942. Betulin (1), kyselina betulinová (2) a betulonová (3) jsou dlouhodobě známé pro své cytotoxické, protivirové a protizánětlivé účinky. 7 Jejich pyrazinové deriváty 6 - 8 vykazují rovněž zajímavé cytotoxické účinky. Zvláště deriváty 7 a 8 vykazují signifikantní aktivity na liniích A 549, K 562 a taxol-rezistentní Pgp-expresivní linií K 562-tax (IC 50 0.25 – 8 µmol/L). 3 Naproti tomu uvedené benzopyraziny 9 - 11 aktivity nevyka- zovaly. 3 Kyselina oleanolová (12) a její pyrazinové deriváty 16 a 17 vykazují především antimutagení a antiangiogenní aktivity.1 Známá je však i je- jich cytotoxická aktivita na linii HeLa (IC 50 6.49 µg/ml). 5 Nově připravené deriváty 18 - 35 jsou v současné době ve stádiu tes- tování na kooperujícím pracovišti LEM FN UP Olomouc. Výsledky cy- totoxických aktivit některých derivátů na linii CEM uvádí Tabulka 1. Bylo připraveno 20 nových sloučenin s přikondenzovaným heterocyklickým jádrem. Zároveň byla zoptimalizována metoda přípravy výchozích substrátů 21 – 23 a 27 – 29. Byly testovány cy- totoxické aktivity všech připravených sloučenin na linii CEM. Poděkování Práce byla financována za laskavé podpory A/CZ 0046/1/0022 of FM EEA NORSKA, GAČR 305/09/1216 a Grantu Nadace pro výzkum rakoviny. Děkuji za technickou a finančni podporu prof. J. Johnovi, CSc a Mgr. D. Vopálkovi, CSc. z Katedry jaderné chemie, FJFI ČVUT Praha. Rovněž děkuji skupině z Laboratoře radioizotopů, ÚOCHB AV ČR za měření NMR spekter. N N R R 2 R 1 CO 2 R 1 R 2 R 3 N N R 2 R 1 COOH R 1 R 2 R 3 R 1 R 2 x R x N N R x N N N N R O O Br S N R R 1 R 2 x 1 α-H, β-OH CH 2 OH dvojná vazba 2 α-H, β-OH CO 2 H dvojná vazba 3 O CO 2 H dvojná vazba 4 α-H, β-OH CO 2 H jednoduchá vazba 5 O CO 2 H jednoduchá vazba R x 6 CH 2 OH dvojná vazba 7 CO 2 H dvojná vazba 8 CO 2 H jednoduchá vazba R x 9 CH 2 OH dvojná vazba 10 CO 2 H dvojná vazba 11 CO 2 H jednoduchá vazba R 1 R 2 R 2 12 α-H, β-OH α-CH 3 , β-CH 3 H, H 13 O α-CH 3 , β-CH 3 H, H 14 α-H, β-OH α-CH 3 , β-H α-H, β-CH 3 15 O α-CH 3 , β-H α-H, β-CH 3 R 1 R 2 R 3 16 H α-CH 3 , β-CH 3 H, H 17 H α-CH 3 , β-CH 3 H, H 18 H α-CH 3 , β-H α-H, β-CH 3 19 H α-CH 3 , β-H α-H, β-CH 3 20 CH 3 α-CH 3 , β-H α-H, β-CH 3 R 1 R 2 21 α-H, β-OH CH 2 OH 22 O CO 2 H 23 α-H, β-OH CO 2 H R 24 CH 2 OH 25 CO 2 H 26 CO 2 CH 3 R 1 R 2 27 α-H, β-OH CH 2 OH 28 O CO 2 H 29 α-H, β-OH CO 2 H R 30 CH 2 OH 31 CO 2 H 32 CO 2 CH 3 33 R 34 NH 2 35 Br Sloučenina IC 50 [μmol/L] 7 1.57 15 12.83 22 6.53 23 3.04 29 34.5 31 26.1 Tabulka 1: Cytotoxicita

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript
Heterocyklické deriváty triterpenů s cytotoxickou aktivitouM. Vlka, J. Šarekb, M. Mayordomo Martíneza, M. Hajdúchc a T. Elbertd
aKatedra jaderné chemie, Fakulta jaderná a fyzikálně inženýrská, ČVUT, Břehová 7, 128 43 Praha; e-mail: [email protected] organické chemie, Přírodovědecká fakulta, Univerzita Palackého v Olomouci, Třída 17. listopadu 12, 772 00 Olomouc
cLab. experiment. medicíny, Dětská a Onkologická klinika, LF UP a FN Olomouc, Puškinova 6, 775 20 OlomoucdLaboratoř radioizotopů, Ústav organické chemie a biochemie, AV ČR, Flemingovo nám. 2, 166 10 Praha 6
Heterocyklické deriváty odvozené od lupanových, oleananových a taraxastanových skeletálních typů za-ujímají popřední místa v žebříčku zájmu výzkumu farmaceutických firem a vědeckých pracovišť díky roz-ličným biologickým aktivitám, jimiž disponuji.1
V přírodě byly některé z těchto triterpenoidních derivátů, obsahujících přikondenzované heterocy-klické jádro na isoprenoidním skeletu, identifikovány a izolovány z živých organizmů.2
V rámci dřívějšího výzkumu byly připraveny heterocyklické deriváty s pyrazinovým motivem, při-kondenzováním heterocyklických jader v poloze 2,3 lupanového a oleananového skeletu (funkcionalizacekruhu A).3 Dříve byly rovněž připraveny deriváty s přikondenzovaným pyrazinovým cyklem jádrem kekruhu E v polohách 21,22 lupanového skeletu, ovšem tyto sloučeniny nevykázaly cytotoxické aktivity.3
Tato práce se zabývá syntézou pyrazinových derivátů odvozených od kyseliny ursonové (15), hetero-betulonové (22), moronové (28) a dále heterobetulinu (21) a moradiolu (27). Výše uvedené kyseliny, rovněžjako příslušné dioly, patří mezi deriváty taraxastanového, oleananového a ursanového skeletálního typu abyly již dříve popsány. V posledních letech však jejich výzkum nabývá na významu hlavně díky jejich an-tivirotickým a cytotoxickým účinkům.4, 5, 6
V návrhu syntetických prací byly stanoveny jako cílové sloučeniny deriváty 18 - 20, 24 - 26, 30 - 32, 34a 35. Nejprve byly syntetizovány výchozí sloučeniny 21, 23, 27 a 29 modifikací postupů již dříve v literatuřepopsaných.6 Prezentované výchozí sloučeniny 21 a 27 jsou výsledkem několikastupňové syntézy vycházejícíz betulinu (1). Heterobetulin (21) a moradiol (27) byly izolovány chromatograficky a dále jednotlivě oxido-vány na příslušné kyseliny 23 a 29 pomocí Jonesova činidla. Z reakční směsi byly izolovány rovněž chro-matografickou cestou a následně krystalovány.
Kyselina ursonová (15) byla získána jemnou oxidací kyseliny ursolové (14) dichromanem sodným. Su-rová kyselina byla dále krystalována. Kondenzační reakce byly provedeny podle známého postupu, reakcíethylendiaminu v bazickém prostředí morfolinu se sírou. Tímto postupem byly připraveny pyrazinové de-riváty 18, 19, 24, 25, 30 a 31; jejich methyl estery 20, 26 a 32 byly připraveny následnou methylací diazo-methanem.
Sloučeniny s přikondenzovaným pětičlenným heterocyklickým jádrem byly připraveny kondenzační re-akcí bromallobetulonu s thiomočovinou v morfolinu. Takto byl získán aminothiazol 34, který byl po chro-matografické separaci dále diazotován na bromthiazolalon 35.
Struktury všech připravených sloučenin byly jednoznačně potvrzeny spektrálními daty.
Reference:1. Dzubak P. et al.: Nat. Prod. Rep., 2006, 23, 394-411.2. Pettit , G. R. et al.: J. Am. Chem. Soc. 1988, 110, 2006-2007.3. Urban M. et al.: J. Nat. Prod., 2007, 70, 526-532.4. Lobo-Echeverri T. et al.: J. Nat Prod., 2005, 68, 577-580.5. Zhang P. et al: Tetrahedron., 2009, 65, 4304-4309.6. Bradbury B. J., Huang M.: Substituted taraxastanes useful fortreating viral infections. PCT Int. Patent Appl. WO 2007098247, 23August 2007.7. Krasutsky P. A. et al.: Nat. Prod. Rep., 2006, 23, 919-942.
Betulin (1), kyselina betulinová (2) a betulonová (3) jsou dlouhodoběznámé pro své cytotoxické, protivirové a protizánětlivé účinky.7 Jejichpyrazinové deriváty 6 - 8 vykazují rovněž zajímavé cytotoxické účinky.Zvláště deriváty 7 a 8 vykazují signifikantní aktivity na liniích A 549, K562 a taxol-rezistentní Pgp-expresivní linií K 562-tax (IC50 0.25 – 8µmol/L).3 Naproti tomu uvedené benzopyraziny 9 - 11 aktivity nevyka-zovaly.3
Kyselina oleanolová (12) a její pyrazinové deriváty 16 a 17 vykazujípředevším antimutagení a antiangiogenní aktivity.1 Známá je však i je-jich cytotoxická aktivita na linii HeLa (IC50 6.49 µg/ml).5
Nově připravené deriváty 18 - 35 jsou v současné době ve stádiu tes-tování na kooperujícím pracovišti LEM FN UP Olomouc. Výsledky cy-totoxických aktivit některých derivátů na linii CEM uvádí Tabulka 1.
Bylo připraveno 20 nových sloučenin s přikondenzovanýmheterocyklickým jádrem. Zároveň byla zoptimalizována metodapřípravy výchozích substrátů 21 – 23 a 27 – 29. Byly testovány cy-totoxické aktivity všech připravených sloučenin na linii CEM.
PoděkováníPráce byla financována za laskavé podpory A/CZ 0046/1/0022
of FM EEA NORSKA, GAČR 305/09/1216 a Grantu Nadace provýzkum rakoviny.
Děkuji za technickou a finančni podporu prof. J. Johnovi,CSc a Mgr. D. Vopálkovi, CSc. z Katedry jaderné chemie, FJFIČVUT Praha. Rovněž děkuji skupině z Laboratoře radioizotopů,ÚOCHB AV ČR za měření NMR spekter.
N
N
R
R2
R1
CO2R1
R2
R3
N
N
R2
R1
COOH
R1
R2
R3
R1
R2
x
R
x
N
N
R
x
N
N
N
N
R
O
O
Br S
N
R
R1 R2 x1 α-H, β-OH CH2OH dvojná vazba2 α-H, β-OH CO2H dvojná vazba3 O CO2H dvojná vazba4 α-H, β-OH CO2H jednoduchá vazba5 O CO2H jednoduchá vazba
R x6 CH2OH dvojná vazba7 CO2H dvojná vazba8 CO2H jednoduchá vazba
R x9 CH2OH dvojná vazba
10 CO2H dvojná vazba11 CO2H jednoduchá vazba
R1 R2 R2
12 α-H, β-OH α-CH3, β-CH3 H, H13 O α-CH3, β-CH3 H, H14 α-H, β-OH α-CH3, β-H α-H, β-CH315 O α-CH3, β-H α-H, β-CH3
R1 R2 R3
16 H α-CH3, β-CH3 H, H17 H α-CH3, β-CH3 H, H18 H α-CH3, β-H α-H, β-CH319 H α-CH3, β-H α-H, β-CH320 CH3 α-CH3, β-H α-H, β-CH3
R1 R2
21 α-H, β-OH CH2OH22 O CO2H23 α-H, β-OH CO2H
R24 CH2OH25 CO2H26 CO2CH3
R1 R2
27 α-H, β-OH CH2OH28 O CO2H29 α-H, β-OH CO2H
R30 CH2OH31 CO2H32 CO2CH3
33R
34 NH235 Br
Sloučenina IC50 [µmol/L]7 1.5715 12.8322 6.53 23 3.0429 34.531 26.1
Tabulka 1: Cytotoxicita
Related Documents