Ernst-Moritz-Arndt-Universiät Greifswald Institut für Botanik und Landschaftsökologie Wälder und ihre Degradationsstadien in der Kura-Niederung (West-Aserbaidschan) Jan Peper Diplomarbeit im Studiengang Landschaftsökologie und Naturschutz Mai 2006 Gutachter: Prof. Dr. Michael Succow Dr. Lebrecht Jeschke Förderung: DAAD

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript
Ernst-Moritz-Arndt-Universiät Greifswald
Institut für Botanik und Landschaftsökologie
Wälder und ihre Degradationsstadien
in der Kura-Niederung (West-Aserbaidschan)
Jan Peper
Diplomarbeit im Studiengang Landschaftsökologie und Naturschutz Mai 2006
Gutachter:
Prof. Dr. Michael Succow Dr. Lebrecht Jeschke
Förderung:
DAAD
VORWORT UND DANKSAGUNG Nachdem ich bereits 2004 die Auwälder am Tarim in der Wüste Takla-Makan während ei-
nes Projektpraktiums kennenlernte, schlug mir Prof. Dr. Michael Succow vor, diese Studien
an weiteren Auwäldern arider Gebiete fortzusetzen. Schnell rückte die Kura-Niederung in
Aserbaidschan in den Blickpunkt, wo im Zapovednik Garayazi noch große Waldflächen
vorhanden sind. Neben der rein landschaftsökologischen Arbeit sollte auch ein konkretes
naturschutzfachliches Konzept erstellt werden, um das aserische Umweltministerium bei
seinem ehrgeizigen Projekten, der Verbesserung des Schutzes der Natur im Lande und
besonders der Erhöhung des Waldanteiles, zu unterstützen.
Besonderer Dank gilt meinen Betreuern Prof. Dr. Michael Succow und Dr. Lebrecht Jeschke
die selbst den langen Weg nach Aserbaidschan nicht scheuten, um mir vor Ort mit ihrem
„Blick für die Landschaft“ wertvolle Ratschläge und Anregungen zu geben und sich auch
später gerne Zeit für fruchtbringende Diskussionen nahmen.
Dem langjährigen Aserbaidschankenner Jonathan Etzold verdanke ich viel Hilfe bei den
Reisevorbereitungen in Greifswald und zermürbenden Kontakten mit der aserbaidschani-
schen Botschaft.
In Baku war mir dann anfangs die Unterstützung durch Dr. Hartmut Müller, dem Vertreter
der Michael Succow Stiftung, gewiss, welcher mir die Türen beim Umweltministerium öff-
nete und viele bürokratische Hindernisse aus dem Weg räumte.
Mein größter Dank gilt der Familie Musayev in Muganli, die mich mit landestypischer Gast-
freundschaft aufnahm, mich hervorragend beköstigte und sehr schnell in die Dorfgemein-
schaft integrierte. Besonders der Hausherr Nabi, seines Zeichens wissenschaftlicher Leiter
im Schutzgebiet, half mir bei der Geländearbeit und begeisterte sich für Holzmesskunde.
Großen Respekt zolle ich den immer entgegenkommenden Dorfbewohnern, die unter
schwierigen Umständen ihr Leben meistern, besonders aber den Frauen, welche täglich
mehr als 16 Stunden in Haus und Hof arbeiten müssen um ihre Familien zu ernähren.
Danken möchte ich dem Umweltministerium Aserbaidschans und der Verwaltung des Za-
povedniks für Genehmigungen und Unterstützung.
Ich danke weiterhin Prof. Dr. Michael Manthey, Prof. Dr. Peter A. Schmidt, Dr. Ingo Holz
Niels Thevs, Sebatian Schmidt und Philipp Meister für viele fachliche Ratschläge, den Kriti-
kern Falk Harnisch, Philipp Pratap Thapa, Cosima Tegetmeyer und Norman Donner, sowie
meiner Familie, die mir in Nah und Fern zur Seite stand.
Nicht zuletzt habe ich mich über das Stipendium des Deutschen Akademischen Austausch-
dienstes gefreut.
Hiermit erkläre ich die vorliegende Diplomarbeit mit dem Thema:
„Wälder und ihre Degradationsstadien in der Kura-Niederung (West-Aserbaidschan)“
selbstständig verfasst und keine anderen Hilfsmittel als die angegebenen verwendet zu ha-
ben. Aus anderen Werken in Wortlaut oder Sinngehalt entnommene Inhalte sind durch
Quellenverweis, auch für Sekundärliteratur, kenntlich gemacht.
Greifswald, den 16.05.2006
Jan Peper
Kontakt:
Jan Peper
Gräfenhainer Straße 9
01936 Königsbrück
Bildnachweis Titelblatt: oben: Blick vom Südufer der Kura auf die Wälder im Untersuchungsgebiet bei Hochwasser. (Juni 2005) unten: Beweidete Talterrasse im Schutzgebiet Garayazi. Im Hintergrund Ausläufer des Kleinen Kaukasus. (April 2005)
Inhaltverzeichnis
1 Einleitung und Fragestellung 1
2 Untersuchungsgebiet 2
2.1 Lage 2 2.2 Geologie 3 2.3 Klima 3 2.4 Abflussverhältnisse der Kura 5 2.5 Boden, Vegetation und Landnutzung am Mittellauf 5
3 Methoden 7
3.1 Auswahl der Aufnahmeflächen 7 3.2 Abiotische Standortfaktoren und Nutzungsgrad 8 3.3 Vegetationskunde 8
4 Ergebnisse 13
4.1 Überblick über die Terrassenniveaus 13 4.2 Feuchtgrünland auf der 1. bis 3. Terrasse 15 4.3 Wälder mit Degradationsstadien 24
4.3.1 Altersbestimmung der Pappeln und Eichen 24 4.3.2 Die Wälder und ihre Degradationsstadien im Überblick 26 4.3.3 Eichen-Ulmenwälder 26 4.3.4 Graupappelwälder 34 4.3.5 Weichholzwälder 41
4.4 Sozioökonomische Situation der umliegenden Dörfer 45 4.5 Zustand des Schutzgebietes 49
5 Diskussion 53
5.1 Relief und Hydrologie der Niederung 53 5.2 Die Weidelandschaft der Terrassen 54 5.3 Dynamik der Vegetation in der Aue 60
5.3.1 Die Rolle der nichteinheimischen Gehölzarten 66 5.4 Die Kura-Niederung ohne Nutzung 67 5.5 Vergleich mit anderen Auwäldern 69
6 Managementempfehlungen 72
6.1 Einleitung 72 6.2 Schutzziele 72 6.3 Gefährdungen 74 6.4 Maßnahmenkatalog 75 6.5 Touristische Nutzung 78
7 Fazit und Ausblick 79
8 Zusammenfassung 80
9 Summary 82
10 Literaturverzeichnis 85
Tabellenverzeichnis Tab.3.1 Wertetabelle für eine PCQ-Aufnahme am Beispiel K17 10
Tab.3.2 Kennwerte für den Bestand und die Baumarten der Aufnahme K 17 11
Tab.4.1 Übersichtstabelle des Feuchtgrünlandes 18
Tab.4.2 Vegetationstypen der Wälder 26
Tab.4.3 Übersichtstabelle der Eichen-Ulmenwälder 28
Tab.4.4 Übersichtstabelle der Graupappelwälder 37
Tab.4.5 Übersichtstabelle der Weichholzwälder 41
Tab.4.6 Nutztiere und Nutzpflanzen 46
Tab.4.7 Kostenrechnung für ein Maisfeld 47
Tab.5.1 Sukzession auf der 1. Terrasse 58
Tab.5.2 Strategien und Standortsansprüche der Gehölzarten 61
Tab.5.3 Eingeführte Gehölze 66
Tab.5.4 Vergleich eurasischer Auwälder 70
Tab.6.1 Empfohlene Höhe der Weidegebühren 76
Abkürzungsverzeichnis AG Artengruppe
Akh Arbeitskraftstunde
DCA Detrended Correspondence Analysis (Korrespondenzanalyse)
GVE Großvieheinheiten
GW Grundwasser
HW Hochwasserlinie
I Wichtigkeit einer Gehölzart im Bestand (Importance)
KA 4 Kartieranleitung Boden 1994
KA 5 Kartieranleitung Boden 2005
m NN Höhe über Normalnull
MW Mittelwasserlinie
PCQ Point-Centered Quarter Method
sp Species (Art)
spp Species (Arten)
SSCAR State Statistical Committee of Azerbaijan Republic
ssp Subspecies (Unterart)
US$ US-Dollar
WRB World Reference Base (Internationale Referenz zur Bodenbenennung)
Abbildungsverzeichnis Abb.2.1 Lage des Untersuchungsgebietes 2Abb.2.2 Geologie 3Abb.2.3 Klima 4Abb.2.4 Querschnitt durch die Kura-Niederung 6Abb.2.5 Boden und Vegetation 6 Abb.3.1 Lage der Untersuchungsflächen 7Abb.3.2 Anlage der Aufnahmeflächen 10Abb.3.3 Aufnahmeanordnung der PCQ-Methode 10 Abb.4.1 Kausalprofil durch das Untersuchungsgebiet 13Abb.4.2 Wald-Offenland Mosaik 14Abb.4.3 Auwald bei Überflutung 14Abb.4.4 Blick über das Feuchtgrünland 15Abb.4.5 Schematischer Querschnitt durch das Feuchtgrünland 15Abb.4.6 Cladium-Ried 16Abb.4.7 Nasturtium Sparganium-Ried 17Abb.4.8 Nasturtium Catabrosa-Ried 17Abb.4.9 DCA des Feuchtgrünlandes 19Abb.4.10 Tümpel mit Zannichellia-Tauchflur 20Abb.4.11 Catabrosa aquatica 20Abb.4.12 Veronica catenata 21Abb.4.13 Karte des Schlenkensystems 21Abb.4.14 Carex otrubae-Rasen 22Abb.4.15 Scorzonera-Wiese 23Abb.4.16 Convolvulus-Rasen 23Abb.4.17 Wachstumskurve von Quercus robur 24Abb.4.18 Wachstumskurve von Populus nigra 25Abb.4.19 Wachstumskurve von Populus x canescens 25Abb.4.20 Quercus-Wald 27Abb.4.21 Kennzahlen des Quercus-Waldes 27Abb.4.22 DCA der Eichen-Ulmenwälder 29Abb.4.23 Carduus-Wald 30Abb.4.24 Kennzahlen des Carduus-Waldes 30Abb.4.25 Baumhöhen des Carduus-Waldes 30Abb.4.26 Origanum-Wald 32Abb.4.27 Kennzahlen des Origanum-Waldes 32Abb.4.28 Baumhöhen des Origanum-Waldes 32Abb.4.29 Verbascum-Lichtung 33Abb.4.30 Schematischer Querschnitt durch die Aue 34Abb.4.31 Vincetoxicum-Wald 35Abb.4.32 Kennzahlen des Vincetoxicum-Waldes 35Abb.4.33 Baumhöhen des Vincetoxicum-Waldes 35Abb.4.34 DCA der Graupappelwälder 36Abb.4.35 Alliaria-Wald 38Abb.4.36 Kennzahlen des Alliaria-Waldes 38
Abb.4.37 Baumhöhen des Alliaria-Waldes 38 Abb.4.38 Tilia-Wald 39 Abb.4.39 Kennzahlen des Tilia-Waldes 39 Abb.4.40 Baumhöhen des Tilia-Waldes 39 Abb.4.41 Normvega im Tilia-Wald 39 Abb.4.42 Periploca-Lichtung 40 Abb.4.43 Flusslauf nach Hochwasser 41 Abb.4.44 Tamarix-Weichholzaue 42 Abb.4.45 Populus-Weichholzaue 43 Abb.4.46 Kennzahlen der Populus-Weichholzaue 43 Abb.4.47 Alnus-Bachsaum 44 Abb.4.48 Kennzahlen des Alnus-Bachsaumes 44 Abb.4.49 Landschaft am Südufer 45 Abb.4.50 Feldbau bei Muganli 45 Abb.4.51 Feuerholznutzung + Situation im Dorf 48 Abb.4.52 Organigramm der Schutzgebietsverwaltung 50 Abb.4.53 Satellitenbild der Schutzgebiete Garayazi und Gardabani 51 Abb.4.54 Gefährdungen des Schutzgebietes 51 Abb.5.1 Schotterterrassen und Quellkuppe 53 Abb.5.2 Schematischer geologischer Querschnitt durch die Niede-
rung 53
Abb.5.3 Hudewald und Abbrennen von Gebüschen 55 Abb.5.4 Entstehung der Tümpel und Schlenken 56 Abb.5.5 Salzanreicherung und Viehtrift 56 Abb.5.6 Vegetationskarte des Schutzgebietes von 1976 59 Abb.5.7 Resultate eines Hochwassers 61 Abb.5.8 Gehölzgruppen mit Kennzahlen der Auwälder 63 Abb.5.9 Entstehung einer Periploca-Lichtung 64 Abb.5.10 Sukzessionsschema der Auwälder 65 Abb.5.11 Vegetation ohne Nutzung 67 Abb.5.12 Lage der verglichenen Auwälder 71
Einleitung
1
1 EINLEITUNG UND FRAGESTELLUNG Durch Gewässerausbau und Nutzung als fruchtbares Ackerland wurden die Auen Eura-
siens schon vor Jahrhunderten stark verändert, so dass es heute nur wenige Flusstäler mit
ausgedehnten Auwäldern gibt, in denen die Auendynamik noch weitgehend ungestört ab-
läuft.
Im ca. 100 km² großen Zapovednik (Naturschutzgebiet) Garayazi am Mittellauf des größten
transkaukasischen Flusses, der Kura, wachsen inmitten eines Steppengebietes Auwälder
und auf Terrassen grundwassergespeiste Niederungswälder. Dieses Gebiet im Westen
Aserbaidschans soll bereits 1701 als Jagdreservat des Russischen Zaren unter Schutz gestellt
worden sein (Musajev 1984, siehe auch Radde 1899), und zählt damit weltweit zu den ältes-
ten Waldschutzgebieten überhaupt. Erstaunlicherweise rückte es kaum in den Blickpunkt
der Wissenschaft.
Erste Beschreibungen lieferte der Botaniker Radde 1899. Ihm folgte Grossheim (1948) mit
einem groben Überblick über die Wälder der Kura-Niederung. Die Arbeiten Prilipkos orien-
tierten sich an diesen Erkenntnissen, vertieften die Materie aber kaum (Prilipko 1954, 1970;
Gulisaschvili et al. 1975). Zuletzt kartierten Alijew & Chalilov 1976 die Wälder entlang der
Kura nach rein forstlichen Gesichtspunkten und warnten schon vor einer Degradation der
Bestände durch Austrocknung und Beweidung. Inzwischen wurden große Talsperren ge-
baut, und die Landnutzung durch Gründung von Genossenschaften stark verändert. Um
1991, nach dem Zusammenbruch der Sowjetunion, setzte eine Übernutzung der Landschaft
ein, die auch vor Naturschutzgebieten nicht halt machte (Schmidt 2005). Seit nunmehr 30
Jahren existieren keine neuen Studien über den Zustand der Wälder und die Wirksamkeit
der Schutzbestimmungen im Schutzgebiet.
Diese Umstände gaben Anlass für folgende Fragestellungen bezüglich der Wälder und ihrer
Degradationsstadien im Zapovednik Garayazi:
1. Welche Vegetationstypen mit welchen Standortsansprüchen sind vorhanden?
2. Wie prägen die einzelnen Gehölzarten die Struktur der Wälder?
3. Lässt sich anhand der Daten eine Sukzessionsreihe von einer Weichholz- zu einer Hart-
holzaue ableiten, oder existiert nur eine Weichholzaue wie in den Tugai-Wäldern Mit-
telasiens?
4. In welchem Zustand befindet sich das Zapovednik Garayazi, und welche Maßnahmen
sind nötig um einen dauerhaften Schutz zu gewährleisten?
Untersuchungsgebiet
2
2 UNTERSUCHUNGSGEBIET
2.1 Lage
Das Untersuchungsgebiet befindet sich in Transkaukasien im Westen Aserbaidschans an
der Grenze zu Georgien bei 41°20’ Nord und 45°11’ Ost etwa 230 m über dem Meeresspiegel
(Abb.2.1). Hier fließt die Kura durch das 97 km² große Naturschutzgebiet Garayazi in die
sich ostwärts öffnende Kura-Niederung. Nach Süden begrenzt das rechte Steilufer des Flus-
ses und nach Westen die georgische Grenze das Gebiet. Im Norden und Osten bildet die
Eisenbahntrasse Baku - Tiflis die Umgrenzung des untersuchten Raumes. Das engere Unter-
suchungsgebiet umfasst einen ein Kilometer breiten Streifen zwischen der Kura und dem
Ort Muganli (siehe auch Abb.5.2) sowie Kiesbänke bei Garayazi.
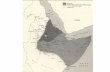
Abb.2.1: Das Naturschutzgebiet (Zapovednik) Garayazi im Zusammenschnitt der topographischen Karten 1:100 000 Ka-sach und Rustavi (Skworzow 1976a+b); kleine Karte mit Übersicht der Kaukasusrepubliken (World Sites Atlas 2005)
Untersuchungsgebiet
3
2.2 Geologie Die Transkaukasische Depression teilt sich in zwei Niederungsbereiche, die Kolchis-Niede-
rung im Westen und die Kura-Niederung im Osten, welche durch das bis zu 2000 m hohe
Surami Bergland getrennt werden (Neef 1956). Das Surami Bergland, der Große Kaukasus
im Norden, sowie das Hochland von Armenien am Südrand, bedingen wesentlich das Kli-
ma und die Abflussregime. Nach Franz (1973) sind diese Beckenstrukturen mit mesozoi-
schen bis paläogenen Flyschen gefüllt, über denen tertiäre und quartäre fluviatile Sedimente
lagern. In den transkaukasischen Mittelgebirgen und den Vorbergen am Rande der Binnen-
becken treten carbonatreiche jurassische und kretazische Schichten zutage (Dolginow &
Kropatschjow 1994; Mamedaliew 1963). Dort wird kalkhaltiges Material abgetragen und in
den Auen sedimentiert. Die große Hangneigung der jungen Gebirge führt zu hohen Abtra-
gungsraten mit erheblichen Geröll- und Schwebstofftransportraten der Flüsse (Franz 1973).
Im Pleistozän wurden am Kura-Mittellauf mächtige Terrassen der Bakinskier und Neukas-
pischen Folge abgelagert, die stellenweise von neogenen Schichten durchragt werden (Ma-
medaliew 1963) (Abb.2.2). Die holozänen carbonatreichen Auensedimente bilden den jüngs-
ten geologischen Horizont in der Kura-Niederung.
2.3 Klima Die Transkaukasische Depression weist einen starken Klimagradienten von West nach Ost
auf. Im feuchtgemäßigten Klima der Kolchis an der Schwarzmeerküste bringen Steigungs-
regen Niederschläge von über 2000 mm pro Jahr (Mühr 2005). Nach Osten, im Lee des Su-
ramischen Scheidegebirges, nehmen die Niederschläge bis zum Kaspischen Meer stetig ab.
In Tiflis, ca. 60 km westlich des Untersuchungsgebietes, fallen noch 492 mm und in Agstafa,
Abb.2.2: Geologie des Kura-Mittellaufes (Ausschnitt der Geologischen Karte 1:1,5 Mio (Mamedaliew 1963) )Das Schutzgebiet liegt im roten Rechteck
Obere Kreide Untere Kreide Oberes Jura
Cr2
Cr1
J3
Mesozoikum:
Paläogen Pg
Tertiär:
Neogen N
Kaspische Folge Gjurkinskische und Bakinskische Folge
Q4
Q1
Quartär:
N Legende:
Untersuchungsgebiet
4
ca. 30 km östlich des Gebietes gelegen, nur noch 359 mm Niederschlag pro Jahr (Abb.2.3).
Somit liegt der Kura-Mittellauf im subhumiden Übergangsbereich vom feuchtgemäßigten
Klima zum semiariden Steppenklima (UNESCO 1977; Mühr 2005). Die Niederschläge wei-
sen Spitzen von April bis Juni und im Oktober auf, wenn feuchte westliche Strömungen
einfließen. Im Winter dominieren östliche Winde mit trockener Kontinentalluft (Franz 1973).
Die im Sommer über das Kaspische Meer einströmenden östlichen Luftmassen werden über
dem Festland so stark erwärmt, dass die Niederschläge im Juli und August auf 28 mm pro
Monat absinken.
Für das Arbeitsgebiet konnten lokale Klimaaufzeichnungen von Nabi Musayev (unveröff.)
für den Ort Muganli verwendet werden (Abb.2.3). Er vermerkt u.a. alle Tage mit Nieder-
schlag. Es ergeben sich auch hier Spitzen im April und Oktober mit acht bzw. sechs Tagen
Niederschlag pro Monat.
Der Große Kaukasus riegelt Transkaukasien klimatisch nach Norden ab, so dass nur sehr
selten arktische Kaltluftmassen eindringen können (Neef 1956). In diesem subtropisch ge-
prägten Klima mit einer Jahresmitteltemperatur von ca. 13°C (Mühr 2005) sind die Winter
mild und ohne starke Fröste. Im Sommer steigen die mittleren Tagestemperaturen auf 25°C
und im Juni setzt aufgrund der geringen Niederschläge und hohen Temperaturen eine bis
September andauernde Trockenphase ein.
Abb.2.3: links: Klimadiagramme von Tiflis (Honkong Observatory 2005) und Agstafa (Alijew & Chalilov 1976), mit Einteilung in Klimaklassifikation nach Köppen aus Mühr (2005)
rechts: Verteilung der Tage mit Niederschlag im Untersuchungsgebiet (Daten: Nabi Musayev (unveröff.) 1984, 1993-1996 und 1999 – 2005 )
BSk Cfa
0
1
2
3
4
5
6
7
8
9
J F M A M J J A S O N D
Tag
e m
it N
ied
ers
chla
g
Muganli 41°21’N / 45°15’E / 245m
mm
Georgia
Tiflis41.70°N / 45.00°E / 490m
[30-30] +13.0°C 476mm
°C
J F M A M J J A S O N D0
10
20
30
40
50
60
70
80
90
100
200
300
10
20
30
40
50
0mm
Azerbaijan
Agstafa41.10°N / 45.45°E / 331m
[ ] +12.2°C 359mm
°C
J F M A M J J A S O N D0
10
20
30
40
50
60
70
80
90
100
200
300
10
20
30
40
50
0
Untersuchungsgebiet
5
2.4 Abflussverhältnisse der Kura Die hydrogeographischen Kenndaten sind im Aserbaidschanischen Atlas von Mamedaliew
(1963) dargestellt. Danach ist die Kura mit 1515 km Länge und 188 000 km² Einzugsgebiet
der größte Fluss der Kaukasusregion. Sie entspringt in der Türkei bei 2740 m NN, fließt
durch Georgien und mündet bei ca. -28 m NN in das Kaspische Meer. Der Mittelwasserab-
fluss im Untersuchungsgebiet beträgt 397 m³/s. Zum größten Teil wird der Abfluss durch
Regenwasser, zu 5 % durch Schmelzwasser und zu 30 % durch Grundwasser gespeist. Mit
den hohen Frühjahrsniederschlägen liegt auch das Abflussmaximum mit 750 m³/s im Mai
am höchsten und im trockenen Januar mit 120 m³/s am niedrigsten. Bei Spitzenabfluss wer-
den 2,6 t Schwebfracht pro Sekunde transportiert. Da in Georgien und der Türkei keine gro-
ßen wasserbaulichen Maßnahmen die Flussdynamik behindern, sind die Abflussverhältnis-
se am Mittellauf noch weitgehend unbeeinflusst. Der verwilderte, breite Flusslauf entsteht
durch ein Gleichgewicht von Frachtzu- und abfuhr bei hohen Transportraten (Bridge 2003).
So ändert sich die Lage des Flussbettes praktisch mit jedem Hochwasserereignis, was im
Untersuchungszeitraum viermal der Fall war.
Flussabwärts wurde 1953 die Talsperre Mingeschaur mit einer Vorsperre in Betrieb ge-
nommen, woraufhin unterhalb die Stofffracht erheblich abnahm und eine Eintiefung des
Flusses erfolgte.
2.5 Boden, Vegetation und Landnutzung am Mittellauf
Entsprechend des Luv-Lee Formenwandels ändert sich auch die zonale Vegetation Trans-
kaukasiens von West nach Ost. In der Kolchis stocken Wälder von der Küstenebene auf-
wärts, wohingegen im Regenschatten des Suramischen Berglandes sich eine untere Wald-
grenze ausgebildet hat. Am Mittellauf liegt diese heute bei etwa 900 m NN auf armenischem
Territorium (Abb.2.4).
Pflanzengeographisch zählt das Gebiet zur zentralkaukasischen-araxischen Provinz der ost-
submeridional-turanischen Florenregion (Meusel et al. 1965).
An der Waldgrenze gehen Eichen-Hainbuchenwälder auf Zimtböden (Kalk-Braunerden) in
tieferen Lagen über Schibljakformationen aus Christusdorn (Pailurus spina-christi) und
Kreuzdorn (Rhamnus pallasii) in Steppen auf Kastanosemen über (Prilipko 1970; Mameda-
liew 1963) (Abb.2.5). Unterhalb 300 m NN beginnt auf Hellen Kastanosemen die Zone der
Artemisia-Halbwüsten (Prilipko 1970), die aber im Gebiet eher Steppencharakter besitzen.
Die sich im Tal anschließenden azonalen Niederungs- und Auwälder mit ihren Degradati-
onsstadien, sind das Untersuchungsobjekt.
Untersuchungsgebiet
6
Viele Terrassenebenen werden als Äcker für die Mais-, Hirse-, Kartoffel- und Weizenpro-
duktion genutzt. Südlich der Kura, oberhalb 300 m NN kommen die Kulturen ohne Bewäs-
serung aus, in der Niederung wird jedoch bewässert. Alle hängigeren Gebiete unterliegen
einer sehr starken Beweidung durch Schafe, Rinder und Wasserbüffel. Prilipko (1970) be-
merkte schon, dass dadurch die Eichen-Niederungswälder aus Quercus robur pedunculiflora
und auch die Übergangswälder der unteren Waldgrenze stark zurückgedrängt wurden.
Wald-Zimtböden Graue-Zimtböden Kastanoseme Helle Kastanoseme Alluviale Wald- und Wiesenböden
8 11 13 19 25
N Legende:
Niederungswälder Tugai–Wälder Schibljak Pistazien–Lichtwald Feuchtwiesen der Niederung Berg-Trockenvegetation Steppe Artemisia–Halbwüste
3 4 5 6 11 13 14 16
N Legende:
Abb.2.5: Ausschnitte der Bodenkarte 1:1,5 Mio (links) und Vegetationskarte 1:1,5 Mio (rechts) aus Mamedaliew (1963) Das Schutzgebiet liegt im roten Rechteck. Der Querschnitt in Abb.2.4 verläuft ungefähr entlang der roten Linie im rechten Bild.
Abb.2.4: Querschnitt durch die Kura-Niederung am Untersuchungsgebiet. Höhendaten und Waldgrenzen aus den topograpischen Karten Kasach und Rustavi (Skworzow 1976a+b).
Methoden
7
3 METHODEN
3.1 Auswahl der Aufnahmeflächen Die Feldarbeiten fanden zwischen Ende März und Anfang Juni 2005 statt. Zur Charakteri-
sierung der Landschaft wurden innerhalb eines Korridors von 1x5 km vom Dorf Muganli
senkrecht zur Kura 126 Untersuchungsflächen in quasi-homogenen Beständen eingerichtet
(Abb.3.1). Da hier die Weichholzaue nicht zugänglich war, wurden ca. 4 km flussabwärts
bei Garayazi entsprechende Flächen mit einbezogen. Zur Veranschaulichung wurden die
Daten zu landschaftsökologischen Kausalprofilen (Billwitz 1997) und Schemata zusammen-
gefasst. Mit meiner Einschätzung zum Gebietszustand beziehe ich mich auf das gesamte
Schutzgebiet und die angrenzenden Räume.
Abb.3.1: Lage der Untersuchungsflächen (Kartengrundlage Landsat-Satellitenbild (NASA 2006))
Methoden
8
3.2 Abiotische Standortfaktoren und Nutzungsgrad
Für jede Aufnahme wurden per GPS Gerät (Garmin Etrex) die Koordinaten, die Entfernung
zum Fluss und zum Dorf sowie die Höhe über Normalnull ermittelt. Im Gelände zeichneten
sich mehrere Terrassenniveaus deutlich ab, deren Höhe untereinander mit dem BLUME-
LEISS Höhenmesser (siehe Prodan 1951) bestimmt wurde.
Der Grundwasserflurabstand wurde auf der 4. Terrasse, also am Dorfrand, in den Haus-
brunnen per Bandmaß gemessen. Ansonsten erreichten die Bodenschürfe das Grundwasser,
oder die Tiefe musste geschätzt werden. Deshalb sind diese Angaben gerade im Auenbe-
reich mit Vorbehalt zu betrachten.
Im Auwald wurde die Höhe der Überflutung anhand frischer Flutmarken einheitlich nach
dem höchsten Wasserstand Ende April an allen Aufnahmepunkten gemessen.
Im Wald wurden auf jeder Fläche, und auf dem Grünland an ausgewählten Stellen, Boden-
schürfe angelegt, die im Zentrum der Probeflächen lagen. An ihnen wurden jeweils die Sub-
strat- und Horizontfolge, der Carbonat- und Humusgehalt sowie Feuchte und Farbe per
Feldansprache nach KA 4 (AG Boden 1994) bestimmt (siehe Anh.6). Die Benennung der Bo-
dentypen enstprechend der deutschen und internationalen Nomenklatur (World Reference
Base) folgt der KA 5 (AG Boden 2005) und die Einordnung in das russische System ent-
spricht den Einheiten der Bodenkarte Russlands (Stolbovoi 2000). Da die Standorte unter-
schiedlich stark anthropogen beeinflusst sind, wurde der Nutzungsgrad in einer Skala von
„1“ für ungestört bis „3“ für starke ganzjährige Beweidung, Holzeinschlag oder andere me-
chanische Störungen erfasst.
3.3 Vegetationskunde
3.3.1 Flora Die Bestimmung der Pflanzen vor Ort erfolgte mit der Exkursionsflora von Deutschland
(Rothmaler et al. 2002). Unbekannte Arten wurden herbarisiert und später mit der Flora
Kavkasa (Grossheim 1949-1967) und Flora Aserbaidschana (Karjagin 1950-1961) bestimmt.
Die Nomenklatur der Gehölzpflanzen folgt den bisher erschienen Teilen der Übersicht
„Bäume und Sträucher Kaukasiens“ (Schmidt 2002-2005), für die Moose der Moosflora Mit-
teleuropas (Frahm & Frey 1992), für die auch in Deutschland vorkommenden krautigen
Arten der Exkursionsflora (Rothmaler et al. 2002) und für die weiteren Arten der Russischen
Referenzliste (Czerepanov 1995). Aufgrund fehlender Blütenstände konnten einige Arten
nur bis auf Gattungsebene bestimmt werden. Alle im Gebiet angetroffenen und bestimmten
Arten und Unterarten sind mit Autorenangabe in Anh.4 aufgeführt.
Methoden
9
3.3.2 Vegetationsaufnahmen Sowohl Offenland- als auch Waldvegetation wurden im Arbeitsgebiet erfasst. Im Offenland
wurde dabei mit quadratischen Aufnahmeflächen von 25 m² gearbeitet und die Artmäch-
tigkeit nach der einfachen Braun-Blanquet-Skala geschätzt.
Für Aufnahmen in Wäldern wird eine Mindestfläche von 200 m² gefordert (Glavac 1996).
Um dem Rechnung zu tragen, wurden die Baum-, Strauch- und Lianenschicht im 22 x 22 m
Quadrat aufgenommen und die Krautschicht in fünf Subplots zu je 25 m² (Abb.3.2). In allen
fünf Aufnahmen wurde nun der Deckungsgrad in Prozent geschätzt. Der Durchschnitt der
Einzelwerte wurde in die einfache Braun-Blanquet Skala übertragen und für die weitere
Datenanalyse verwendet.
3.3.3 Vegetationskartierung Das Feuchtgrünland auf der 3. Terrasse weist ein feinverzweigtes Schlenkensystem mit un-
terschiedlichen Vegetationstypen auf. Zur Veranschaulichung wurde ein 100 x 140 m großer
Ausschnitt kartiert (Abb.4.13). Als Kartiereinheiten wurden drei im Feld gut erkennbare
Vegetationstypen verwendet. Das Gebiet wurde mit Kompass und GPS-Gerät in einem
10 x 10 m Raster abgelaufen und die jeweils umgebende Fläche kartiert.
3.3.4 Point-Centered Quarter (PCQ) Method Waldbestände lassen sich anhand forstlicher Kennzahlen, wie Bestandesdichte und Wich-
tigkeit (Importance) der einzelnen Baumarten charakterisieren und vergleichen. Daher
wurden auf Untersuchungsflächen im Wald mit der personalextensiven PCQ-Methode
(Mitchell 2001; Cottam & Curtis 1956) Bäume vermessen. Ihr Nachteil, die Unterschätzung
der Gehölzartenvielfalt (Bryant et al. 2005), wird durch die parallel durchgeführten Vegeta-
tionsaufnahmen kompensiert. Als Baum galt jede lebende Pflanze mit mehr als 12 cm
Brusthöhenumfang.
Gemäß Abb.3.3 wird die Fläche vom Zentrum per Kompass in vier Quadranten unterteilt
und in jedem Quadranten mit einem Maßband die Entfernung zwischen Zentrum und
nächstgelegenem Baum und sein Brusthöhenumfang gemessen, sowie dessen Art notiert.
Diese Prozedur wird in allen vier Himmelsrichtungen in 15 m Entfernung zum Zentrum
wiederholt, so dass am Ende Werte von je 20 Bäumen wie im Beispiel K17 (Tab.3.1) vorlie-
gen.
Methoden
10
Danach wurde der Durchmesser und die Grundfläche der Bäume errechnet. Nun wurden
über die mittlere Entfernung der Bäume die Stammzahl und mittlere Bestandeskreisfläche
sowie für jede Art der Anteil am Bestand, die Grundfläche je Hektar und die Frequenz (gibt
an in wieviel Prozent der Subplots die Art vorkommt) ermittelt (Mitchell 2001). Die Wich-
tigkeit einer Gehölzart ist die Summe der Anteile am Bestand und der Bestandeskreisfläche
sowie der relativen Frequenz, und kann dadurch Werte zwischen 0 und 300 annehmen. Als
Beispiel sind in Tabelle 3.2 die ermittelten Werte für die Aufnahme K17 dargestellt.
Abb.3.2: Anlage der Vegetationsaufnahmen mit Bodenschurf (B) südl. des Zentrums. I-V sind die einzelnen 25 m² Subplots im Plot von 484 m².
Abb.3.3: Aufnahmeanordnung der PCQ-Methode. Die Kreise stellen Bäume dar, die schmalen Striche zwischen Zent-rum und Baum die Entfernungen. Das Zentrum ist mit dem Mittelpunkt der jeweiligen Vegetationsaufnahme identisch.
Nr. Subplot Quadrant Art bzw. Gattung
Entfernung [m]
Umfang [cm]
Durchmesser [cm]
Grundfläche [cm²]
K17 I NE Prunus divaricata 2,5 19 6 29 K17 I SE Robinia 2,0 20 6 32 K17 I SW Crataegus 1,7 13 4 13 K17 I NW Quercus 5,7 29 9 67 K17 II NE Fraxinus 1,6 64 20 326 K17 II SE Ulmus 4,5 37 12 109 K17 II SW Quercus 4,4 60 19 286 K17 II NW Ulmus 1,0 112 36 998 K17 III NE Crataegus 5,7 74 24 436 K17 III SE Quercus 3,2 200 64 3183 K17 III SW Crataegus 6,0 15 5 18 K17 III NW Quercus 5,3 32 10 81 K17 IV NE Populus x canescens 3,5 50 16 199 K17 IV SE Crataegus 2,8 18 6 26 K17 IV SW Crataegus 0,5 30 10 72 K17 IV NW Crataegus 2,4 12 4 11 K17 V NE Quercus 1,0 60 19 286 K17 V SE Ulmus 2,4 23 7 42 K17 V SW Quercus 7,2 150 48 1790 K17 V NW Robinia 3,7 12 4 11
Tab.3.1: Wertetabelle für eine PCQ-Aufnahme am Beispiel K 17.
Methoden
11
3.3.5 Weitere dendrologische Parameter Baumhöhe:
Für jeden mit der PCQ-Methode eingemessenen Baum wurde die Höhe geschätzt. Zum Ab-
gleich der Schätzwerte wurden ausgewählte Bäume mittels BLUME-LEISS Höhenmesser noch
vor der Belaubung vermessen, um große Fehlerabweichungen (Prodan 1951; Kramer 1988)
zu vermeiden. Die Unterschiede zwischen Schätzung und Messung lagen zwischen 0 % und
15 % bei insgesamt 30 Proben. Dennoch muss gerade bei hohen Bäumen von einem Schätz-
fehler bis zu 20 % ausgegangen werden.
Alter:
Um das Alter der Pappeln und Eichen annähernd ermitteln zu können, wurden auf dem
direkten Zusammenhang zwischen Durchmesser und Alter basierende Wachstumskurven
erstellt. Dafür wurden alle auffindbaren und noch gut erhaltenen, zumeist von Holzdieben
hinterlassenen Stümpfe zwischen 30 und 40 cm Höhe einbezogen. Aller fünf Jahresringe
wurde der Durchmesser und das Alter notiert. Mit dem Programm EXCEL wurden dann per
Trendlinie Wachstumskurven modelliert, die zur Altersbestimmung der per PCQ-Methode
aufgenommen Bäume wie folgt modifiziert werden müssen:
Die Messhöhendifferenz zwischen Stubben und Brusthöhe ist das erste Problem. Hier muss
die Zeit zur Wachstumsfunktion addiert werden, welche die Bäume brauchen um von 0,3
auf 1,3 Meter zu wachsen. Dieses Wachstum unterliegt starken Schwankungen und wird für
die betrachteten Arten für diese Wuchsregionen nicht in der Literatur angegeben. Deshalb
wird im folgenden einheitlich ein Alterskorrekturfaktor von fünf Jahren verwendet.
Zweitens geht die Wachstumskurve vom Durchmesser ohne Rinde aus. Der mit Rinde ge-
messene Durchmesser ist somit durch einen Rindenkorrekturfaktor zu bereinigen. Da der
Rindenanteil sehr stark variiert (Robertson 1993), wird laut Holzmessanweisung (Prodan
1951) einheitlich bei glattrindigen Arten von 10 % (Quercus) und bei sehr grobrindigen Ar-
ten von 15 % (Populus) ausgegangen.
Bestand Crataegus Quercus Prunus
divaricata Fraxinus Robinia Populus x
canescens Ulmus
Mittlere Entfernung [m] 3,36
Anzahl 6 6 1 1 2 1 3
Anteil am Bestand [%] 100 30 30 5 5 10 5 15
Anzahl je Hektar 888 267 267 44 44 89 44 133
Summe der Grundflächen [cm²] 576 5695 29 326 43 199 11
Mittlere Grundfläche [cm²] 96 949 29 326 22 199 383
Grundfläche je Hektar [m²/ha] 35,6 2,6 25,3 0,1 1,4 0,2 0,9 5,1
Anteil an Bestandeskreisfläche [%] 100 7 71 0,4 4 1 3 14
Absolute Frequenz [%] 280 60 80 20 20 40 20 40
Relative Frequenz [%] 100 21 29 7 7 14 7 14
Wichtigkeit (I) 300 59 130 13 16 25 15 44
Tab.3.2: Kennwerte für den Bestand und die Baumarten der Aufnahme K 17. Die grauhinterlegten Werte ergeben als Summe in jeder Spalte die Wichtigkeit.
Methoden
12
3.3.6 Datenverarbeitung Nach Beendigung der Feldarbeiten lagen nun Daten zur Vegetationszusammensetzung,
Bestandesstruktur, Nutzungsgrad und Bodenprofilbeschreibungen vor. Mit dem Programm
EXCEL wurden die Vegetationsaufnahmen nach Dierschke (1994) und Koska et al. (2001) in
Vegetationstypen gegliedert (Anh.8 und 9), welche in Übersichtstabellen mit Stetigkeitsklas-
sen nach Dierschke (1994) zusammengefasst wurden. Mit einer Korrespondenzanalyse
(DCA) im Programm PCORD wurde das Indikationsvermögen der vorher ausgegliederten
soziologisch-ökologischen Artengruppen bezüglich abiotischer Standortparameter über-
prüft. Zur Bestandescharakterisierung wurden alle PCQ-Messungen eines Vegetationstyps
jeweils zusammen analysiert (Anh.5). Die Erstellung der Schemata, Karten und Kausalprofi-
le erfolgte mit COREL DRAW 11, POWER POINT und ADOBE PHOTOSHOP. Die Transliteration
in Kyrillischer Schrift vorliegender Bezeichnungen richtet sich nach den Vorgaben der
Encyclopaedia Britannica (1997).
3.4 Einschätzung des Gebietszustandes Während des dreimonatigen Aufenthaltes im Dorf Muganli habe ich sowohl die direkten
Beeinträchtigungen des Schutzgebietes durch die Bevölkerung, als auch die Arbeit der
Schutzgebietsverwaltung erlebt. Gespräche mit Hirten, Schutzgebietswärtern und Bauern
rundeten das Bild ab. Fast täglich begleitete ich die Viehherden ins Naturschutzgebiet und
schätzte für das Gebiet die Besatzstärken. Verwertbare offizielle Erhebungen existieren nicht
und die Angaben der Hirten waren höchst widersprüchlich.
Um Naturschutzkosten für die Verdrängung von Äckern aus dem Schutzgebiet zu ermit-
teln, führte ich eine Vollkostenrechnung am Beispiel eines typischen Maisackers durch.
Bei einigen Fahrten durch das gesamte Gebiet erhielt ich einen Überblick über die Situation.
Um die Schutzwürdigkeit zu untermauern, erfasste ich während der Arbeit alle beobachte-
ten Tierarten. Die Artenlisten mit Angaben zu verschiedenen Gefährdungsindizes sind in
den Anhängen 1 und 2 aufgeführt.
Ergebnisse
13
4 ERGEBNISSE Einleitend wird die naturräumliche Situation der Niederung zwischen Muganli und der Kura
im Überblick beschrieben. Anschließend sollen die Vegetationstypen der Wälder und des
Feuchtgrünlandes mit ihren Standorten vertiefend auf der topischen Ebene dargestellt wer-
den. Auf den Zustand des Schutzgebietes und den Nutzungsdruck durch die Anlieger wird
am Ende eingegangen.
4.1 Überblick über die Terrassenniveaus Die Niederung besteht im Untersuchungsgebiet aus der eigentlichen Aue und vier höherge-
legenen Flussterrassen (Abb.4.1). Das Dorf liegt dabei auf der 4. Terrasse ca. 8 m über dem
Fluss. Direkt an die Streusiedlung mit Äckern und Obstgärten schließen sich Eichen-Hude-
wälder und Robinienplantagen an, in denen Jungvieh und Geflügel weiden. Hier liegen 3 m
mächtige schluffige Tone über Terrassenschottern. Diese Schichten werden durch tiefe Grä-
ben angeschnitten, in denen das Grundwasser 3,5 m unter Flur strömt. An einer 3,4 m hohen
Böschung geht der Hudewald in das Feuchtgrünland der 3. Terrasse über. Am Böschungsfuß
treten Quellen zutage. Regen- und Quellwasser sammeln sich in einem Netz aus Gräben,
Tümpeln und Schlenken, die in ein Moor mit Cladium- und Phragmites-Röhrichten münden.
Humusreiche Gleye und Haftpseudogleye dominieren die höher gelegenen Bereiche dieser
Terrasse, auf der Baumstümpfe von gerodeten Eichen-Ulmenwäldern zeugen. Durch andau-
ernde Entwässerungen über Gräben wird der Wasserhaushalt verändert und erste Oberflä-
chenversalzungen treten auf.
Abb.4.1: Kausalprofil durch das Untersuchungsgebiet zwischen Muganli und der Kura
Talboden 1. Terrasse
2. Terrasse
3. Terrasse
4. Terrasse
Terrassenniveau
0,5 2 2,8 3,6 4,6 8 Höhe über Mit-
telwasser [ca. in m]
Schotterbänke Tamarixgebüsch
Auwald Wald-Offenland Mosaik
Feuchtgrünland und Moore
Eichen-Hudewald Vegetation
Überflutung Grundwasser Infiltration Wasserregime Rambla Vega Gley / Haftpseudogley Tschernosem Bodentyp
Ergebnisse
14
Die beiden unteren Terrassen weisen ein Mosaik aus trockenen Wiesen, sumpfigen Quellstel-
len sowie eutrophen Eichenwäldern und Gebüschen auf. Obwohl täglich durch Büffel und
Kühe beweidet, gelingt es Gebüschen aus Crataegus rhipidophylla und Smilax excelsa sich aus-
zubreiten (Abb.4.2). Plantagen aus Populus x canadensis sind dort hingegen abgestorben. Zwei
Bäche drainieren die quelligen Flächen, so dass der Grundwasserstand stellenweise auf 1,2 m
unter Flur absinkt. Prägend sind dennoch humose Gleye und Haftpseudogleye.
Zwischen den Terrassen und dem jenseitigen Hochufer liegt der knapp 3 km breite Talboden
mit der Aue (Abb.4.3), welche durch periodische Überschwemmungen mit Ablagerung von
Sedimenten aller Korngrößen geprägt ist. Im verwilderten Flusslauf mit Schotterbänken do-
minieren Tamarix-Arten und Populus nigra. Die höhergelegenen, älteren Auwälder stocken
auf kiesunterlagerten Schluffen, wo die Graupappel (Populus x canescens) auf den grundwas-
sernahen Vega-Gleyen wächst. Noch höhere Stellen tragen Wälder aus Quercus robur, Cratae-
gus und Ulmus minor auf kalkreichen Vegaböden. Dazwischen liegen von Gebüschen be-
grenzte Blößen mit thermophilen Rasen. Auch die Auwälder dienen als Weidegründe für die
Viehherden der Dörfer.
Abb.4.2: Wald-Offenland Mosaik mit Beweidung auf der 1. Terrasse. Die Sträucher sind Cratae-gus rhipidophylla. Horste von Iris carthaliniae werden nicht gefressen. (Mai 2005)
Abb.4.3: Auwald und Tamarix-Inseln bei Überflu-tung. Blick von Süden in Richtung des Ortes Garayazi (Mai 2005)
Ergebnisse
15
4.2 Feuchtgrünland auf der 1. bis 3. Terrasse
4.2.1 Übersicht Große Teile der Niederung im Zapovednik Garayazi sind heute Wiesen und Weiden für die
großen Viehbestände der umliegenden Dörfer (Abb.4.4). Im Gegensatz zur angrenzenden
Steppe werden diese Gebiete zusätzlich vom Grundwasser gespeist, und weisen somit eine
ausgeglichenere Wasserversorgung auf. Zudem hat der anstehende carbonatreiche Ton ein
hohes Wasserhaltevermögen. Eine direkte Verbindung zum Überflutungsregime der Aue
existiert indes nicht.
Abb.4.5: Schematische Darstellung der Vegetations- und Bodentypen des Feuchtgrünlandes einschließlich des Cladium-Riedes in Abhängigkeit vom Substrat und Wasserstand. (Die Scorzonera-Wiese und das Cladium-Ried kommen nur auf der 3. Terrasse vor.)
Abb.4.4: Blick über das Feuchtgrünland mit weidenden Wasserbüffeln.
Im Hintergrund Ausläufer des Kleinen Kaukasus (April 2005)
Moor Schlenken Tümpel Weide Graben Wiese Graben Weide Geländetyp
Cla
diu
m Rie
d
Nas
turt
ium
C
atab
rosa
Rie
d
Alis
ma
Cat
abro
a Rie
d
Cat
abro
sa
Sch
lam
mflur
Zan
nic
hel
lia
Tau
chflur
Car
ex o
trubae
Ras
en
Nas
turt
ium
Spar
gan
ium
Rie
d
Sco
rzoner
a W
ie-
se
Nas
turt
ium
Spar
gan
ium
Rie
d
Convo
lvulu
s Ras
en
Vegetationstyp
Kal
k-N
ieder
moor
Gyt
tja
(z
.T.
Nas
sgle
y)
Nas
sgle
y
Gyt
tja
Hum
us
Gle
y -
Haf
t -P
seudogle
y
Hum
us
Gle
y-H
aft-
Pseu
dogle
y
Hum
us
H
aft-
Pseu
dogle
y
Bodentyp
Ergebnisse
16
Neun Vegetationstypen, die in Abb.4.5 schematisch dargestellt sind, wurden im Grünland
und den Kleingewässern ausgegliedert. Der Wasserstand und die Nutzungsintensität sind
die wichtigsten vegetationsbeeinflussenden Faktoren, was auch in der Korrespondenzanalyse
(DCA) (Abb.4.9) deutlich wird.
Im Folgenden schließt der Begriff „Feuchtgrünland“ das ungenutzte Cladium-Ried mit ein.
Auf den trockensten Standorten tritt der Convolvulus-Rasen auf. Der Carex otrubae-Rasen und
die Scorzonera-Wiese liegen näher am Grundwasser, wobei ersterer starker Beweidung unter-
liegt und letztere als mehrschürige Wiese genutzt wird. Am Übergang zu den aquatischen
Standorten findet sich die stark durch Tritt beeinflusste Catabrosa-Schlammflur. Ihr schließen
sich im tieferen Wasser das Alisma Catabrosa- und Nasturtium Catabrosa-Ried an. Moorstand-
orte werden vom Cladium-Ried eingenommen. In Meliorationsgräben wächst das hohe
Nasturtium Sparganium-Ried und in kleinen abgeschlossenen Tümpeln ist die Zannichellia-
Tauchflur zu finden.
4.2.2 Cladium-Ried
Die Cladium-Riede kommen nur in Senkenlagen der 3. Terrasse auf Mooren aus kalkreichen
Krummmoostorfen vor. Eine genaue Abgrenzung der oft vom Mineralboden durchragten
Moorflächen auf einer Fläche von ca. 400 ha war nicht möglich. Unter den Aufnahmeflächen
war das Moor mindestens 60 cm tief. Wie ich es zweimal erlebte, versinken selbst Wasserbüf-
fel darin, und kommen um. Deshalb sind hier die einzigen weitgehend unbeweideten Berei-
che. Dominiert werden die Riede von basenliebenden Arten wie Cladium mariscus, Mentha
longifolia und in der Moosschicht von Drepanocladus aduncus, die typisch für Kalk-
Zwischenmoore sind (Succow 2001). Als weitere Arten treten Phragmites australis, Carex ripa-
ria, Schoenoplectus tabernaemontani, Mentha aquatica sowie Nasturtium officinale als Art quelli-
ger, basenreicher Standorte auf.
Typische Arten: Cladium mariscus Drepanocladus aduncus Mentha longifolia
Kennzeichnende Artengruppen:
1; 4; 6
Standorttyp: Breite Senken (in tiefsten Berei-chen der 3. Terrasse)
Trophiestufe: mesotroph Wasserregime: topogen; z.T. perkolativ Torfart: Krummmoostorf (Hmbd) mit
Schneidenwurzeln, Bodentyp KA5: WRB: Russland:
Kalk-Niedermoor Calcari-Sapric Histosol Peat-soil
Ökologischer Moortyp:
Kalk-Zwischenmoor
Hydrogenetischer Moortyp:
Wahrscheinlich Grundwasser-Versumpfungsmoor, evtl. Durch-strömungsmoor Abb.4.6: Cladium-Ried auf der 3. Terrasse (Mai 2005)
Ergebnisse
17
4.2.3 Nasturtium Sparganium-Ried
In alten Gräben und Schlenken bei Wasserständen um 20 cm kommt dieser Vegetationstyp
vor. Typisch sind eutraphente Arten wie Lemna minor, Typha latifolia und T. angustifolia sowie
Berula erecta. Weniger stetig sind Ricciocarpus natans, Carex distans und Carex acutiformis. Be-
sonders in tiefen Gräben werden grundwasserleitende Schichten angeschnitten. Hier domi-
niert sofort Nasturtium officinale.
4.2.4 Nasturtium Catabrosa-Ried
Das Nasturtium Catabrosa-Ried ähnelt dem vorangegangenen Typ, liegt jedoch in breiteren
Senken und ist damit für weidende Wasserbüffel zugänglich. Dadurch entstehende Trittstö-
rungen ermöglichen die Etablierung von Arten der Schlammfluren so Ranunculus sceleratus,
Catabrosa aquatica und Veronica catenata. Von den Arten der höheren Riede sind vor allem
Sparganium erectum und Schoenoplectus tabernaemontani hochstet vertreten. Letztere bildet aber
nie geschlossene Bestände. Das Substrat ist schluffiger Ton, auf dem sich Nassgleye und sub-
hydrische Gyttjaböden entwickelten. Durch ständige Zufuhr von Quellwasser ist die Gefahr
der sommerlichen Austrocknung gering.
Typische Arten: Nasturtium officinale Ricciocarpus natans Sparganium erectum Typha spp.
Kennzeichnende Artengruppen:
2; 3; 4; 6
Standorttyp: Gräben, schmale Senken mit steilem Ufer
Trophiestufe: eutroph Wasserregime: topogen Bodentyp KA5: WRB: Russland:
Subhydrischer Rohboden nach Grabenaushub oder Gyttja -/- -/-
Abb.4.7: Nasturtium Sparganium-Ried im Vorder-grund mit Typha und Phragmites. Dahinter Carex otrubae-Rasen. (Juni 2005)
Typische Arten: Nasturtium officinale Schoenoplectus tabernaemontani Sparganium erectum Catabrosa aquatica Ranunculus sceleratus
Kennzeichnende Artengruppen:
3; 4; 5; 6
Standorttyp: Flache, breite Senken Trophiestufe: eutroph Wasserregime: überwiegend perkolativ Besonderheiten: Wird von Wasserbüffeln
beweidet Bodentyp KA5: WRB: Russland:
Nassgley; Gyttja Gleysol Meadow-Soil
Abb.4.8: Nasturtium Catabrosa-Ried auf der 2. Terrasse. Weißblühend Nasturtium officinale entlang des austretenden Quellbaches, daneben Sparganium erectum. (April 2005)
Ergebnisse
18
Vegetationstyp Nr.: 1 2 3 4 5 6 7 8
Substrat Oberboden Hn Hn,t t t t t t u;l;t Nutzungsgrad 1 1.5 2 2.5 3 3 1.5 3 Nutzungstyp S S;G S S S W M W mittlere Krauthöhe [m] 1.5 0.9 0.9 0.5 0.3 0.2 0.4 0.2 mittlere Deckung [%] 80 70 80 60 40 80 90 70 mittlerer Wasserstand [cm] 0 20 25 15 5 -30 -40 -100 Anzahl der Aufnahmen 3 11 6 8 7 8 4 3 Artengruppe 1
Cladium mariscus V Calystegia sepium IV Mentha longifolia IV Lysimachia vulgaris IV Drepanocladus aduncus II AG 2
Carex acutiformis II II I Ricciocarpus natans II Carex distans II II Lythrum salicaria II I AG 3
Lemna minor II IV IV I Berula erecta III II Typha angustifolia III III Typha latifolia II IV Lycopus exaltatus I III AG 4
Nasturtium officinale V V V IV Schoenoplectus tabernaemontani V IV V III I Phragmites australis V III I I II Carex riparia V II III IV Chara sp. IV II I II I Sparganium erectum II V V IV Mentha aquatica II II II Alisma plantago-aquatica + II IV AG 5
Ranunculus sceleratus V V V I Catabrosa aquatica II V V V Veronica catenata + V IV V Ranunculus chius II I I Ranunculus trichophyllus I IV II Iris pseudacorus II AG 6
Juncus articulatus IV II IV IV IV V Agrostis sp. II I III IV II IV AG 7
Carex otrubae II I II III V Carex duriuscula IV Plantago major II II IV II Puccinellia distans III II AG 8
Juncus compressus II V V Mentha suaveolens II II II IV Carex disticha + II I IV AG 9
Lavathera thuringiaca V Scorzonera parviflora V Tragopogon dubius V Festuca pratensis V II Cichorium intybus IV Dactylorrhiza incarnata II I IV Equisetum ramosissimum IV II Ranunculus acris III AG 10
Festuca arundinacea I I III V V IV Carex diluta V V V Taraxacum officinale III V V V Lotus tenuis IV V III Hordeum leporinum III IV Iris carthaliniae III V AG 11
Cerastium semidecandrum V Convolvulus lineatus V Poa angustifolia V Ranunculus bulbosus V Eryngium campestre IV Centaurea calcitrapa IV Potentilla recta IV Galium parisiense IV Sherardia arvensis IV
Tab. 4.1: Übersichtstabelle der Vegetationstypen des Feuchtgrünlandes inklusive des Cladium-Riedes.
Legende zur Tabelle: Vegetationstypen: 1 Cladium-Ried 2 Nasturtium Sparganium-Ried 3 Nasturtium Catabrosa-Ried 4 Alisma Catabrosa-Ried 5 Catabrosa-Schlammflur 6 Carex otrubae-Rasen 7 Scorzonera-Wiese 8 Convolvulus-Rasen Substrat: Hn Torf t Ton u Schluff l Lehm Nutzungstyp: S Schlenke G Graben W Weide M Mähwiese Mittelwerte gerundet Größe der Aufnahmeflächen: 25 m²
Ergebnisse
19
Abb.4.9: DCA der Arten des Feuchtgrünlandes mit farbig unterstrichenen Artengruppen (siehe Tab. 4.1). Hiermit wird der Wasserstand als prägender Standortfaktor bestätigt. Der Nutzungsgrad hängt vom Wasserstand, also von der Be-gehbarkeit der Flächen durch Weidevieh ab. Eine Ausnahme bildet die Scorzonera-Wiese mit AG 9, die nicht bewei-det wird.
3
6
9
2
5
8
11
Art
engru
ppen
1
4
7
10
Ergebnisse
20
4.2.5 Tümpel mit Zannichellia-Tauchflur
Eine Eigentümlichkeit stellen die Tümpel im Carex otrubae-Rasen dar. Sie sind abflusslos, bis
40 cm tief, haben steile Ufer und können kreisrund bis langgestreckt sein. In ihnen sammelt
sich das Oberflächenwasser der umgebenden tonigen Standorte und trägt Nährstoffe ein.
Puccinellia distans weist an den Rändern auf hohe Elektrolytgehalte hin. Bis zum völligen Aus-
trocknen im Sommer werden die Tümpel von den Wasserbüffeln als Abkühlbecken genutzt.
Im Anh. 7 sind alle Aufnahmen der Tümpel aufgelistet, und es zeigt sich eine Dominanz des
eutraphenten Teichfadens (Zannichellia palustris) gemeinsam mit Ranunculus trichophyllus und
Chara-Arten. Vereinzelt kann Carex disticha in die Tümpel vordringen. Arten der Röhrichte
halten sich nur in Kümmerformen.
4.2.6 Alisma Catabrosa-Ried
Oberhalb der Nasturtium-Riede wächst in flachen schmalen Schlenken das Alisma Catabrosa-
Ried. Hier steht das Wasser im Frühjahr nur 10 bis 20 cm über Flur und schützt die Vegetati-
on nicht mehr vor Beweidung. Ein Austrocknen der Nassgleye im Hochsommer ist wahr-
scheinlich. Dadurch sinkt die Gesamtbedeckung unter 80 % und Typha, Lemna minor und Be-
rula erecta werden verdrängt. Dafür erreichen die Arten der Schlammfluren (AG 4) sowie die
Typische Arten:
Zannichellia palustris Ranunculus trichophyllus Chara sp.
Standorttyp: Runde bis gestreckte Mulden mit steilen Ufern
Trophiestufe: eu- bis polytroph Wasserregime: geogen, Stauwasser Besonderheiten: Speisung durch Oberflächen-
und z.T. Quelllwasser Leichte Versalzung
Bodentyp: Gyttja
Abb.4.10: Langgestreckter Tümpel im Blühaspekt von Ranunculus trichophyllus umgeben vom Carex otrubae-Rasen. (April 2005)
Typische Arten: Alisma plantago aquatica Carex riparia Catabrosa aquatica Ranunculus trichophyllus
Kennzeichnende Artengruppen:
4;5;6
Standorttyp: schmale flache Senken mit flachen Rändern
Trophiestufe: eutroph Wasserregime: perkolativ, wechselnass Besonderheiten: stark trittgestört
Bodentyp KA5: WRB: Russland:
Nassgley, z.T Gyttja Gleysol Meadow-Soil
Abb.4.11: Das Quellgras (Catabrosa aquatica) als typische Art quelliger und trittgestörter Flächen (Mai 2005)
Ergebnisse
21
auf allen nassen und feuchten Standorten anzutreffenden Juncus articulatus und Agrostis sp.
höhere Deckungsgrade. Carex riparia, Sparganium erectum und Alisma plantago aquatica schei-
nen der Tritt- und Verbissbelastung zu widerstehen.
4.2.7 Catabrosa-Schlammflur
Der Ursprung der Schlenken liegt in einem in Abb.4.13 dargestellten, netzartigen System aus
flachen Senken auf der 3. Terrasse. Hier sammeln sich abfließendes Regenwasser und austre-
tendes Quellwasser. Dadurch wird der tonige Boden stark aufgeweicht und durch tägliche
Viehtrift entstehen Schlammflächen. Nur noch die einjährigen Arten der Schlammfluren und
Juncus articulatus können sich hier in artenarmen, lichten und niedrigen Beständen halten.
Mitte Juni etablierte sich hier Cyperus flavescens, welches jedoch nicht mehr in die Vegetati-
onsaufnahmen einbezogen wurde.
Typische Arten: Ranunculus sceleratus Veronica catenata Catabrosa aquatica Juncus articulatus
Kennzeichnende Artengruppen:
5; 6
Standorttyp: sehr flache Senken Trophiestufe: eu- bis polytroph Wasserregime: geogen - wechselnass Besonderheiten: Gesamtdeckung 30-40%
Stark trittgestört Bodentyp KA5: WRB: Russland:
Nassgley Gleysol Meadow - Soil
Abb.4.12: Veronica catenata in der Catabrosa-Schlammflur (Mai 2005)
Abb.4.13: Karte (100x140 m) des Schlen-kensystems im Quellbereich der 3. Terrasse
Ergebnisse
22
4.2.8 Carex otrubae-Rasen
Auf den terrestrischen Standorten sind die Grundwassertiefe und die Beweidungsintensität
besonders vegetationsprägend. Durch tägliche Beweidung (Nutzungsgrad 3) entstehen nied-
rige Rasen mit beweidungsresistenten Arten wie Juncus articulatus und Agrostis sp.. Die kenn-
zeichnenden Arten sind wie Carex otrubae, C. duriuscula, Festuca arundinacea und Puccinellia
distans salztolerant. Das Grundwasser steht ca. 30 cm unter Flur und steigt in den Kapillaren
der tonigen carbonatreichen Humus-Gley-Haftpseudogleye bis an die Oberfläche. Aufgrund
starker Verdunstung kommt es dort zu Salzanreicherungen (Abb.5.5). Dieser Prozess wird
sich weiter verstärken, da die letzten verbliebenen Bäume der ehemals bewaldeten Standorte
absterben, und durch höhere Sonneneinstrahlung die Verdunstung zunimmt.
4.2.9 Scorzonera-Wiese Auf den gleichen Standorten wie der Carex otrubae-Rasen kann sich durch Fernhalten der
Weidetiere die Scorzonera-Wiese herausbilden. Diese grundwassernahen Bereiche (ca. 40 cm
unter Flur) sind durch breite tiefe Gräben von den Weiden abgetrennt, und dienen als mehr-
schürige Heuwiesen. Die erste Mahd findet Anfang Juni statt. Viele höherwüchsige Arten
kommen nur hier vor. Zu ihnen zählen Lavathera thuringiaca, Scorzonera parviflora, Dactylorrhi-
za incarnata sowie Cichorium intybus.
Substrat: Ton Typische Arten: Juncus articulatus Carex otrubae Carex duriuscula Juncus compressus Festuca arundinacea
Bodentyp KA5: WRB: Russland:
Humus-Gley Haftpseudogley Gleysol Meadow-Soil
Kennzeichnende Arten-gruppen:
6; 7; 8; 10 Weitere Bodenparameter:
Carbonatreich (C 3-4) Humose Horizonte über 40 cm mächtig
Trophiestufe: eutroph Wasserregime: Grund-/ Stauwasser
Standorttyp: Ebenen (ca. 30 cm über Grund-wasserspiegel)
Besonderheiten: tägliche starke Beweidung Krauthöhe unter 20 cm
Abb.4.14: links: Carex otrubae –Rasen am Standort 3. Im Bild die letzte absterbende Eiche auf dem Feuchtgrünland. (April 2005) rechts: Profil Nr. 3. Humus-Gley Haftpseudogley auf schluffigen über sandigen Ton. (4.4.2005)
Ah Ah-Sg Ah-Go-Sg
Ergebnisse
23
4.2.10 Convolvulus-Rasen Standorte mit Grundwasserständen um einen Meter trocknen im Sommer an der Oberfläche
stark aus. Der Boden ist sehr carbonatreich, besteht aus schluffigen Tonen und hat einen bis
zu 40 cm mächtigen Ah-Horizont. Auf diesen stark beweideten Flächen wachsen lichte kurze
Trockenrasen mit nur einzelnen Horsten aus Iris carthaliniae, die nicht abgefressen werden.
Die Artengarnitur unterscheidet sich erheblich von der feuchterer Standorte.
Besonders niedrige Arten mit Schutzmechanismen gegen Beweidung, wie stachligen Blättern,
(Eryngium campestre, Centaurea calcitrapa) und Therophyten (Sherardia arvensis, Galium parisien-
se) treten auf. Weitere typische Arten sind Convolvulus lineatus, Ranunculus bulbosus und Po-
tentilla recta. Im Schutze der Iris-Horste können sich auch noch Festuca arundinacea und Carex
diluta halten.
Typische Arten:
Scorzonera parviflora Juncus compressus Lavathera thuringiaca Tragopogon dubius
Kennzeichnende Artengruppen:
8; 9; 10
Standorttyp: Ebenen, von Gräben umgeben Trophiestufe: eutroph Wasserregime: Grund-/ Staunässe Besonderheiten: Unbeweidet, mehrschürig
Standorte wie Carex otrubae-Rasen nur Grundwasser bei 40 cm unter Flur Hoher Salzgehalt
Bodentyp KA5: WRB: Russland:
Humus–Gley–Haftpseudogley Gleysol Meadow-Soil
Abb.4.15: Scorzonera-Wiese durch Gräben abgegrenzt. Im Vordergrund blühende Dactylorrhiza in-carnata und Ranunculus acris (Mai 2005)
Abb.4.16: links: Convolvulus lineatus als typische Rasenart (Mai 2005) rechts: Profil Nr. 30. Gley-Haftpseudogley auf stark schluffigen Ton der 1. Terrasse - einmal gepflügt (15.4.2005)
Standorttyp: Ebenen und flache Hänge mindestens 60 cm über Grundwasserspiegel
Typische Arten: Iris carthaliniae Convolvulus lineatus Poa angustifolia Ranunculus bulbosus Substrat: Stark schluffiger Ton
Kennzeichnende Artengruppen:
10; 11 Bodentyp KA5: WRB: Russland:
Gley - Haftpseudogley Gleysol Meadow - Soil
Trophiestufe: mesotroph Wasserregime: Infiltration, Haftnässe
Besonderheiten: kurzrasig Horste von Iris carthaliniae als Weideunkraut
Weitere Bodenparameter: Carbonatreich (C 4)
Axh Axh-Sg Sg Sg-Go/Gr
Ergebnisse
24
4.3 Wälder mit Degradationsstadien Trotz des hohen Nutzungsdruckes durch die umliegenden Dorfgemeinschaften blieben Au–
und Niederungswälder im Schutzgebiet Garayazi erhalten, doch degradierten die Bestände
durch Beweidung und Holzentnahme, so dass ein Mosaik aus Lichtungen, Gebüschen und
Hudewäldern entstand. Zu Beginn dieses Kapitels werden die Ergebnisse der Altersbestim-
mung für Pappeln und Eichen (vgl. Kap. 3.3.5) vorgestellt, und danach die einzelnen Vegeta-
tionstypen beschrieben.
4.3.1 Altersbestimmung der Pappeln und Eichen An auffindbaren abgesägten Baumstümpfen wurden 196 Alters- und Durchmesserwerte der
Arten Populus nigra, Populus x canescens und Quercus robur ausgezählt. Den Altersangaben in
den Bestandsbeschreibungen liegen die hier errechneten Wachstumskurven zugrunde.
Quercus robur: Aufgrund der hohen Witterungsbeständigkeit von Eichenholz konnten auch ältere Baum-
stümpfe ausgezählt werden. Abb.4.17 zeigt die Alterswerte mit der berechneten nichtmodifi-
zierten Wachstumskurve. Der älteste Baumstumpf hatte ein Alter von 205 Jahren bei einem
Durchmesser von 1,48 Metern. Für alle Bäume ergibt sich ein mittlerer Durchmesserzuwachs
von einem Zentimeter pro Jahr, welcher an der unteren Grenze der von Prilipko (1975) für
Quercus robur ermittelten Spanne von 1,0 bis 2,8 cm/a liegt, aber noch dreimal höher als in
mitteleuropäischen Eichenforsten der ersten Ertragsklasse ist (Schober 1995).
Am Beispiel von Quercus wird die Ermittlung der modifizierten Wachstumsgleichung erläu-
tert. Ausgangspunkt ist die per Computer berechnete Regressionsgleichung:
A = 0,0042d2 + 0,67d A... Alter in Jahren [a]; d... Durchmesser [cm]
Der Rindenkorrekturfaktor (k = 0,90) wird mit dem Durchmesser multipliziert, sowie die Hö-
hen- bzw. Alterskorrekturzahl (h = 5) als Konstante der Gleichung hinzugefügt. Es entsteht
die für die Altersbestimmung genutzte modifizierte Wachstumsgleichung:
A = 0,003402d² + 0,5427d + 5
Quercus robur
R2 = 0,9679n = 132
0
50
100
150
200
250
0 40 80 120 160Durchmesser d [cm]
Alter
A [
a]
Art: Quercus robur Regressionsgleichung: A = 0,0042d2 + 0,67d Rindenkorrekturfaktor: k = 0,90 Höhen- bzw. Alterskor-rekturzahl:
h = 5
Modifizierte Wachs-tumsgleichung:
A = 0,003402d²+0,5427d+5
Mittlerer Durchschnitts-zuwachs:
Zd = 1,01 cm/a
Abb.4.17: Ausgezählte Alters- und Durchmesserwerte für Quercus robur und nichtmodifizierte Wachstums-kurve als Trendlinie
Ergebnisse
25
Populus nigra und P. x canescens:
Durch die geringe Beständigkeit des Pappelholzes und oft auftretende Kernfäule konnten nur
15 bzw. 49 Datensätze aufgenommen werden (Abb.4.18 und 4.19).
Für P. x canescens kommt hinzu, dass bevorzugt unterdrückte Bäume absterben und abgesägt
werden. Die unterschiedlichen Wuchsbedingungen führen auch zu einer starken Streuung
der Werte und verringern die Genauigkeit der Wachstumsgleichung. So müssten für herr-
schende Bäume höhere Zuwächse und damit ein geringeres Alter angenommen werden.
Aufgrund fehlender besserer Daten wird unter Kenntnis dieser Einschränkungen mit der
errechneten Gleichung gearbeitet. Die mittleren Durchmesserzuwächse sind für Populus nigra
mit 1,63 cm/a und für Populus x canescens mit 1,90 cm/a hoch, aber für Pappeln, als schnell-
wachsende Pioniergehölze typisch (Schober 1995). Aliyew & Chalilov (1976) ermittelten im
Gebiet auch Zuwächse um 2 cm/a und widersprechen damit Prilipko (1954) welcher nur von
1,04 cm/a ausgeht.
Art: Populus nigra Regressionsgleichung: A = 0,0044d2 + 0,4059d Rindenkorrekturfaktor: k = 0,85 Höhen- bzw. Alters-korrekturzahl:
h = 5
Modifizierte Wachs-tumsgleichung:
A = 0,003179d²+0,345015d+5
Mittlerer Durch-schnittszuwachs:
Zd = 1,63 cm/a
Art: Populus x canescens Regressionsgleichung: A = 1,1117d0,8243 Rindenkorrekturfaktor: k = 0,85 Höhen- bzw. Alters-korrekturzahl:
h = 5
Modifizierte Wachs-tumsgleichung:
A = 0,972316d0,8243 + 5
Mittlerer Durch-schnittszuwachs:
Zd = 1,90 cm/a
Populus x canescens
R2 = 0,7878n = 49
0
20
40
60
80
100
0 40 80 120 160Durchmesser d [cm]
Alter
A [
a]
Abb.4.19: Ausgezählte Alters- und Durchmesserwerte für Populus x canescens und nichtmodifizierte Wachstumskurve als Trendlinie.
Abb.4.18: Ausgezählte Alters- und Durchmesserwerte für Populus nigra und nichtmodifizierte Wachs-tumskurve als Trendlinie
Populus nigra
R2 = 0,845n = 15
010203040506070
0 20 40 60 80 100
Durchmesser d [cm]
Alter
A [
a]
Ergebnisse
26
4.3.2 Die Wälder und ihre Degradationsstadien im Überblick Die Wälder im Schutzgebiet lassen sich nach zwei Gesichtspunkten gliedern: Erstens kann
man zwischen Niederungswäldern auf den Terrassen und Auwäldern auf dem Talboden
unterscheiden. Zweitens ist aber eine klare Dreiteilung in Eichen-Ulmenwälder, Graupap-
pelwälder und Weichholzwälder anhand der Gehölzzusammensetzung möglich (Tab.4.2).
Gemäß der Abfolge in Tab.4.2 werden die Wälder nun unter Zuhilfenahme von Ordinations-
diagrammen und Übersichtstabellen mit den jeweils relevanten Artengruppen beschrieben.
Letztere sind Ausschnitte aus der Vegetationstabelle für alle Wälder in Anh. 9.
4.3.3 Eichen-Ulmenwälder Es ist anzunehmen, das alle vier Terrassen ursprünglich von Eichen-Ulmenwäldern bestockt
waren. Neben Solitärbäumen in der Feldflur existieren noch sehr lichte Quercus-Wälder auf
der trockenen 4. Terrasse am Südrand der Dörfer. Hauptsächlich im Bereich der 1. bis
3. Terrasse wächst der Carduus-Wald auf frischen bis feuchten Standorten. Auf hohen Kies-
bänken in der Aue (Abb.4.30) ist der Origanum-Wald und seine degradierte Form, die Verbas-
cum-Lichtung mit wärmeliebenden Gebüschen anzutreffen. Der Carduus- und der Origanum-
Wald weisen ein feines Mosaik aus dichteren Baumgruppen, kleinen Gebüschinseln, Säumen
und Blößen auf.
4.3.3.1 Quercus-Wald Einer lichten Parklandschaft gleichend, schließt der Quercus-Wald unmittelbar an die Sied-
lungen an. Grundwasser in 3,5 m Tiefe, im Ton aufsteigendes Kapillarwasser und Nieder-
schläge, vor allem zu Beginn der Vegetationsperiode, gewährleisten die Existenz dieser Wäl-
der (Gulisaschvili et al. 1976). Die tonigen, bei Trockenheit stellenweise aufreißenden Böden
haben sich zu carbonatreichen Schwarzerden mit 40 cm mächtigen Humushorizonten ausge-
bildet (vgl. Urushadze 2005).
Ständige Beweidung und das Abschlagen von Sträuchern ließen drei Vegetationsschichten
entstehen:
1. Die lichte, mit 61 Bäumen je ha geringbestockte Baumschicht, weist eine Dominanz 40 bis
90 jähriger Eichen auf. Wildobstarten (Pyrus, Crataegus) sowie einzelne gepflanzte Robi-
1. Eichen-Ulmenwälder 2. Graupappelwälder 3. Weichholzwälder
Vegetationstypen: Quercus-Wald
Carduus-Wald
Origanum-Wald
Verbascum-Lichtung
Vincetoxicum-Wald
Tilia-Wald
Periploca-Lichtung
Alliaria-Wald
Tamarix-Weichholzaue
Populus-Weichholzaue
Alnus-Bachsaum
Tab. 4.2: Vegetationstypen der Wälder und ihrer Degradationsstadien
Ergebnisse
27
nien sind eingestreut (Abb.4.21). Alle Bäume werden für die Feuerholznutzung geschnei-
telt.
2. Die niedrige, inselartige, stark verbissene und trockenheitsresistente Strauchschicht be-
steht aus Paliurus spina-christi und Rhamnus pallasii.
3. Der kurze Rasen besteht aus annuellen und verbissresistenten Arten wie Scleranthus an-
nuus, Geranium pusillum, Alhagi pseudalhagi und Eremostachys iberica. Arten, die sich in den
anderen Waldtypen voll entwickeln, bilden hier nur flache Rosetten aus. Dazu zählen u.a.:
Eryngium campestre, Centaurea calcitrapa und Ranunculus bulbosus.
73N =
Quercus
Alter
in J
ahre
n
160
140
120
100
80
60
40
20
0
Abb.4.20: links: Quercus-Wald mit weidendem Jungvieh und Geflügel. In der Mitte Crataegus-Strauch von Rhamnus pallasii umgeben. (Mai 2005)
rechts: Profil Nr. 1. Normtschernosem auf schluffigem über sandigem Ton. (2.4.2005)
Axh Axh-lCc lCc
Wichtigkeit (I)
185 10
266
Quercus
Robinia
Pyrus
Crataegus
Stammzahl je ha: 61 Bestandeskreisfläche: 25 m²/ha gemessene Bäume: 80 Mittleres Alter von Quercus robur:
67 Jahre
Abb.4.21: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen des Quercus-Waldes, sowie Darstellung der Altersverteilung von Quercus robur im Boxplot.
Substrat: Schluffiger bis sandiger Ton Typische Arten: Falcaria vulgaris Eremostachys iberica Paliurus spina christi Scleranthus annuus
Bodentyp KA 5: WRB: Russland:
Normtschernosem Chernosem Calcic Chernozems southern
Kennzeichnende Artengruppen:
17-19; 23; 24 Weitere Bodenparameter: carbonatreich, teilweise mit Pseudomycel Humose Horizonte bis 40 cm mächtig Grundwasser bei 3,5 m unter Flur
Standorttyp: Ebenen der 4. Terrasse
Wasserregime: Infiltration
Besonderheiten: Tägliche starke Beweidung Krautschicht als Rasen ausgeprägt Eichen werden geschneitelt Stellenweise Robinienplantagen
Ergebnisse
28
Vegetationstyp Nr.: 1 2 3 4 GW-Tiefe [m] 0,4-2 1,5-2,5 1,5-2 3-3,5 Terrasse 0;1;3 0 0 4 Höhe der Überflutung [cm] 0-20 0-50 20-50 0 Bodenart (0-40 cm) t;u t;u;l;s u;l;G t Bodenart (>40cm) t;l;u u;s;G u;l;G t Mächtigkeit Ah-Horizont [cm] 30 10 8 30 Carbonat (0-40) nach KA4 3 4 4 4 Nutzungsintensität 1,9 1,9 2 3 B1 Höhe [m] 20 20 B1 Deckung [%] 35 30 B2 Höhe [m] 11 9 10 17 B2 Deckung [%] 35 25 5 20 S Höhe [m] 3 3 3 2 S Deckung [%] 30 50 25 10 L Deckung [%] 10 10 1 K Höhe [m] 0.3 0.4 0.3 0.2 K Deckung [%] 50 50 50 70 Anzahl der Aufnahmen 8 8 7 4 AG 13 K Cynoglossum germanicum II K Alliaria petiolata II K Listera ovata I I K Arctium tomentosum II I K Carex melanostachya II I AG 15 K Carduus crispus IV I K Fallopia convolvulus III K Stellaria media IV II K Urtica dioica II K Plantago major IV K Persicaria maculosa II S Celtis sp. II K Silybum marianum II I K Carex diluta II AG 7 S Cornus sanguinea III III S Euonymus europaeus III IV I B2 Crataegus sp. III IV L Smilax excelsa IV V L Periploca graeca IV IV I L Humulus lupulus I L Hedera helix II III B1 Populus x canescens I III AG 8 K Elytrigia repens IV V III K Brachypodium sylvaticum V V K Hedera helix II IV K Gleditsia caspica IV K Galium spurium III II K Prunella vulgaris I II AG 9 K Glechoma hederacea II V K Viola spp. IV V II B2 Ulmus minor II IV I K Physalis algekengi IV II K Geum urbanum V IV K Buglossoides purpurocaeroleum III V K Asperula rivalis II IV K Festuca gigantea III I K Vincetoxicum scandens I II K Agrimonia eupatoria IV V S Frangula alnus I II AG 12 S Prunus spinosa IV IV S Gleditsia caspica II II B1 Quercus robur I II K Smilax excelsa II I K Carex tomentosa I IV K Inula helenium II I K Quercus robur II II II AG 14 K Thalictrum minus II IV I K Cirsium arvensis II I K Silene wallichiana III II K Fragaria viridis II IV II B2 Malus orientalis II I AG 10 B2 Robinia pseudacacia II II III S Ligustrum vulgare II V V S Cornus mas I I I S Robinia pseudacacia III I S Rosa canina II II III S Pyrus sp. II II II AG 20 S Rhamnus cathartica II III III K Euphorbia virgata III IV III K Salvia nemorosa II II V K Geranium dissectum I IV I K Euphorbia helioscopa I V K Ajuga genevensis I II III K Bromus arvensis II II II K Lavathera thuringiaca III IV III AG 17 K Asparagus officinalis II IV II II K Eryngium campestre IV V III V K Potentilla reptans IV I I IV
Fortsetzung 1 2 3 4 AG 19 K Cynodon dactylon II I IV III K Veronica polita III I IV K Achillea micrantha II V IV K Galium parisiense II I I III K Capsella bursa-pastoris II I V K Galium mollugo IV IV II IV K Centaurea calcitrapa II I V K Potentilla recta II IV III II K Medicago lupulina II IV I V S Rhamnus pallasii II II III S Pailurus spina-christi I II III AG 18 K Ranunculus bulbosus V IV II K Trifolium repens III III III K Chenopodium album II I II K Ballota nigra II I II K Trifolium dubium II I IV AG 16 K Origanum vulgare V K Orchis militaris II K Polygala anatolica II K Equisetum variegatum II K Asparagus verticillatus II S Malus orientalis I III K Equisetum ramosissimum I II AG 21 K Verbascum phoeniceum II III K Hypericum perforatum III III K Linum austriacum II III K Medicago minima II V AG 22 K Myagrum perfoliatum III K Daucus carota V K Ranunculus illyricus IV K Bromus commutatus II AG 23 K Erodium cicutarium V IV K Poa bulbosa I IV IV K Arenaria serpyllifolia I II IV K Vulpia ciliata I III AG 24 K Poa annua II III K Scleranthus annuus IV K Alhagi pseudoalhagi III K Eremostachys iberica II K Falcaria vulgaris II IV K Polygonum aviculare II III K Geranium pusillum II V K Cerastium semidecandrum I IV
Tab. 4.3: Übersichtstabelle der Eichen-Ulmenwälder
Legende zur Tabelle: Vegetationstypen: 1 Carduus-Wald 2 Origanum-Wald 3 Verbascum-Lichtung 4 Quercus-Wald Vegetationsschicht: B1 Baumschicht 1 B2 Baumschicht 2 S Strauchschicht L Lianenschicht K Krautschicht Bodenart: t Ton u Schluff l Lehm s Sand G Kies Mittelwerte gerundet Aufnahmeflächen: 484 m² Gehölze 5x25 m² Krautschicht
Ergebnisse
29
Achillea micrantha
Agrimonia
Ajuga genevensis
Alhagi pseudalhagi
Alliaria
Arctium
Arenaria
Asparagus o.
Asparagus v.
Asperula
Astragalus hamosus
Astragalus sp.
Populus can. B1
Robinia B1
Ulmus B2
Quercus B1
Malus B2
Ballota
Brachypodium
Bromus arvensis
Bromus commutatus
Buglossoides
Capsella
Carduus
Carex diluta
Carex mel.
Carex tomentosa
Centaurea
Cerastium semidec.
ChenopodiumCirsiumConium
Vincetoxicum
Cynodon
Cynoglossum
Daucus carota
ElytrigiaEquisetum r.
Equisetum v.
Eremostachys iberica
Erodium
Eryngium
Euphorbia helioscopa
Euphorbia virgata
Falcaria vulgaris
FallopiaFestuca gigantea
Fragaria
Galium mollugo
Galium parisiense
Galium spurium
Geranium dis.
Geranium pussilum
Geum
Glechoma
Hedera
Humulus Hyoscyamus
Hypericum
Inula
Lavathera
Linum
Listera
Medicago lupulina
Medicago minimaMyagrum perfoliatum
Orchis militaris
Origanum
Periploca
Persicaria
Physalis
Plantago major
Poa annua
Poa bulbosa
Polygala anatolica
Polygonum
Potentilla recta
Prunella
Ranunc. bulb.
Ranunculus illyricus
Salvia nemorosa
Scleranthus
Cornus mas S
Cornus sang. S
Euonymus S
Frangula S
Gleditsia SSilene
Silybum
Ligustrum S
Malus S
Smilax L
Smilax K
Pailurus S
Prunus spinosa S
Prunus div. S
Pyrus S
SRhamnus
Rhamnus pallasii S
Robinia SRosa canina S
Stellaria
Thalictrum
Trifolium dubium
Trifolium repens
Urtica
Verbascum phoeniceum
Veronica polita
Viola
Vulpia ciliata
Grundwassertiefe
Aue
Überflutungshöhe
Bodenart Ton
Mächtigkeit Ah-Horizont
Nutzungsgrad
Entfernung vom Dorf
Eichenwald
Achse 1
Achse 2
Artengruppen
13; 15 - Arten des Carduus-Waldes (nitrophil)
7; 8; 9; 12; 14 - Arten der geschlossenen Wälder (Carduus- und Origanum-Wald)
10; 20 - Arten in Aue und der 1.-3. Terrasse
17; 19 - Arten in allen Eichenwaldtypen
18 - Arten nur auf tonigen Böden
16-kennzeichnende Arten des Origanum - Waldes
21 - Arten der Verbascum-Lichtung und des Origa-num-Waldes
22 – kennzeichnende Arten der Verbascum-Lichtung
23 – Arten der Verbascum-Lichtung und des Quercus-Waldes
24 – kennzeichnende Arten des Quercus-Waldes
Abb. 4.22: DCA der Arten der Eichen-Ulmenwälder mit Standortparametern (Bei Bodenart Ton und Lage in der Aue wurde zur Analyse je „1“ oder „0“ zugeordnet). Arten einer Artengruppe sind jeweils farbig unterstrichen.
Achse 2 erklärt hauptsächlich den Gradienten zwischen den tonigen, starkbeweideten dorfnahen Standorten der Terrassen und den schluffig-sandigen, sowie überfluteten Standorten der Aue. Achse 1 scheint den Feuchtegradienten, bzw. die Wasserstufe zu erklären, wonach dem Substrat unter feuchteren Bedingungen eine geringe vegetationsprägende Wirkung zukommt.
Ergebnisse
30
4.3.3.2 Carduus-Wald Fast alle Restwälder auf der 1. bis 3. Terrasse, sowie einzelne Bestände der Aue, sind dem
Carduus-Wald zuzurechnen. Unter tonigen (Gley-)Haftpseudogleyen (Abb.4.23) steht das
Grundwasser zwischen 0,4 und 2 m unter Flur. Dadurch, und durch die den Boden beschat-
tenden Bäume ist der Standort deutlich mesophil. Diese Flächen werden vom Vieh als Ru-
heplätze genutzt, wodurch es zu Störungen und besonders zur Eutrophierung kommt.
364N =
Quercus roburPopulus x canescens
Alter
in J
ahre
n
160
140
120
100
80
60
40
20
0
Substrat: Schluffige bis sandige Tone; z.T. Schluffe Typische Arten: Carduus crispus Stellaria media Cynoglossum germanicum Geum urbanum
Bodentyp KA 5: WRB: Russland:
Gley-Haftpseudogley Stagnic-Eutric Gleysol Meadow Soils
Kennzeichnende Artengruppen:
7-10; 12-15; 17-20 Weitere Bodenpa-rameter:
Humose Horizonte bis 20 cm mächtig Grundwasser zwischen 0,4 und 2,0 m u. Flur Humusform: L-Mull
Standorttyp: Ebenen der 1. bis 3. Terrasse. punktuell auch in der Aue
Wasserregime: Infiltration, selten Überflutung
Besonderheiten: Wald vom Vieh als Ruheplatz genutzt, dadurch entstehen stark eutrophierte Bereiche.
Abb.4.23: links: Cynoglossum germanicum im Carduus-Wald. Im Hintergrund Ulmus minor (April.2005) rechts: Profil Nr.25. Gley-Haftpseudogley in schluffigem Ton auf der 1. Terrasse (12.4.2005)
Stammzahl je ha: 281 Bestandeskreisfläche: 68 m²/ha gemessene Bäume: 130
Mittleres Alter in Jahren Quercus robur: 60 Populus x canescens: 33
Abb.4.24: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen des Carduus-Waldes, sowie Darstellung der Altersvertei-lung von Quercus robur und Populus x canescens im Boxplot.
L Axh Ah-Sg Sg Sg-Go
Wichtigkeit (I)
6
124
73
18
16
914 2 6
28
4Populus x c.QuercusUlmusCrataegusGleditsiaPyrusMalusElaeagnusRobiniaCornus sang.Morus
Abb.4.25: Mittlere Baumhöhen der Arten des Carduus-Waldes. Grundlage sind die mit der PCQ-Methode vermessenen Bäume.
0
2
4
6
8
10
12
14
16
18
Quercus Populus xc.
Robinia Gleditsia Ulmus Morus Crataegus Pyrus Malus Elaeagnus Cornussang.
Mit
tlere
Bau
mh
öh
e [
m]
Ergebnisse
31
Nitrophyten wie Hyoscyamus niger, Carduus crispus, Cynoglossum germanicum (Abb.4.23) und
Alliaria petiolata werden begünstigt. Cynoglossum germanicum kommt auch in Mitteleuropa
hauptsächlich auf Wildlägern vor (Weber 2003). Weiterhin sind alle typischen Arten der
geschlossenen Wälder wie Brachypodium sylvaticum, Geum urbanum und Festuca gigantea
sowie die Sträucher Ligustrum vulgare und Prunus spinosa anzutreffen. Auf kleinen Blößen
wachsen Eryngium campestre und Ranunculus bulbosus.
Quercus robur beherrscht mit durchschnittlich 17 m hohen Bäumen und I=124 die Bestände
(Abb.4.24; 4.25). Hauptsächlich sind die Bäume zwischen 40 und 70 Jahren alt, doch treten
auch alte Hudeeichen (ca. 150 Jahre) neben wenigen Jungbäumen (20 Jahre) auf. Naturver-
jüngung der Eiche ist kaum anzutreffen. An feuchten Stellen etablieren sich die Lianen Smi-
lax und Periploca mit Deckungsgraden um 70 % in den Kronen der Sträucher und Bäume.
Die Strauchschicht und zweite Baumschicht werden durch krummwüchsige Crataegus, Ul-
mus minor, sowie Pyrus und Malus geprägt (Abb.4.24), wobei der Weißdorn (I=73) klar do-
miniert. Robinia, Morus alba und Gleditsia caspica verwilderten aus Pflanzungen, sind aber
nur mit 12 % am Bestandesaufbau beteiligt. Untypisch ist das Vorkommen der Graupappel
auf der 1. Terrasse. Es beschränkt sich auf alte Grabenränder und Wälle. Wahrscheinlich
konnte die Pappel auf diesen anthropogenen Störstellen keimen, oder wurde sogar im Zuge
der misslungenen Aufforstungen um 1970 mit eingebracht.
4.3.3.3 Origanum-Wald Die Standorte des Origanum-Waldes weisen eine deutliche Prägung durch das Auenregime
auf. Trotz ihrer hohen Lage werden sie periodisch von Hochwässern flach überflutet, wo-
durch humus- und kalkreiches Material (überwiegend Schluffe) über sandigen Kiesen abge-
lagert wird. Es bilden sich Vegaböden (Abb.4.26) mit nur geringmächtigen Ah-Horizonten
aus.
Kennzeichnende Arten sind Origanum vulgare, Orchis militaris (Abb.4.26) und Polygala anato-
lica. Weiterhin haben Thalictrum minus, Fragaria viridis, Carex tomentosa und Agrimonia eupa-
toria ihren Schwerpunkt in diesem Vegetationstyp.
Die Bestände sind selten höher als 10 m (Abb.4.28) und mit 578 Bäumen je Hektar sehr dicht
bestockt. Davon entfallen allein 60 % auf den prägenden Crataegus (I=140) und 13 % auf Ul-
mus (I=34) (Abb.4.27). Beigemischt sind Malus, Gleditsia und junge Eichen. Ältere Eichen (40-
80 Jahre) erheben sich als Solitärbäume darüber. Auf flussnahen Flächen wachsen auch 30
bis 40 jährige Populus x canescens und Populus nigra, die Höhen von ca. 25 m und Durchmes-
ser von 80 cm erreichen. Eine Vermehrung dieser Pioniergehölze im Origanum-Wald wurde
aber nicht beobachtet.
Ergebnisse
32
1235N =
Quercus roburPopulus nigraPopulus x canescens
Alter
in J
ahre
n
100
80
60
40
20
0
Stammzahl je ha: 578 Bestandeskreisfläche: 50 m²/ha gemessene Bäume: 120
Mittleres Alter in Jahren Quercus robur: 45 Populus x canescens: 38 Populus nigra: 35
L; Of aAh aM II aM
Abb.4.26: links: Saum des Origanum-Waldes aus Crataegus. Davor Fragaria viridis und Euphorbia helioscopa blühend. (April 2005) mitte: Orchis militaris, typische Art des Origanum-Waldes. (Mai 2005) rechts: Profil Nr.18. Normvega auf Schluff über Kies (10.4.2005)
Abb.4.27: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen des Origanum-Waldes, sowie Darstellung der Altersver-teilung von Quercus robur und der Populus-Arten im Boxplot.
Abb.4.28: Mittlere Baumhöhen der Arten des Origanum-Waldes.
Wichtigkeit (I)
29
13
4
57
34
140
7 5 8 3 P. x canescensP. nigraElaeagnusQuercusUlmusCrataegus
MalusDiospyrosRobiniaGleditsia
Substrat: Schluffe über sandigen Kiesen Typische Arten: Origanum vulgare Potentilla recta Polygala anatolica Malus orientalis
Bodentyp KA 5: WRB: Russland:
Normvega Fluvisols calcaric Alluvials calcareous
Kennzeichnende Artengruppen:
7-10;12;14;17-21 Weitere Bodenparameter:
humus- und carbonatreiches Material Schmaler Ah Horizont Humusform: F-Mull
Standorttyp: erhöhte Ebenen in der Aue Wasserregime: Infiltration, Überflutung
Besonderheiten: Niedrige Wälder bis Gebüsche, Überflutungshöhe 0-50 cm
0
5
10
15
20
25
P. xcanescens
P. nigra Quercus Elaeagnus Robinia Diospyros Malus Ulmus Gleditsia Crataegus
Mit
tlere
Bau
mh
öh
e [
m]
Ergebnisse
33
4.3.3.4 Verbascum-Lichtung Auf ähnlichen Standorten wie denen des Origanum-Waldes gibt es baumfreie Blößen bis ca.
1 ha Größe. Der kiesige Boden und starke Sonneneinstrahlung bedingen schnelle Austrock-
nung.
Auf diesen Verbascum-Lichtungen dominieren thermophile Weideunkräuter, die z.T. auch
im Quercus-Wald vorkommen. Arten wie Ranunculus illyricus, Verbascum phoeniceum, Poa
bulbosa und Linum austriacum haben hier ihren Schwerpunkt, sind aber auch stellenweise im
Origanum-Wald anzutreffen. Besonders wärmeliebende Gehölze, so Ligustrum vulgare, Rosa
canina und Rhamnus cathartica treten hier auf. Gemeinsam mit Crataegus scheinen sie sich
trotz Beweidung auszubreiten.
Abb. 4.29: Verbascum-Lichtung als Büffelweide. Verbascum phoeniceum (purpur) Linum austriacum (hellblau) und Myagrum perfo-liatum (gelb) werden vom Vieh verschmäht und bleiben als „Weideunkräuter“ stehen. (Mai 2005)
Substrat: Flacher Schluff über sandigem Kies Typische Arten: Verbascum phoeniceum Linum austriacum Ranunculus illyricus Salvia nemorosa
Bodentyp KA 5: WRB: Russland:
Normvega Fluvisols Calcaric Alluvials calcareous
Kennzeichnende Artengruppen:
10; 17; 19-23 Weitere Bodenparameter:
Wie bei Origanum Wald Schnelle Austrocknung
Standorttyp: Hochgelegene sehr flache Kuppen in der Aue Wasserregime: Infiltration, (Überflutung)
Besonderheiten: Lichte Stellen bis 1 ha Größe, im Sommer täglich beweidet
Ergebnisse
34
4.3.4 Graupappelwälder
Die größten Teile der Aue sind mit Graupappelwäldern (Tab.4.2) bestanden. Sie erstrecken
sich über den 2 km breiten Talboden nördlich der Kura, und werden in höheren Bereichen
von Eichen-Ulmenwäldern, sowie entlang eines Quellbaches am Übergang zu den Terrassen
vom Alnus-Bachsaum unterbrochen (Abb.4.30). Erst in Flussnähe schließt sich dann die ei-
gentliche Weichholzaue an. Das prägende Element dieser Wälder sind mächtige Graupap-
peln, welche bis in ihre Kronen von Lianen umrankt werden. Besonders dichte Bestände
existieren am Fluss und an grundwassernahen Rinnen. Die Standorte innerhalb der Aue
unterscheiden sich durch ihre Substratfolgen, die Höhe der Überflutung sowie den Kronen-
schlussgrad der Bäume. Gemeinsamkeiten bestehen in hohen Carbonatgehalten (>7 Masse-
%) der Böden und den dynamischen Abtragungs- und Sedimentationsprozessen.
In allen Typen sind die Sträucher Ligustrum vulgare, Crataegus rhipidophylla, Euonymus euro-
paeus und Cornus sanguinea, die Lianen Smilax excelsa, Periploca graeca und Hedera helix, in der
Krautschicht Brachypodium sylvaticum, Glechoma hederacea, Geum urbanum sowie die Veilchen
Viola alba, V. odorata und V. sieheana hochstet vertreten. 3
4.3.4.1 Vincetoxicum-Wald Besonders in breiten Rinnen und auf grundwassernahen tiefergelegenen Ebenen in Flussnä-
he (Abb.4.31) wächst der Vincetoxicum-Wald. Nach Überflutungen kann sich in den Rinnen,
ähnlich wie in Altarmen, Wasser über Wochen stauen. Typische Böden sind Gley-Vega und
Abb. 4.30: Schematischer Querschnitt durch die Kura-Aue mit den verschiedenen Vegetationstypen.
Ergebnisse
35
Normvega auf schluffigen Tonen über Sanden. Einzelne Hochwässer können bis zu 15 cm
Sediment ablagern.
In der Krautschicht wachsen nur schattentolerante Arten wie Physalis algekengi oder Brachy-
podium sylvaticum, Frühblüher wie Viola spp. und Glechoma, sowie rankende Pflanzen, dar-
unter Asperula rivalis und das hochstete Vincetoxicum scandens.
1136N =
Quercus roburPopulus x canescens
Alter
in J
ahre
n
160
140
120
100
80
60
40
20
0
Substrat: Schluffige Tone über Sand oder Schluff Wasserregime: Infiltration und Überflutung
Typische Arten: Periploca graeca Populus x canescens Vincetoxicum scandens Clematis vitalba
Bodentyp KA 5: WRB: Russland:
Gley-Vega Calcaric Fluvisol Alluvials calcareous (kalkreicher Auenboden)
Kennzeichnende Artengruppen:
7-13 Weitere Bodenparameter: Humusform Mull Schmaler aAh-Horizont
Besonderheiten: Überflutungen bis 1,2 m kaum Beweidung
Standorttyp: Rinnen im Talboden und niedriggelegene Ebenen
W icht igkeit ( I)
101
32
35
104
152 22
222
P. x canescensQuercusUlmusCrataegusFraxinusPrunus cera.PyrusDiospyrosRobiniaCornus sang.M orus
Abb. 4.31: links: Direkt an den Fluss angrenzender Vincetoxicum-Wald mit Populus x canescens und Lianen (Mai 2005) mitte: Vincetoxicum scandens (Asclepiadacea) (Juni 2005) rechts: Profil Nr. 9. Gley-Vega auf schluffigem Ton über Mittelsand (5.4.2005)
L aAh aM aM-Go
Stammzahl je ha: 559 Bestandeskreisfläche: 79 m²/ha gemessene Bäume: 140
Mittleres Alter in Jahren Quercus robur: 43 Populus x canescens: 31
Abb.4.32: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen des Vincetoxicum-Waldes, sowie Darstellung der Alters-verteilung von Quercus robur und Populus x canescens im Boxplot.
Abb.4.33: Mittlere Baumhöhen der Arten des Vince-toxicum- Waldes.
0
5
10
15
20
25
30
P. xcanescens
Quercus Fraxinus Pyrus Robinia Ulmus Morus Crataegus Prunuscera.
Diospyros Cornussang.
mit
tlere
Bau
mh
öh
e [
m]
Ergebnisse
36
Acer campestre S
Agrimonia
Alliaria
Arctium
Asparagus officinalis
Asperula rivalis
Populus x canescens B1
Robinia B1
Crataegus B2
Pyrus B2
Ulmus B2
Populus nigra B1
Quercus B1
Carpinus B2
Malus B2
Morus alba B2
Tilia B2
Brachypodium
Buglossoides
Carex divulsa
Carex melanostachya
Carex tomentosa
Carpinus S
Cirsium arvense
Clematis vitalba
Vincetoxicum
Cynoglossum germanicum
Elytrigia
Eryngium
Euphorbia stricta
Festuca gigantea
Fragaria
Galium spurium
Geum
Glechoma
Gleditsia K
Hedera K
Hedera L
Humulus
Inula helenium
Listera
Lonicera caprifolium
Periploca
Phragmites
Physalis
Prunella vulgaris
Quercus K
Cornus mas S
Cornus sanguinea S
Euonymus S
Frangula S
Gleditsia S
Silene wallichiana
Ligustrum S
Smilax K
Smilax L
Prunus divaricata S
Prunus spinosa S
Pyrus S
Robinia S
Rosa canina
Thalictrum
Tilia S
Viola
Vitis vinifera
toniger Boden
schluffiger Boden
Mächtigkeit Ah-Horizont
Carbonatgehalt
Entfernung vom Fluss
0
0
40 80
40
80
Graupappelwälder
Achse 1
Achse 2
Artengruppen
6 – kennzeichnende Arten des Tilia-Waldes
7 –11 typische Arten aller Graupappelwälder
12; 13 – Arten des Vincetoxicum- und Alliaria Waldes
14; 17 – Arten des Alliaria Walde
Die feuchten Bedingungen sind ideal für das Wachstum der über 25 Meter hohen Graupap-
peln in der ersten Baumschicht sowie der Lianen Smilax und Periploca. In der zweiten Baum-
schicht stocken neben Eichen und Ulmen auch einzelne Exemplare von Fraxinus excelsior,
Robinia und Morus alba. Wiederum ist der Weißdorn in der hohen Strauchschicht dominant.
Er kann sich aber auch zu Bäumen mit 30 cm Durchmesser entwickeln. Die Gesamtdeckung
der höheren Stockwerke liegt über 100 %, wodurch der Boden fast vollständig beschattet
wird. Die überall präsente Stechwinde (Smilax) und die dichte Strauchschicht behindern das
Eindringen von Vieh.
Abb.4.34: DCA der Arten der Graupappelwälder mit Standortparametern. Arten aus Artengruppen mit gleicher Amplitude sind jeweils farbig unterstrichen. Der Gradient zwischen tonigen und schluffigen Böden wird in der Vegetationszu-sammensetzung deutlich. Ein kausaler Zusammenhang zwischen Vegetation und Carbonatgehalt ist hingegen nicht anzunehmen. Der von Achse 2 aufgezeigte Gradient ist mit den ausgegliederten Artengruppen nicht nachvollzieh-bar.
Ergebnisse
37
Vegetationstyp Nr.: 1 2 3 4 GW-Tiefe [m] 1,2-1,5 1-2 1-2 1 Terrasse 0 0 0;1 0 Höhe der Überflutung [cm] 0-80 30-120 0-80 80 Bodenart (0-40 cm) u;s t;u;s t;u u Bodenart (>40 cm) u;s/G t;u;s;G t;l;s;G u Mächtigkeit Ah-Horizont [cm] 4 6 13 5 Carbonat (0-40 cm) nach KA4 4 4 4 4
Nutzungsintensität 1.5 1.2 1.4 1 B1 Höhe [m] 27 25 20 B1 Deckung [%] 25 40 35 B2 Höhe [m] 12 12 9 B2 Deckung [%] 60 30 45 S Höhe [m] 2 2 2 3 S Deckung [%] 35 30 20 15 L Deckung [%] 15 15 20 70 K Höhe [m] 0.5 0.4 0.3 1.5
K Deckung [%] 35 40 35 2 Anzahl der Aufnahmen 4 7 7 5 AG 6
B2Tilia begoniifolia IV B2Carpinus betulus III STilia begoniifolia III SAcer campestre III I SCarpinus betulus II LLonicera caprifolium III
B1Populus nigra III KCarex divulsa V I
AG 7a
LSmilax excelsa V V V V LPeriploca graeca IV V IV V LHumulus lupulus III II III V
AG 7
SCornus sanguinea III IV V SEuonymus europaeus V V V
B2Crataegus rhipidophylla V V V LHedera helix V V V
B1Populus x canescens III V III
AG 8
KElytrigia repens III V V KBrachypodium sylvaticum V V V KHedera helix IV V V KGleditsia caspica II III IV KGalium spurium IV IV IV SPrunus divaricata IV IV
AG 9
KGlechoma hederacea V V V KViola sp. V V V
B2Ulmus minor V III V KPhysalis algekengi III III III KGeum urbanum V V V KBuglossoides purpurocaeroleum IV V V KAsperula rivalis II III III KFestuca gigantea IV I KVincetoxicum scandens IV V III KAgrimonia eupatoria II II III SFrangula alnus II I
Fortsetzung 1 2 3 4
AG 10
B2Robinia pseudacacia III II II SLigustrum vulgare V V V SCornus mas III II I SRobinia pseudacacia III II II SPyrus sp. I I
AG 11
LVitis vinifera III III LClematis vitalba III III I
B2Pyrus sp. II II II KEuphorbia stricta IV III II
B2Morus alba III III I
AG 12
SPrunus spinosa III V SGleditsia caspica III I
B1Quercus robur I III KSmilax excelsa II III KCarex tomentosa II III K Inula helenium I III KQuercus robur II III
AG 13
KCynoglossum germanicum II III III KAlliaria petiolata II V IV KListera ovata II III KArctium tomentosum III III KCarex melanostachya I II
AG 14
KThalictrum minus I IV KCirsium arvense III KFragaria viridis II
AG 17
KAsparagus officinalis II III KEryngium campestre II III
4.3.4.2 Alliaria-Wald
Die Standorte ähneln denen des Vincetoxicum-Waldes und können bis zu 80 cm überflutet
werden, wobei Schluffe und Tone sedimentieren. Durch starke Bodenaktivität bilden sich
trotz der hohen Dynamik deutlich erkennbare aAh-Horizonte in den Gley-Vegaböden aus.
Neben den Arten des Vincetoxicum-Waldes kommen auf stärker besonnten Flächen u.a. auch
Thalictrum minus, Asparagus officinalis, Agrimonia eupatoria und Buglossoides purpurocaeruleum
vor.
Tab.4.4: Übersichtstabelle der Typen der Graupappelwälder
Legende zur Tabelle:Vegetationstypen: 1 Tilia-Wald 2 Vincetoxicum-Wald3 Alliaria-Wald 4 Periploca-Lichtung Vegetationsschicht: B1 Baumschicht 1 B2 Baumschicht 2 S Strauchschicht L Lianenschicht K Krautschicht
Bodenart: t Ton u Schluff l Lehm s Sand G Kies Mittelwerte gerundet
Ergebnisse
38
Quercus und Populus sind hier gleichermaßen bestandesprägend (I=51), wobei die Eichen im
Durchschnitt zehn Jahre jünger sind, und einmal die Pappelüberhälter ablösen werden. Im
dichten Unterwuchs (775 Bäume je ha) dominiert Crataegus. Es sind jedoch weitere 21
Gehölzarten in der Strauchschicht beigemischt. Diese hohe Dichte und Diversität wird nur im
Alliaria-Wald erreicht. Gleditsia-Bäume spielen im Bestand eine völlig untergeordnete Rolle,
obwohl Keimlinge und Jungpflanzen in großer Zahl vorhanden sind.
187N =
Quercus roburPopulus x canescens
Alter
in J
ahre
n
80
70
60
50
40
30
20
10
7
Wichtigkeit (I)
2
51
382
126
72
51
5942 P. x canescens
ElaeagnusQuercusUlmusCarpinusCrataegusMalusPyrusEuonymusRobiniaGleditsiaMorus
Stammzahl je ha: 775 Bestandeskreisfläche: 74 m²/ha gemessene Bäume: 120
Mittleres Alter in Jahren Quercus robur: 32 Populus x canescens: 42
Abb.4.35: links: Graupappel im Alliaria-Wald, mit Efeu bewachsen. In der Krautschicht Cynoglossum germanicum. (April 2005) rechts: Profil Nr. 27. Gley-Vega aus stark schluffigem Ton über stark schluffigem Sand (13.04.2005)
L aAh aM aM-Go
Abb.4.36: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen des Alliaria-Waldes, sowie Darstellung der Altersvertei-lung von Quercus robur und der Populus x canescens im Boxplot.
Abb.4.37: Mittlere Baumhöhen der Arten des Alliaria-Waldes.
Substrat: schluffige Sande, Schluffe, schluffige Tone
Typische Arten: Alliaria petiolata Thalictrum minus Prunus spinosa Buglossoides purpurocaeruleum
Bodentyp KA 5: WRB: Russland:
Gley-Vega, Vega Fluvisols calcaric Alluvials calcareous
Weitere Bodenparameter: Humusform: L-Mull Kennzeichnende Artengruppen:
7-14; 17 Wasserregime: Infiltration und Überflutung
Besonderheiten: zumeist beweidet. auf lichten Stellen thermophile Arten
Standorttyp: Ebenen des Talbodens; selten auch auf 1. Terrasse
0
5
10
15
20
25
30
P. x can
esce
ns
Quercus
Gleditsia
Morus
Robinia
Malus
Ulmus
Cratae
gus
Carp
inus
Pyru
s
Euon
ymus
Elae
agnu
s
mit
tlere
Bau
mh
öh
e [
m]
Ergebnisse
39
4.3.4.3 Tilia-Wald Auf Standorten mit guter Wasserversorgung und schluffigen Böden (Abb.4.41) etablieren sich
anspruchsvolle Laubhölzer (Tilia begoniifolia, Acer campestre, Carpinus betulus) in 45 bis 70 jäh-
rigen (Abb.4.39) Vincetoxicum-Wäldern.
513N =
Quercus roburPopulus nigraPopulus x canescens
Alter
in J
ahre
n
80
70
60
50
40
30
20
10
Abb.4.38: links: Tilia begoniifolia (hellgrün) zwischen Smilax (braun) und Graupappel (silbern) (Mai 2005) rechts: Sich zwischen Lianen behauptende Tilia begoniifolia (hinten links) in alter Baumsturzlücke; im Mittelgrund
eingewachsener Graupappelstumpf; vorne Ranke von Smilax excelsa. (Juni 2005)
Wichtigkeit (I)
51
10
24
34
125
15
733
19 9 P. x canescensP. nigraQuercusUlmusCrataegusTiliaAcerMalusCornus masRobiniaMorus
Stammzahl je ha: 669 Bestandeskreisfläche: 67 m²/ha gemessene Bäume: 80
Mittleres Alter in Jahren Quercus robur: 34 Populus x canescens: 52 Populus nigra : 58
Abb.4.39: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen des Tilia-Waldes, sowie Darstellung der Altersverteilung von Quercus robur und der Pappeln im Boxplot.
Abb.4.41: Profil Nr.42. Normvega auf tonigem Schluff mit frischer Sedimentlage (24.4.2005)
Abb.4.40: Mittlere Baumhöhen der Arten des Tilia-Waldes.
aA(i)h aAh-aM aM
Substrat: Schluff Typische Arten: Tilia begoniifolia Carex divulsa Acer campestre Carpinus betulus
Bodentyp KA 5: WRB: Russland:
Normvega Calcaric Fluvisol Alluvials calcareous (kalkreicher Auenboden)
Kennzeichnende Artengruppen:
6-11 Weitere Bodenparameter: Humusform Mull Schmaler aAh-Horizont
Standorttyp: Ebenen Besonderheiten: Überflutungen bis 0,8 m kaum Beweidung seltener Waldtyp Wasserregime: Infiltration und Überflutung
0
5
10
15
20
25
30
P. x can
esce
ns
P. n
igra
Quercus
Robinia
Tilia
Acer
Malus
Morus
Ulmus
Crat
aegu
s
Corn
us m
as
Mit
tlere
Bau
mh
öh
e [
m]
Ergebnisse
40
Diese sehr seltenen Bestände sind auf einen schmalen Streifen, der in ca. 200 m Entfernung
parallel zum Fluss verläuft, beschränkt.
Charakteristisch sind mächtige, über 40 Jahre alte Pappeln, die sich teilweise schon im Zerfall
befinden (Abb.4.38). Darunter entwickelt sich die neue Baumgeneration aus Quercus, Ulmus,
Tilia, und Acer. Die bis 6 m hohe Strauchsicht wird von Crataegus dominiert. In der Kraut-
schicht und niedrigen Strauchschicht wachsen viele junge Acer-, Carpinus- und Tilia-Pflanzen
sowie Cornus mas. Auch anspruchsvolle Lianen, so Lonicera caprifolium und Vitis vinifera, sind
hier anzutreffen. Eine kennzeichnende Art in der Krautschicht ist Carex divulsa. Neben den
absterbenden Pappeln werden auch Linden und Ahorne umgesägt und als Brennholz ab-
transportiert. Das ist eventuell eine der Ursachen für die Seltenheit der Tilia-Wälder.
4.3.4.4 Periploca-Lichtung Auf feuchten Standorten in Rinnen im Talboden existieren Lichtungen, die von einem zwei
bis drei Meter hohen Flechtwerk aus Smilax und Periploca bestehen. Dazwischen wachsen nur
noch Rubus canescens, Humulus lupulus und einzelne bis 6 m hohe Phragmites-Halme empor
(Abb.4.42). Sehr wenige schnellwüchsige Morus- und Robinia-Bäume können den Lianen
standhalten und führen eventuell zur Ausbildung neuer Wälder.
Abb.4.42: links: Periploca-Lichtung mit Humulus lupulus, Phragmites, Smilax und Rubus canescens (Mai 2005) mitte: Blüte von Periploca graeca (Asclepiadaceae) (Juni 2005) rechts: Früchte von Smilax excelsa (Smilacacea) (April 2005)
Standorttyp : Rinnen und niedrige Ebenen Wasserregime: Grundwassser und Überflutung
Typische Arten: Humulus lupulus Periploca graeca Smilax excelsa Phragmites australis Rubus canescens
Besonderheiten: Undurchdringliche 2 m hohe Lianenschicht -> unbeweidet Lichtungen bis 0,5 ha Größe Zerfallsphase des Graupappelwaldes
Ergebnisse
41
4.3.5 Weichholzwälder Auf den jungen Kiesbänken und Inseln im Fluss wachsen Gebüsche und Wälder aus Pionier-
gehölzen, die einer hohen Dynamik ausgesetzt sind. Flache Inseln werden durch Hochwässer
so stark gestört, dass sich darauf höchstens Ephemerenfluren einstellen können (Abb.4.43).
Auf höheren Kies- und Sandbänken etabliert sich die Tamarix-Weichholzaue, die zur Populus-
Weichholzaue überleitet. Ein anderer Typ der Weichholzwälder ist der Alnus-Bachsaum an
permanent wasserführenden Bächen am Rande des Talbodens.
Vegetationstyp Nr.: 1 2 3
GW-Tiefe [m] 0,4 1-1,5 0,2-0,4 Terrasse 0 0 0 Höhe der Überflutung [cm] 80 50-100 20-150 Bodenart (0-40 cm) s u;s u;t Bodenart (>40 cm) s/G u;s;G u;t Mächtigkeit Ah-Horizont [cm] 0 0 4 Carbonat (0-40) nach KA4 4 4 3
Nutzungsintensität 1 2 1,2 B1 Höhe [m] 24 22 B1 Deckung [%] 50 20 B2 Höhe [m] 15 12 B2 Deckung [%] 35 30 S Höhe [m] 5 2 3 S Deckung [%] 70 30 45 L Deckung [%] 5 30 K Höhe [m] 0.7 0 1
K Deckung [%] 10 20 45 Anzahl der Aufnahmen 2 3 5 AG 4
SPopulus nigra V SSalix triandra V KCalamagrostis pseudophragmites V
AG 3 STamarix ramosissima V IV KAlopecurus tiflisiensis V IV KXanthium strumarium V IV KLolium perenne V IV KRanunculus repens III IV KPhalaris arundinacea III II II KCyperus rotundus III II
AG 5 B1Salix alba II B2Salix alba II B2Populus nigra IV KConyza canadensis IV
AG 8 KElytrigia repens V KBrachypodium sylvaticum V KHedera helix IV II KGleditsia caspica II KGalium spurium II KPrunella vulgaris II
Fortsetzung: 1 2 3 AG 1
SSalix alba III II III SAcer negundo III II II SAmorpha fruticosa V V III LCalystegia sepium II III KLycopus exaltatus V II IV
AG 7 SCornus sanguinea II V SEuonymus europaeus III
B2Crataegus rhipidophylla III LSmilax excelsa II V LPeriploca graeca IV V LHumulus lupulus II IV LHedera helix II IV
B1Populus x canescens II III AG 2
B2Alnus glutinosa IV KRanunculus sceleratus III KLysimachia vulgaris IV KCarex acutiformis IV KNasturtium officinalis V K Iris pseudacorus V KMentha aquatica V KSparganium erectum IV KLythrum salicaria IV KCarex riparia IV
Abb.4.43: Der verzweigte Flusslauf mit Treibholz, Sand- und Kiesbänken nach einem Hoch-wasser (Mai 2005)
Tab.4.5: Übersichtstabelle der Weichholzwälder
Legende zur Tabelle:Vegetationstypen: 1 Tamarix-Weichholzaue 2 Populus-Weichholzaue 3 Alnus-Bachsaum Vegetationsschicht: B1 Baumschicht 1 B2 Baumschicht 2 S Strauchschicht L Lianenschicht K Krautschicht
Bodenart: t Ton u Schluff s Sand G Kies Mittelwerte gerundet
Ergebnisse
42
4.3.5.1 Tamarix-Weichholzaue Im jungen und nährstoffreichen Flusssediment, auf Ramblaböden, können nach den Hoch-
wässern Ephemere und Gehölze keimen. Außerdem siedeln sich einige Arten durch ange-
spülte Pflanzenteile an. Dazu sind Calamagrostis pseudophragmites und Cyperus rotundus zu
rechnen. Typische Ephemere sind Xanthium strumarium, Bromus sterilis und auch Tomaten
(Lycopersicon esculentum). Während des Bearbeitungszeitraumes waren die Annuellenfluren
aber größtenteils von Hochwässern vernichtet. Von einer reichhaltigeren Entfaltung im
Sommer ist auszugehen. Alle diese heliophilen Arten werden sehr schnell durch die sich aus-
breitenden Gehölze verdrängt.
Bedingt durch hohe Sonneneinstrahlung im Sommer, kommt es zu Trockenstress, dem am
besten die Tugai-Arten Tamarix ramosissima, T. meyeri und Elaeagnus caspica gewachsen sind.
Jungpflanzen von Populus nigra, P. x canescens, Salix alba und S. triandra keimen in sehr dich-
ten Verbänden, die bei einem Alter von sieben Jahren noch eine Dichte von 9800 Pflanzen je
ha aufweisen. Sie werden durch den Trockenstress in ihrer Entwicklung gehemmt, und be-
ginnen ihr schnelles Wachstum erst, wenn sie sich durch Beschattung des Bodens ein feuchte-
res Mikroklima geschaffen haben. Nun kann sich in wenigen Jahren die Populus-Weich-
holzaue etablieren.
Abb.4.44: links: Tamarix-Weichholzaue mit jungen Populus nigra (vorne links) und Tamarix ramosissima; dahinter älteres Stadium der Populus-Weichholzaue (Mai 2005) rechts: Calamagrostis pseudophragmites, typische Art an mittelasiatischen Flussläufen (Mai 2005)
Substrat: Kiese und Sande unter flachen Tonen und Schluffen
Typische Arten: Tamarix ramosissima Populus nigra Salix triandra Calamagrostis pseudophragmites Xanthium strumarium
Bodentyp KA 5: WRB: Russland:
Normrambla Calcaric Fluvisol Alluvials calcareous (kalkreicher Auenboden)
Kennzeichnende Artengruppen:
1;3-4 Weitere Boden-parameter:
Carbonatreich Jährlicher Auftrag neuer M-Horizonte
Standorttyp: Sand- und Kiesbänke im verzweigten Flusslauf Besonderheiten: Oft überflutet, dadurch starke Schäden an Gehölzen Wasserregime: Überflutung und Infiltration
Ergebnisse
43
4.3.5.2 Populus-Weichholzaue Ab einem Alter von sechs Jahren erreichen die Pappelbestände der Tamarix-Weichholzaue die
Dickungsphase. Alle unterdrückten Bäume sterben nun ab und werden als Feuerholz ge-
nutzt. Im Sommer gelangt das Vieh aus den südlich angrenzenden Dörfern auf die Inseln und
schädigt die Pappelbestände zusätzlich. Mit nur noch 390 Bäumen je ha bei einem Alter von
17 Jahren entsteht ein sehr lichter, von Populus nigra dominierter Wald. Salix alba und Tama-
risken sind noch beigemischt, prägen die Bestände aber nur gering (Abb.4.46). Neben Arten,
die schon auf freien Kiesbänken vorkommen (AG 3) stellen sich langsam Vertreter der älteren
Wälder wie Eytrigia repens, Hedera helix und Brachypodium sylvaticum ein.
38N =
Populus nigra
Alter
in J
ahre
n
30
20
10
0
Abb.4.45: links: Bestand aus Populus nigra mit Hedera helix auf Insel im verwilderten Flusslauf (März 2005) rechts: Normrambla in kiesig-sandigem Substrat (28.05.05)
Stammzahl je ha: 388 Bestandeskreisfläche: 20 m²/ha gemessene Bäume: 40
Mittleres Alter in Jahren Populus nigra: 17
Abb.4.46: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen der Populus-Weichholzaue, sowie Darstellung der Alters-verteilung von Populus nigra im Boxplot.
Wichtigkeit (I)
278
11 11
Populus nigra
TamarixramosissimaSalix alba
Substrat: Kiese und Sande unter flachen Tonen und Schluffen Typische Arten: Populus nigra Salix alba Elytrigia repens Conyza canadensis
Bodentyp KA 5: WRB: Russland:
Normrambla Calcaric Fluvisol Alluvials calcareous (kalkreicher Auenboden)
Kennzeichnende Artengruppen:
1;3;5;7-8 Weitere Bodenparameter: Carbonatreich jährlicher Auftrag neuer M-Horizonte
Standorttyp: Sand- und Kiesbänke im verzweigten Flusslauf Besonderheiten: Oft überflutet, dadurch starke Schä-den an Gehölzen Wasserregmie: Überflutung und Infiltration
aAi aelC
Ergebnisse
44
4.3.5.3 Alnus-Bachsaum Eine Sonderstellung in der Aue nehmen die Säume entlang ganzjährig wasserführender Bä-
che ein. Nur hier ist Alnus glutinosa mit der transkaukasischen Unterart barbata vertreten. Au-
ßerdem stehen am Bachufer noch lianenumrankte Quercus, Morus (Abb.4.49) und Cornus san-
guinea. Auch die Neophyten Amorpha fruticosa und Acer negundo sind hier hochstet vertreten.
Derartige Wälder wachsen sonst nur in der niederschlagsreichen Kolchis-Niederung oder in
den Hyrkanischen Wäldern am Kaspischen Meer (Gulisaschvili et al. 1976). Auf den tonigen
Gleyen und Nassgleyen gedeihen Carex acutiformis, Iris pseudacorus, Carex remota und Mentha
aquatica. Wo Quellwasser in den Bach strömt wächst Nasturtium officinale. Dieser Wald und
der Bach wirken als Barriere am Rande der Aue. Nur an wenigen Stellen legte man Furten an
um das Vieh in den dahinterliegenden Auwald treiben zu können.
Stammzahl je ha: 311 Bestandeskreisfläche: 33 m²/ha gemessene Bäume: 16
Mittleres Alter in Jahren Quercu robur 59
Wichtigkeit (I)
36
33
30
37
164
Alnus
Quercus
Crataegus
Cornus sanguinea
Morus
Abb.4.47: links: Einblick in den Alnus-Bachsaum mit Iris pseudacorus in der Nähe einer Furt. (Mai 2005) rechts: Normnassgley am Ufer eines Baches. (13.04.2005)
Abb.4.48: Wichtigkeit (I) der Baumarten und forstliche Kennzahlen sowie mittlere Baumhöhen des Alnus-Bachsaumes.
Substrat: Schluffige Tone Typische Arten: Alnus glutinosa Iris pseudacorus Carex remota Cornus sanguinea
Bodentyp KA 5: WRB: Russland:
Normnassgley Gleysol Meadow-Soil
Kennzeichnende Artengruppen:
1;2;7 Weitere Bodenparameter: Carbonatreich Jährlicher Auftrag neuer M-Horizonte
Wasserregime: topogen und Überflutung Standorttyp: Senken am Rande der Aue
Ah-Go Go Go-Gr
0
5
10
15
20
Alnus Quercus Morus Crataegus Cornussanguinea
mit
tlere
Bau
mh
öh
e [
m]
Ergebnisse
45
4.4 Sozioökonomische Situation der umliegenden Dörfer
4.4.1 Übersicht Das Schutzgebiet ist von neun Dörfern (Abb.2.1) mit insgesamt ca. 10 000 Einwohnern umge-
ben, wobei es deutliche Unterschiede zwischen den Siedlungen im Norden und Süden gibt.
Die südlich angrenzenden Orte Schichli I und II sowie Juchari Salachli liegen an der Fernstra-
ße Tiflis – Baku. Ihre Bewohner verkaufen Waren an Ständen entlang der Straße und betrei-
ben auf kleinen Feldern Ackerbau (Abb.4.49). Ihre Viehherden weiden in der südlich angren-
zenden Steppe, und werden nur im trockenen Sommer auf die Inseln im Fluss getrieben.
Nach den Hochwässern nutzen die Anwohner das Schwemmholz zur Feuerung. Die Abhän-
gigkeit von Flächen im Zapovednik, und damit die Intensität der Störungen, ist wesentlich
geringer, als die der Orte nördlich der Kura.
Am Nordrand des Zapovedniks sind die Ortschaften entlang der Eisenbahntrasse verteilt,
wobei Muganli mit ca. 2000 Einwohnern der größte Ort ist. Da ich während der Feldarbeiten
dort wohnte, und am Leben der Bewohner teilnehmen konnte, soll nun der Fokus, stellvertre-
tend für die anderen Dörfer, auf diesen Ort gelegt werden.
Abb.4.49: Blick von Schichli I nach Süden: Vorne die eingefriedeten Anwesen mit Obstgärten, in der Mitte die Fernstraße und kleine Äcker. Dahinter eine Hochterrasse mit weidendem Vieh in der Artemisia-Steppe. Am Horizont die Ausläufer des Kleinen Kaukaus mit Buchen-Hainbuchenwäldern in Armenien. (Juni 2005)
Abb. 4.50: Kartoffellegen am Rande eines Hirseackers bei Muganli. Dahinter geschneitelte Eichen des Quercus-Waldes. (April 2005)
Ergebnisse
46
4.4.2 Landwirtschaft Muganli ist eine wachsende Streusiedlung auf der 4. Terrasse in der Kura-Niederung und
besteht aus ca. 300 Hofstellen, die über ein verzweigtes Netz aus unbefestigten Wegen mit-
einander verbunden sind. Neben den Häusern, Brunnen und Viehschuppen stehen meist
mächtige Eichen als sommerliche Schattenspender. Daran schließt sich ein bewässerter Obst-
garten und ungefähr 0,5 ha kleine Felder für den Gemüse-, Mais- und Hirseanbau an, welche
durch Hecken aus Gleditsia caspica geschützt werden. Einige Familien bewirtschaften zusätz-
lich noch Äcker am Dorfrand und im Schutzgebiet (Abb.4.50). Zwischen den Gärten und am
Rande des Dorfes weiden das Jungvieh und Geflügel zusammen mit Schafherden, die
manchmal auch auf das Feuchtgrünland getrieben werden. Büffel und Kühe grasen in größe-
rer Entfernung zum Dorf auf den niederen Terrassen, und vor allem im Sommer in den Au-
wäldern. Tab.4.6 fasst die wichtigsten Nutztiere und Nutzpflanzen zusammen.
Nutztiere Feldfrüchte Gemüse Obst
Wasserbüffel Kühe
Pferde und Esel Schafe Puten
Hühner Gänse Bienen
Mais Hirse
Winterweizen Kartoffeln
Tomaten Bohnen
Kohlarten Zwiebeln
Pflaumen Aprikosen
Sauerkirschen Birnen und Äpfel
Kakipflaumen Kornelkirschen
Wein Maulbeeren
Kaum ein Bewohner dieser strukturschwachen Gegend steht in einem festen Arbeitsverhält-
nis. Da zudem die Löhne, Renten und Arbeitslosengelder sehr gering sind, besteht eine hohe
Abhängigkeit von der Subsistenzlandwirtschaft. So werden fast alle Erzeugnisse in den Fami-
lien verbraucht. Als Wintervorrat werden Kartoffeln und Zwiebeln eingelagert und Obst und
Gemüse eingekocht. Große Mengen des Obstes werden auch vergoren und zu minderwerti-
gen Obstbränden weiterverarbeitet. Der Genuss dieser Getränke bleibt den Männern vorbe-
halten. Für die aufwendige Pflege der Mais- und Hirsekulturen mit einfachsten Handgeräten
sind vornehmlich die Frauen zuständig, deren gesamte Arbeitskraft im Haushalt und der
Landwirtschaft gebunden ist. Hirsebesen sind eine wichtige Einnahmequelle der Dörfer in
der Garayazi-Steppe und werden hauptsächlich nach Georgien exportiert. Sie werden von
den Familien arbeitsintensiv per Hand im Winter gebunden. Ein Hektar Acker liefert dabei
Material für 2000 Besen, die für umgerechnet 0,5 US$ pro Stück verkauft werden. Mit der
Weiterverarbeitung der Aufwüchse eines Hektars Hirse wird somit ein Erlös von 1000 US$
erzielt, von dem höchstens 50 US$ für den Transport und Verkauf auf den nahegelegenen
georgischen Märkten abgezogen werden müssen. Bei einem durchschnittlichen Monatsein-
kommen von 25 US$ (SSCAR 2006), hat die Bewirtschaftung der kleinen Felder also große
Bedeutung. Als Koppelprodukt fallen auch Hirsesamen zur Fütterung an. Da alle Arbeits-
Tab. 4.6: Die wichtigsten Nutztiere und Nutzpflanzen der Dörfer
Ergebnisse
47
kraft der Frauen gebunden ist, und die Männer für gewöhnlich nur wenig arbeiten, ist eine
Erweiterung der Produktion im Ackerbau nicht möglich.
Körnermais wird fast ausschließlich in der eigenen Geflügelhaltung veredelt. Als Beispiel ist
eine Kostenrechnung für das 0,64 ha große Maisfeld der Familie Musayev angeführt
(Tab.4.7). Datengrundlage sind die Aussagen des Hausherren und eigene Beobachtungen.
Auf einen Hektar hochgerechnet, müssen 34,40 US$ und 300 unbezahlte Arbeitskraftstunden
(Akh) erbracht werden, um 47 dt Körnermais mit einem internen Zukaufswert von 1044 US$
zu ernten. Zum Vergleich liegt der Ertrag von Körnermais in Mitteleuropa bei 100 dt/ha (Hin-
terholzer 1999). Den Nutzern der nichtlegitimen Äcker im Schutzgebiet würden so ca. 1000
US$ je Hektar und Jahr entgehen, käme es zu einem Bewirtschaftungsverbot.
Körnermaisanbau auf 0,64 ha der Familie Musayev; Muganli
0,64 ha Betrag je ha Bemerkungen:
Finanzielle Aufwendungen [US$]
Fixkosten -/- -/- Keine Pacht, Grundsteuer, eigene Maschinen
Pflügen und Einsaat Wasser Sonstiges Gesamt
13,30 6,50 2,20
22,00
34,40 US$
Extern, durch Traktorbesitzer Undurchschaubares Quotensystem Zaun etc.
Arbeitsleistungen Zeit [Akh] Werden von Familie erbracht
Bewässerung Unkrautbekämpfung Ernte und Aufbereitung Abräumen des Feldes Gesamt:
4 x 10 64 80 8
192
300 Akh
Ertrag Marktpreis [US$/dt] Erlös [US$]
30 dt 22,20
667,00
47 dt
1044,00
In Mitteleuropa 100 dt/ha Ohne Anrechnung der Arbeitszeit.
Gewinn [US$] 645,00 1010,40 Theoretisches Einkommen der arbeitenden Frauen läge damit bei 3 US$/h.
Ein weiteres Standbein ist die Viehzucht, wofür jede Familie im Durchchnitt ca. acht Mutter-
schafe mit Lämmern, eine Milchkuh, sechs Büffel und ein Pferd oder Esel besitzt. Zum Ort
gehören somit ungefähr 2400 Schafe, 300 Kühe, 1800 Wasserbüffel und 300 Pferde bzw. Esel,
die nur im Winter mit Heu zugefüttert werden. Silage wird nicht verwendet. Neben großen
Mengen an Geflügel wird der Eigenbedarf an Fleisch durch Schafe und Kälber gedeckt. Die
Kuh- und Büffelmilch wird zu Käse verarbeitet, doch gibt eine Büffelkuh wegen suboptima-
ler Haltungsbedingungen nur durchschnittlich 1 kg Milch je Tag. Finanziell bedeutend ist der
Verkauf von Wolle (2 US$/kg). Auch Jungpferde und Büffel bringen auf Viehmärkten Erlöse
zwischen 250 und 500 US$ pro Stück. Einige Imker verkaufen Honig in die Kreisstadt, doch
sind die Erträge durch schlechte Pflege der Stöcke extrem niedrig. Es finden höchstens zwei
Honigernten im Jahr statt, wobei die Robinientracht die größte Rolle spielt. Ich nahm an einer
Ernte teil, bei der wir 20 kg Honig von sechzehn Völkern ernteten. Der Jahresertrag lag bei
diesem Imker bei 40 kg, also bei 2,5 kg je Volk. Imker in Deutschland ernten fast die zehnfa-
che Menge.
Tab. 4.7: Kostenrechnung für ein Maisfeld in Muganli und Hochrechnung auf ein Hektar
Ergebnisse
48
4.4.3 Energieversorgung Bis ins Jahr 2002 war der Ort noch an die Erdgasversorgung angeschlossen, welche aber we-
gen technischer Überalterung eingestellt wurde. Die Stromversorgung funktioniert hingegen
mit nur wenigen Stunden Ausfall am Tag. Nach Jahrzehnten mit relativ moderner Energie-
versorgung müssen die Einwohner deshalb wieder auf Holz zum Kochen und Heizen zu-
rückgreifen. Neben Abschnitten von Obstbäumen werden verstärkt auch die Eichen im Dorf
geschneitelt. Um 1970 wurden zur Bauholzgewinnung für die Kolchosen und Sovchosen Ro-
binienplantagen angelegt (Musajev 1984). Von diesen werden nun mit langen Stangen illegal
Äste abgebrochen. Bei anhaltender Erntemenge werden die Plantagen bis 2010 verschwun-
den sein. Weiterhin werden Treibholz und alle abgestorbenen Bäume des Auwaldes genutzt.
Diese Holzvorräte nehmen durch Übernutzung ab, und es steht zu befürchten, dass in naher
Zukunft auch die Wälder der niederen Terrassen und der Aue nach und nach abgeschlagen
werden. Das Feuerholz wird vorher kaum aufgearbeitet sondern oft als ganzer Stamm auf
einfache Feuerstellen gelegt (Abb.4.51). Eine Bevorratung ist unüblich.
Abb.4.51: oben links: Bauer beim Zerhacken von Walnuss-holz vor seinem Hirseacker.
Neben ihm eine Eiche vom Eichenbock (Cerambyx cerdo) befallen (April 2005)
oben rechts: Backen von Brotfladen an einfacher Feuerstelle. Am Bildrand Utensilien zur Schnapsbrennerei. (Mai 2005)
links: Typischer Laden mit angeschlossener „Schankstube“ in Muganli (Juni 2005)
Ergebnisse
49
4.4.4 Bevölkerung Aserbaidschan hat eine sehr junge Bevölkerung – 27 % sind unter 15 Jahre alt - und einen
deutlichen Geburtenüberschuss (SSCAR 2006). In Muganli gehen 500 Kinder, also ein Viertel
der Einwohner des Ortes, in die Schule und allein im April 2005 wurden 42 Ehen geschlossen.
In einem durchschnittlichen Haushalt des Ortes wohnt ein Ehepaar mit zwei bis drei Kin-
dern, zwei Großeltern und manchmal noch weiteren Familienangehörigen. So kommen auf
eine Hofstelle zwischen sechs und sieben Bewohner. Obwohl einige Jugendliche nach Baku
ziehen, scheint die Einwohnerzahl zu steigen und es werden auch ständig neue Häuser er-
richtet. Das Geld dafür stellen meist im Ausland arbeitende Verwandte zur Verfügung.
Im Ort gibt es nur sehr wenige, äußerst schlecht bezahlte Arbeitsplätze im Krankenhaus,
Schule, der Gemeinde- und Schutzgebietsverwaltung. Wenige einfache Läden werden von
Selbstständigen betrieben. Auch diese Einkommen reichen nicht für die Versorgung der Fa-
milien. Deshalb ist die Rolle der Landwirtschaft existentiell. Von steigenden Einwohnerzah-
len und dem damit verbundenen Nutzungsdruck werden künftig zusätzliche Gefährdungen
für das Zapovednik ausgehen.
4.5 Zustand des Schutzgebietes Im Folgenden wird die Arbeit der Schutzgebietsverwaltung und der Grad der Nutzungsfrei-
heit des Zapovedniks beschrieben. Die Ergebnisse dieser Analyse werden in der Diskussion
später wieder aufgegriffen, um Gefährdungen abzuleiten und konkrete Verbesserungsmaß-
nahmen vorzuschlagen.
Garayazi ist das älteste Schutzgebiet Aserbaidschans, welches bereits 1701 von Zar Peter dem
großen als Jagdreservat eingerichtet wurde (Musajev 1984). 1978 wurde es dann als 49 km²
großes Naturschutzgebiet ausgewiesen (Kovalev 2000). Das Zapovednik umfasst heute, nach
einer Erweiterung im Jahre 2001, 9658 ha der Kura-Niederung und ist Staatseigentum. Der
angrenzende Auwald auf georgischer Seite wird durch das 3484 ha umfassende Reservat
Gardabani geschützt. Nach Angaben des WWF (2005) beträgt die Fläche der in beiden Reser-
vaten eingeschlossenen Auwälder 2129 ha und die der Niederungswälder 1400 ha. Der frü-
hen Unterschutzstellung ist es wohl zu verdanken, dass hier Wälder auf landwirtschaftlichen
Gunststandorten überdauern konnten.
Ergebnisse
50
Zapovedniks wurden eingerichtet, um durch Abschirmung die ungestörte Entwicklung eines
Landschaftsausschnittes zu gewährleisten (WWF 2005). Auch nach dem heutigen Gesetz ist
jegliche Nutzung in den Naturschutzgebieten untersagt (Umweltministerium Aserbaidschan
2006). Als Schutzziel für das Gebiet muss also die ungestörte Entwicklung der Au- und Nie-
derungswälder angesehen werden.
4.5.1 Schutzgebietsverwaltung Die Schutzgebietsverwaltung besteht aus 42 schlecht augebildeten Mitarbeitern, die mit der
Sicherung des Gebietes beauftragt sind. Der Hauptsitz steht in Poily am Ostrand des Schutz-
gebietes und ist nur sehr sparsam mit Schreibtischen, zwei Schreibmaschinen und Stühlen
ausgestattet. Unterlagen zum Gebiet oder anderes Arbeitsmaterial fehlen weitgehend. Als
einziges Fahrzeug steht dem Chef ein Lada Niva zur Verfügung. Alles weitere Material müss-
ten sich die Mitarbeiter selbst zulegen, welche ca. 20 US$ pro Monat verdienen. Trotz nicht-
vorhandener Ausstattung sind im Innendienst Sekretärinnen, Buchhalterinnen und Laboran-
ten beschäftigt, deren Produktivität gering ist. In Abb.4.52 werden die Strukturen der Verwal-
tung dargestellt. Direkt an der Basis arbeiten „Ranger“, die in den umliegenden Orten woh-
nen und denen jeweils ein Streifen des Gebietes bis zum Fluss zugeteilt ist. In Dreier- bis Vie-
rergruppen unterstehen sie je einem ortsansässigen Inspektor. Ihre Aufgabe ist es, alle For-
men der Landnutzung im Gebiet zu unterbinden, und dafür per Pferd oder zu Fuß ihr Ter-
rain zu durchstreifen. Ich lernte fast alle Mitarbeiter kennen, von denen aber nur wenige ihre
Pflichten erfüllten. In der Realität finden Kontrollgänge nur einmal im Monat statt, ansonsten
wird die Zeit zum Erfahrungsaustausch, Betreuung der eigenen Äcker und des Viehs im
Schutzgebiet, sowie zur Werbung von Feuerholz genutzt.
Inspektor des Umweltministeriums (kontrolliert sporadisch)
Leiter der Verwaltung
Wissenschaftlicher Leiter Chef der Inspektoren
2 Laboranten 10 Hausmeister, Sekretä-rinnen, Buchhalterinnen etc.
6 Inspektoren
20 „Ranger“
Abb.4.52: Organisation der Schutzgebietsverwaltung nach Angaben des Wissenschaftlichen Leiters. (Stand Juni 2005)
Ergebnisse
51
Inspektoren des Ministeriums kontrollieren unregelmäßig die Durchführung der Aufgaben.
Vor solchen Kontrollen wird das Vieh nicht in das Gebiet getrieben und staut sich als blöken-
de Masse im Dorf. Der Inspektor wird durch diesen Stau gefahren und angesichts des kurzra-
sigen Feuchtgrünlandes davon überzeugt, dass im Moment keine Beweidung im Schutzge-
biet stattfindet. Nach einer Beratung endet die Inspektion.
Nur in seltenen Fällen wird von Holzdieben eine Strafe von 10 US$ gefordert, was wenigs-
tens das Unrechtsbewusstsein in der Bevölkerung aufrechterhält, und die Diebstähle in die
Nacht verlagert. Um alle Probleme zu lösen, möchte der Direktor einen tiefen Kanal als Gren-
ze um das Gebiet baggern lassen. Dieser Eingriff würde die hydrologischen Verhältnisse
stark verändern.
Abb.4.53: Satellitenbild der Schutzgebiete Garda-bani (Georgien) und Garayazi (Aserbai-dschan). In Georgien sind die Wälder wesentlich dichter, doch wurden hier die Terrassenwälder durch Äcker ver-drängt.
In Aserbaidschan sind die Wälder auf-gelichtet, oder durch Grünland ersetzt worden. Als rotbraune Flecken sind auch Äcker zu erkennen. Das Garayazi Schutzgebiet scheint stärker genutzt als das Gardabani Reservat.
(Bildgrundlage: GoogleEarth (2006))
Abb.4.54: links: Breiter, nutzenfreier Kanal mit seitlichen Erdwällen, der am Rande des Schutzgebietes den Quercus-Wald zerschneidet. (Mai 2005)
rechts: Durch Versalzung absterbender Pappelwald bei Poily, der durch Tamarix- und Elaeagnus-Gebüsche ersetzt wird. (Mai 2005)
Ergebnisse
52
4.5.2 Nutzung im Gebiet Entgegen den gesetzlichen Vorgaben ist das Schutzgebiet nicht nutzungsfrei. Wie aus den
Beschreibungen der Vegetationstypen ersichtlich, gibt es kaum einen Bereich im Gebiet, der
nicht beweidet wird. Im knapp 20 km² großen Korridor zwischen Muganli und Kura weiden
ca. 900 Büffel, 150 Kühe und 1200 Schafe. Die Besatzstärke liegt somit bei ca. 0,7 Großviehein-
heiten je ha. In Abb.4.53 ist die daraus resultierende mosaikartige Hudelandschaft im Satelli-
tenbild zu erkennen. Auf georgischer Seite ist der Wald hingegen wesentlich dichter, und
wird wahrscheinlich nicht beweidet.
Einschneidende Wirkung haben vor allem Entwässerungsgräben um Äcker im Schutzgebiet,
die besonders das Feuchtgrünland der 3. Terrasse entwässern sowie andere, oft nutzenfreie
Eingriffe (Abb.4.54). Bei Poily sterben mehrere Quadratkilometer Pappelwälder durch Ver-
salzung ab. Hier kreuzt ein 60 Jahre alter Eisenbahndamm die Aue, welcher den Abfluss von
Hochwässern verringert und den Grundwasserstrom aufstaut. Das jetzt höher anstehende
Grundwasser gelangt durch Kapillaraufstieg ganzjährig an die Oberfäche und verdunstet.
Dadurch nimmt die Salzkonzentration des Bodens zu. Hier gedeihen nur noch halophile Ar-
ten wie Tamarix und Elaeagnus. Kleinflächig treten solche Versalzungen auch im Grünland
auf den Terrassen auf.
Es gibt also eine Diskrepanz zwischen dem Ziel eines nutzungsfreien Schutzgebietes und der
Realität, da die Verwaltung nicht in der Lage ist, gesetzliche Bestimmungen durchzusetzen.
Auf Möglichkeiten, dieses Problem zu überwinden und Gefährdungen für die Wälder abzu-
schwächen, wird in Kapitel 6 eingegangen.
Diskussion
53
5 DISKUSSION
5.1 Relief und Hydrologie der Niederung Die bereits bei der Darstellung der Vegetationstypen getroffenen Überlegungen zum Wasser-
haushalt der Kura-Niederung sollen hier noch einmal unter Einbeziehung des Einzugsgebie-
tes vertiefend dargelegt werden. Es besteht kein Zweifel, dass die bis zu 100 m hohen Schot-
terterrassen nördlich der Kura (Abb.5.1) die hydrologische Situation in der Niederung stark
beeinflussen.
Laut Mamedalijew (1961) wurden die Schotterterrassen im mittleren Pleistozän abgelagert.
Später schnitt sich die Kura tiefer ein, bis neue Akkumulationsprozesse bei geringem Flussge-
fälle einsetzten und die 4. Niederterrasse aus Tonen und Lehmen im Jungpleistozän ablager-
Abb.5.2: Schematischer geologischer Querschnitt durch die Kura-Niederung bei Muganli mit Darstellung der Terrassen und vermuteten Grundwasserströme. Bildungsepochen aus Mamedaliew (1961).
Alt-pleistozän
Holozän Jungpleistozän Mittleres Pleistozän Bildungs-epoche
Steilufer Talboden mit verwildertem
Fluss
Niedere Terrassen Schotterterrasse Morphotyp
Ober-flächen-abfluss
Überflutung Quellregime Versickerung und Grundwasserneubildung
Wasser-regime
Abb.5.1: links: Blick von den nördlichen Schotterterrassen (Versickerungsgebiet) auf die 4. Niederterrasse mit Äckern. Die stark beweideten Gebüsche bestehen aus Paliurus spina-christi und Rhamnus pallasii. (Mai 2005) rechts: Ca. 30 cm hohe Quellkuppe (hinter dem Spaten) am Fuße der 4. Terrasse aus stark zersetztem Radicellentorf.
(Juni 2005)
Diskussion
54
ten. Hierfür war sicher die Einengung der Niederung bei Poily verantwortlich, in der sich ein
epigenetisches Durchbruchstal ausbildete. Dieses langsame, mehrfach stark abgeschwächte
Einschneiden des Tales führte zur Bildung der drei weiteren Terrassen. Es ist davon auszu-
gehen, dass diese Prozesse andauern und in den heutigen Talboden eine weitere Terrasse
eingeschnitten wird.
Auf den großen Schotterflächen der von Artemisia-Steppen bewachsenen Hochterrassen ver-
sickert das hauptsächlich im Frühjahr und Herbst fallende Regenwasser und bildet Grund-
wasser (Abb.5.2), das dann die auf den Niederterrassen austretenden Quellen speist. Beson-
ders am Fuße der 4. Terrasse treten zahlereiche flache Quellmoore auf (Abb.5.1). In den hei-
ßen Sommern ist die Torfabbaurate aber gegenwärtig so hoch, dass die Entstehung größerer
Quellmoore verhindert wird. Die Quellaustritte versorgen somit die Niederungswälder und
das Feuchtgrünland stetig mit Wasser, während die Auwälder vom wechselnden Wasser-
stand des Flusses abhängig sind. Entwässert werden die Terrassen durch den Garasu
(Schwarzer Fluss), welcher mit einem kontinuierlichen Abfluss von 20 m³/s (Skworzow
1976a) in die Kura mündet.
Somit spielen die hohen Schotterterrassen, welche die Kura-Niederung im Norden begleiten
als Grundwasserneubildungsareale eine entscheidende Rolle.
5.2 Die Weidelandschaft der Terrassen
5.2.1 Zur Entstehung der Weidelandschaft bei Muganli Nach Angaben älterer Bewohner frequentierten noch bis 1920 große wandernde Viehherden
die Kura-Niederung. Es existierte offenbar ein Wanderweidesystem, das sich von Höhenla-
gen des Kleinen Kaukasus (heute Armenien) als Sommerweidegebiet bis zu den nördlich der
Kura gelegenen Steppen (heute z.T. Georgien) als Frühjahrs- und Herbstweiden erstreckte.
Die Niederung selbst wurde jeweils zum Frühjahrsende durchwandert und diente vielleicht
auch als Winterweide. Diese Herden aus Tausenden von Schafen und Ziegen, sowie Kühen
sollen Großfamilien gehört haben, welche damals in Dörfern am Nordhang des Kleinen Kau-
kasus wohnten. Wasserbüffel spielten anscheinend noch keine Rolle. Die Niederung wurde
somit, anders als heute, nur periodisch beweidet. Dennoch befand sich der Wald um 1840 in
einem „schrecklichen Zustande“ (Radde 1899). In den folgenden Jahrzehnten nutzte man ihn
wieder stärker als „großfürstliche(n) Sauenstand“, also als Jagdreservat, und Radde (1899)
fand in der zweiten Hälfte des 19. Jahrhunderts wieder sichtlich erholte Wälder vor.
Diskussion
55
Mit Einstellung der Wanderweidewirtschaft entwickelten sich dann Orte wie Muganli, von
denen aus das Gebiet ganzjährig beweidet wurde, so dass die Waldlandschaft mehr und
mehr zu einer Weidelandschaft wurde. Mitte des 20. Jahrhunderts wurden dann die Genos-
senschaften gegründet und ein Teil der Viehhaltung in Ställe verlagert. Viele Offenflächen im
Wald wurden nun durch eine staatlichen Forstbetrieb (Leschose) aufgeforstet und bei Bedarf
bewässert (Alijew & Chalilov 1976). Zugleich legte man Kanäle und Gräben zur Entwässe-
rung der Terrassen an. Dieser Einschnitt in die Landschaftsgenese währte bis 1991, als sich
die Genossenschaften nach dem Zusammenbruch der Sowjetunion auflösten und jedes Mit-
glied seinen Anteil an Vieh oder Maschinen erhielt. Es setzte eine primitive, kaum regulierte
Weidewirtschaft im staatlichen Schutzgebiet ein. Heute sind alle Entwicklungsstadien einer
Hudelandschaft, die gleichzeitig die Energieversorgung sichern muss in der Niederung vor-
handen.
Ursprünglich bedeckten mehr oder weniger geschlossene Wälder, mit Quellen, Mooren und
Bächen die Terrassen. Über die Zusammensetzung dieser Wälder lassen sich heute nur Ver-
mutungen anstellen. Welche Rolle die einzelnen Baumarten spielten, dürfte neben der Was-
serversorgung der Standorte vor allem auch von den walddynamischen Prozessen abhängig
gewesen ein. Beispielsweise verjüngen sich die Eichen nur, wenn ausreichend Licht auf den
Boden gelangt, es müssen also größere Lücken entstanden sein. Nach der Besiedelung, ver-
mutlich bereits im Neolithikum, lichtete sich der Wald durch Holzeinschlag und Beweidung
auf. Die lichtliebenden Eichen erhielten eine Chance neben verbissresistenten Gehölzen wie
Crataegus, Paliurus, Rubus und Smilax. Letztere werden besonders am Dorf auch heute noch
abgebrannt (Abb.5.3), wodurch die Quercus-Wälder mit sehr wenigen Sträuchern entstehen.
In größerer Entfernung zum Dorf wird dem Gebüsch weniger stark zugesetzt, so dass dort
auf feuchteren Standorten der Carduus-Wald mit einer zu 30 % deckenden Strauchschicht
wächst. Die Krummwüchsigkeit der Bäume in diesen Wäldern ist eine Folge der Schädigung
durch das Vieh und die Schneitelwirtschaft.
Abb.5.3: links: Abbrennen von Brombeergebüsch (April 2005); rechts: typischer, täglich frequentierter Hudewald (April 2005)
Diskussion
56
Starke Beweidung verhindert dann das Aufkommen von Jungwuchs und mindert die Vitali-
tät der Bäume, so dass der Wald nun von der Triftweide verdrängt wird (Ellenberg 1996).
Dieser Prozess wird seit den 70er Jahren durch die Holländische Ulmenkrankheit (Ophiostoma
ulmi), verstärkt (Alijew & Chalilov 1976), welche schnell die schon geschwächten Bäume be-
fallen konnte. In dieser Zeit starb der Wald auf der 3. Terrasse ab, von dem nur noch einzelne
Bäume und Stümpfe zeugen (Abb.4.14). Durch den Rückgang des Waldes steigt die potentiel-
le Verdunstung (Thomasius & Schmidt 1996), so dass sich in den grundwassernahen Gleyen
höhere Salzkonzentrationen anreichern (Abb.5.5). In positiver Rückkopplung werden so wie-
derum die verbliebenen Bäume geschädigt. Weiterhin begünstigt selektive Beweidung die
Etablierung von Weideunkräutern (Nitsche 1994). Als Ergebnis entsteht der Carex otrubae-
Rasen auf feuchten, und der Convolvulus-Rasen auf trockenen Standorten. Grossheim (1948)
führt als typische Art dieser Waldersatzgesellschaften Iris carthaliniae (gehört zur Artengrup-
pe Iris spuria) an, und nennt als Wuchsorte leicht versalzte, grundwassernahe Wiesen in der
Kura-Araks Niederung.
Die für Weidelandschaften charakteristischen Kleinformen, die das Feuchtgrünland bei Mu-
ganli auszeichnen, lohnen eine nähere Betrachtung. Schlenken und Tümpel dürften samt und
sonders durch die Aktivitäten der Weidetiere entstanden sein. Im Wald existieren derartige
Hohlformen nicht. Auch eine Entwicklung aus alten Gräben wird durch die unregelmäßige
Abb.5.4: Mögliche Entstehung der Tümpel und Schlenken. Phase 1: aufgeweichter Boden durch Niederschlag und Quellwasser; Phasen 2 und 3: wiederholter Austrag von Boden an feuchten Stellen; Phase 4: Quell- und Oberflächenwasser füllen die Hohlformen
Abb.5.5: links: Fläche mit Salzanreicherung auf der 3. Terrasse (Mai 2005) rechts: Viehtrift mit typischen Riffeln und ausgetretenen Pfaden (Mai 2005)
Diskussion
57
Anordnung ausgeschlossen. Folgende Hypothese zur Entstehung erscheint daher möglich
(Abb.5.4):
1. An quelligen Stellen, besonders nach Regen, sinken die schweren Büffel und Kühe in
den Tonboden ein und zerstören so die Vegetation.
2. Ton bleibt an den Hufen der Tiere hängen und wird ausgetragen.
3. Häufige Wiederholung führt zur Bildung der Hohlformen, mit einer scharfen Kante
am Übergang zu trockeneren Bereichen.
4. Es entstehen
a. Tümpel in abgeschlossenen Lagen (Abb.4.10) mit der Zannichellia-Tauchflur, von
Büffeln als Kühlbecken genutzt, oder
b. Schlenken mit Ablauf, vom Alisma-Catabrosa-Ried oder der Catabrosa-Schlammflur
bewachsen. (Abb.4.13)
5. Hochfrequentierte Flächen und Pfade sind vegetationsfrei und tragen ein typisches
Riffelmuster senkrecht zur Triftrichtung (Abb.5.5)
5.2.2 Möglichkeiten der Regeneration der Wälder Viele Eichen-Ulmen-Niederungswälder Transkaukasiens wurden im Laufe der Zeit in Äcker
umgewandelt (Prilipko 1970), oder degradierten wie beschrieben zum Feuchtgrünland.
Grossheim (1948) und Prilipko (1970) erwähnen neben den Beständen im Schutzgebiet weite-
re Reste dieser Wälder im Alasantal, in der Karabachsteppe und bei Kuba im Nordosten des
Landes. Grossheim (1948) unterscheidet dabei eine trockene Ausprägung, die dem Quercus-
Wald entspräche und einen feuchten, dem Carduus-Wald nahestehenden Typ mit Lianen,
Brachypodium sylvaticum, Viola spp. und anderen.
Wie hoch ist nun das Regenerationspotential dieser degradierten Wälder im Gebiet?
Generell ist bei geringer Nutzungsintensität eine Regeneration zu erwarten. Mit zunemhen-
der Entfernung vom Dorf verbessern sich die Chancen der Wälder. Bei starker Beweidung
können sich Jungbäume nur im Schutze typischer pyramidenförmiger Weidebüsche entwi-
ckeln (Nitsche 1994). Im trockenen, dorfnahen Quercus-Wald werden diese abgebrannt, so
dass nur wenige Bäume jünger als 40 Jahre sind und eine altersbedingte Ausdünnung der
Bestände zu befürchten ist.
In einer anderen Situation befinden sich die Wäldern der 1. und 2. Terrasse auf Gley-Haft-
pseudogleyen, die fast nur von Büffeln und Rindern beweidet werden. Trotz einer Besatz-
stärke von 0,7 GVE / ha ist hier eine Ausdehnung von Weißdorngebüschen zu beobachten
(Abb.4.2), in deren Folge auch Ulmen und Eichen aufkommen. Einzig durch Rodung der
Sträucher könnten die Hirten diesen Prozess unterbinden. Bis zum Ulmensterben soll Ulmus
minor eine dominante Rolle gespielt haben, doch stirbt sie heute gewöhnlich in einem Alter
Diskussion
58
von 20 Jahren ab und prägt die Bestände weniger als Eiche und Weißdorn (siehe z.B.
Abb.4.23). Solange die Krankheit anhält, wird allein die Eiche die herrschenden Bäume stel-
len.
Vegetationstyp 1 2 3
Aufnahmenummer 30 7 31 32 25 6 8 34 Nutzungsintensität 3 3 2 2 2 2 1 2 Deckung Gehölze [%] 0 0 50 70 60 80 80 90 Deckung Lianen [%] 5 5 10 5 60 Höhe Krautschicht [cm] 10 10 20 20 20 40 30 40 Deckung Krautschicht [%] 70 50 50 40 30 40 40 10 Artenzahl 28 27 48 44 58 48 47 43
Rasenarten Sherardia arvensis 1 + Euphorbia helioscopa 1 + + Poa pratensis 1 1 1 Convolvulus lineatus 2 2 1 Trifolium dubium 1 1 1 + Galium parisiense 1 + 1 + +
Offenlandarten Festuca arundinacea 1 + + 1 1 Eryngium campestre 1 1 1 + 1 + Ranunculus bulbosus 1 + 1 1 + + + Poa angustifolia 1 1 1 1 + + + Potentilla reptans 1 1 1 2 1 1 1 Elytrigia repens 1 + 1 1 1 1 +
Lägerarten Centaurea calcitrapa + 1 1 + Cirsium arvensis + + 1 + Geranium pusillum 1 + + Plantago major + + + Carduus crispus + + + + + Arctium tomentosum + +
Gehölze Crataegus riphidophylla 3 4 3 2 2 2 Prunus spinosa 1 1 1 2 1 1 Pyrus sp. 1 1 1 1 2 Ulmus minor 2 2 2 1 1 Cornus sanguinea 1 1 1 Ligustrum vulgare 1 1 1 Quercus robur 1 1 3 4
Waldarten Viola spp. + 1 1 1 1 Geum urbanum + 1 + 2 + Brachypodium sylvaticum + 1 1 + 1 + Vincetoxicum scandens + + Festuca gigantea + + + Physalis algekengi 1 1 +
Lianen Smilax excelsa 1 1 1 1 3 Periploca graeca 1 1 2 1 2 Humulus lupulus 1 Vitis vinifera 1
Anhand von Vegetationsaufnahmen (Tab.5.1) der 1. Terrasse wird die Sukzession auf weni-
ger beweideten Standorten dargestellt:
1. Ausgangspunkt ist hier der sehr niedrige Convolvulus-Rasen (Abb.4.16) mit bewei-
dungstoleranten Arten wie Convolvulus lineatus, Eryngium campestre und Ranunculus
bulbosus.
2. Von den Rändern dringen Crataegus rhipidophylla, Prunus spinosa und Pyrus sp. in die
Flächen ein, in deren Schutz auch Lianen, Eichensämlinge und Wurzelbrut von Ulmus
minor aufwachsen. Durch Beschattung und Abdeckung mit Falllaub gehen die Rasen-
arten zurück, und Waldarten (z.B.: Viola spp., Geum urbanum, Brachypodium sylvaticum)
kommen zur Geltung. Entlang von Viehpfaden wachsen Lägerarten wie Carduus
crispus, Geranium pusillum und Plantago major - der Carduus-Wald etabliert sich.
Tab. 5.1: Sukzession vom Convolvulus-Rasen zum Alliaria-Wald auf der 1. Terrasse.
Legende zur Tabelle: Vegetationstypen: 1 Convolulus-Rasen 2 Carduus-Wald 3 Alliaria-Wald Deckungsgrade in der Braun-Blanquet-Skala
Diskussion
59
3. Eichen, Ulmen und Weißdorn bilden jetzt mit Vitis vinifera und anderen Lianen einen
geschlossenen Schirm aus, so dass in der Feldschicht nur noch schattentolerante Arten
überleben. Diese seltenen Bestände sind dem Alliaria-Wald zuzurechnen.
Aliyew & Chalilov (1976) kartierten die Waldbestände entlang der Kura für forstliche Zwe-
cke, und lieferten so eine Grundlage für die Abschätzung der Waldentwicklung in den letz-
ten 30 Jahren. Folgende Umstände werden aus dieser Karte (Abb.5.6) ersichtlich:
1. Unterhalb Muganlis erstreckte sich das Grünland in der Aue bis zum Fluss.
2. Aufforstungen fanden auf Blößen im Auwald und als Ergänzung der Eichen-
Ulmenwälder statt.
3. Auf der 4. Terrasse, südlich Muganlis, bedeckte der Quercus-Wald noch 50 % der Flä-
chen.
4. Äcker gab es nur bei Muganli und Garayazi.
Folgende Veränderungen sind heute im Vergleich zu damals in der Landschaft zu erkennen:
1. Grünland wurde stellenweise durch den Auwald verdrängt.
2. Im Auwald gibt es auf den alten Forstflächen Lichtungen, die langsam von Sträuchern
erobert werden.
3. Die dorffernen Eichen-Ulmenwälder konnten sich auf Kosten des Grünlandes aus-
dehnen.
4. Die Bestände des Quercus-Waldes der 4. Terrasse haben sich ungefähr halbiert, bzw.
bestehen nur noch aus Solitärbäumen.
5. Äcker finden sich jetzt auch auf der 2. und 3. Terrasse bei Muganli.
Abb.5.6: Schematische Karte der Vegetation entlang der Kura (bearbeiteter Ausschnitt aus Aliyew & Chalilov (1976).
Diskussion
60
Aus der unterschiedlichen Entwicklung dorfnaher und dorfferner Wälder lassen sich folgen-
de Schlüsse ziehen:
1. Unter den rezenten Weidebedingungen mit Büffeln und Rindern werden die dorffer-
nen Wälder nicht zurückgedrängt. Dies ist zum einem auf das nichtselektive Grasen
der Rinder (Pykälä 2003) und zum anderen auf die gute Wüchsigkeit dorniger und
giftiger Gehölze (Smilax, Crataegus, etc.) zurückzuführen. Durch das Vieh wird die
Struktur- und Artenvielfalt erhöht (Weibull et al. 2003), ein Zustand, der einer ur-
sprünglichen Naturlandschaft mit Großsäugern wie Rothirsch und Wisenten ähneln
soll (Bunzel-Drüke et al. 1999).
2. Ungezäunte Aufforstungen tragen nicht zur Waldmehrung bei.
3. Äußerst gefährdet sind die dorfnahen Bestände, also ein Großteil der schon stark ge-
schrumpften Eichen–Ulmen-Niederungswälder. Feuerholzwerbung, gekoppelt mit
Beweidung durch unterschiedlichste Tierarten (Ziegen, Schafe, Pferde, Rinder, Geflü-
gel) stabilisiert hier das Offenland (vgl. Schley & Leytem 2004). Um diese Wälder zu
erhalten sind also strikte Nutzungsbeschränkungen nötig.
Eine Erholung des Waldes durch Eliminierung der Nutzung führte schon einmal nach 1840
zum Erfolg (Radde 1899), und würde heute sicher ähnlich ablaufen.
5.3 Dynamik der Vegetation in der Aue In der Aue unterliegen die Standorte durch Flussbettverlagerung und Sedimentation bei
Hochwasser einer hohen Dynamik, in deren Folge immer wieder Neuland entsteht und alte
Ufer abgetragen werden (Abb.5.7). In Kapitel 1.3 wurden die von dieser Dynamik abhängi-
gen Vegetationstypen mit ihren Standorten beschrieben. Nun soll mit Hilfe der ermittelten
Bestandesdaten (Abb.5.8) der Versuch unternommen werden, sie miteinander räumlich und
zeitlich in Beziehung zu setzen (Abb.5.10). Um die Veränderung der Gehölzzusammenset-
zung im Laufe der Zeit zu verstehen, sind die Vermehrungsstrategien und Standortsansprü-
che der Arten im Gebiet zu beachten (Tab.5.2).
Viele Vegetationstypen in Auen lassen sich in eine Sukzessionsfolge einordnen, sofern sie auf
ähnlichen Substraten stehen. Dennoch ist die Schlussfolgerung aus einem räumlichen Neben-
einander auf Sukzessionsabläufe mit Vorsicht zu betrachten (Mayer 1986; Ellenberg 1996). Im
Allgemeinen entwickeln sich in der gemäßigten Zone Auen von offenen Kies- und Sandbän-
ke über Weichholzauen aus Salix und Populus zu Hartholzauen mit Quercus und Ulmus (Wal-
ter 1968). Eine Sonderstellung nehmen Erlenbruchwälder auf dauerhaft feuchten und wenig
gestörten Standorten ein. Diese Grobeinteilung ist auch am Kura Mittellauf nachvollziehbar,
wo selbst die Erlenwälder auf Sonderstandorten anzutreffen sind.
Diskussion
61
Typen Vertreter im Gebiet Strategien und Ansprüche Aussage über Bestandesalter
Kurzlebige Sträucher
Salix triandra Tamarix spp.
Keimen nur auf jungen Sand- und Kiesbänken und verschwinden bei Beschattung. Vermehrung über Wurzelbrut nur sehr selten.
Junge Bestände
Konkurrenzstarke Weichholzbäume
Populus x canescens Populus nigra Salix alba
Schnelles Höhenwachstum verhindert Unterdrü-ckung durch Lianen etc.. In alten Beständen keine Vermehrung. Wurzelbrut von P. x canescens stirbt im Schat-ten ab.
Standorte sind in etwa so alt wie die Bäume.
Lianen Clematis vitalba Hedera helix Periploca graeca Smilax excelsa Vitis vinifera
Keimen im Halbschatten. Ranken schnell an Bäumen empor und können diese unterdrücken. Existieren nach Zusammenbruch von Bäumen weiter.
Bestände älter als ca. 10 Jahre
Edellaubhölzer Acer campestre Carpinus betulus Quercus robur Tilia begoniifolia Ulmus minor
Keimen im Schutze der Pappelwälder und füllen Baumsturzlücken aus. Ulmus minor kann sich durch Wurzelbrut aus-breiten. In zu dichten Beständen kann sich Quercus-Jungwuchs nicht mehr etablieren.
ältere Standorte, Harthölzer sind jünger als die Weichhölzer und lösen diese ab.
Dornige oder giftige Sträucher
Crataegus rhipidophylla und weitere Rosaceae Elaeagnus caspica Euonymus europaeus Ligustrum vulgare
Gleiche Keimungsbedingungen wie vorherge-hende. Sind oft trockenheitsresistent und werden vom Vieh verschmäht. Können sich auf Lichtungen behaupten.
Wie vorhergehende, zeigen aber Beweidung an. Zumeist in Degradations-stadien der Wälder.
Der wichtigste Faktor im Ökosystem Aue ist die Flussdynamik (Schnitzler 1997). Einerseits
entsteht durch sie zu besiedelndes Neuland, andererseits können große Hochwässer alte
Wälder komplett abtragen und damit die Sukzession abrupt beenden (Abb.5.7). Sehr bedeu-
tend ist auch die jährliche Sedimentation von Schluffen und Sanden in den Auwäldern. Nach
Hochwässern fließt das Wasser binnen weniger Tage aus der Aue ab, so dass die Gehölze nur
kurzeitig dem Stress der Überflutung ausgesetzt sind.
Zu Beginn der Sukzession stehen also die Neulandbildungen, welche erst von Ephemeren
und dann von der Tamarix-Weichholzaue besiedelt werden. Bei geringer Störung dauert
dieses Stadium nur zehn Jahre bis sich die Populus-Weicholzaue einstellt. Auf kiesigen und
sandigen Substraten wird Populus nigra vorherrschend, wohingegen die häufigere
Populus x canescens meist auf Schluffen anzutreffen ist. In diesen Beständen dominieren die
Weichhölzer mit I = 300 absolut (Abb.5.8), wobei die Stammzahl in den ersten 20 Jahren unter
400 Stämme je ha absinkt. Damit sind die Bestände aber noch doppelt so dicht bestockt wie
Pappelforsten Mitteleuropas gleichen Alters (Schober 1995). Das Stadium der Weichholzaue
dauert ca. 25 Jahre und ist damit kürzer als in anderen Regionen Europas (Mayer 1986).
Tab. 5.2: Strategien und Standortsansprüche ausgewählter Gehölzarten und daraus ableitbare Aussagen
Abb.5.7: Reslutate eines Hochwassers: links: Junge Sedimentschicht; rechts: Abgespülte Graupappel (Mai 2005)
Diskussion
62
Durch gegenseitige Beschattung werden die Pappeln weiter selektiert, Hochwässer lagern
fruchtbares Feinsubstrat ab und das Bestandesklima wird ausgeglichener. In der Krautschicht
verdrängen schattentolerante Arten die Besiedlungspioniere. Die Harthölzer Quercus, Ulmus
sowie Wildobst stellen sich ein und begründen auf schluffigen Standorten den Vincetoxicum-
Wald. Dieser ähnelt den südmitteleuropäischen Eichen-Ulmen Auwäldern, deren Charakter-
art auch Populus x canescens ist (Seibert 1987). Mit 79 m²/ha Grundfläche, 560 Bäumen je ha
und 27 Gehölzarten ist dieser im Vergleich zu anderen Auwäldern der temperaten Zone
(Brinson & Verhoeven 1999) artenreicher und hat bei unterdurchschnittlicher Stammzahl eine
sehr große Bestandesgrundfläche, was auf die mächtigen Graupappelbäume zurückzuführen
ist. In diesem Stadium gewinnt das Wildobst, besonders Crataegus, in der Strauch- und zwei-
ten Baumschicht an Bedeutung und prägt mit I=108 die Bestände mehr als die Pappeln
(I=101). Diese Dominanz ist mit Sicherheit auf die Waldweide zurückzuführen. Ähnliche
Verhältnisse wurden auch in beweideten Auwäldern Bulgariens (Stojanoff 1926) und in ehe-
maligen Mittelwäldern am Oberrhein (Dister 1985) beobachtet. Dister meint aber, dass Euo-
nymus, Cornus und Crataegus durch zu hohe Wildbestände verdrängt werden, was an der
Kura selbst unter hohem Weidedruck nicht nachvollziehbar ist.
Selten ist der Tilia-Wald als nächstes Entwicklungsstadium anzutreffen. Hier wachsen nur
noch 33 Pappeln je ha, die mindestens 40 Jahre alt sind und einen Brusthöhendurchmesser
von ca. 1 m aufweisen. Die Eichen sind zwar jünger als die Pappeln, doch fehlen unter 30
Jahre alte Bäume, was auf die Beschattung durch Lianen, Linden und Hainbuchen zurückge-
führt werden kann. Mögliche Gründe für die Seltenheit dieser Wälder sind:
1. Das Vieh verhindert den Aufwuchs junger Linden und Hainbuchen.
(Stojanoff (1926) fand in beweideten Auwäldern Bulgariens auch keine Linden).
2. Linden werden bevorzugt gefällt. (Jeder zweite Stamm war abgesägt.)
3. In zu lichten Beständen vertrocknen die anspruchsvollen Jungpflanzen der Laubhöl-
zer im Sommer.
4. Hochwässer im Mai und Juni bewirken kurzzeitig anoxische Bedingungen, wodurch
Linden und Hainbuchen während ihrer intensivsten Wachstumsphase geschädigt
werden (vergl. Schnitzler (1997)).
Auf grundwassernahen Standorten kann der Vincetoxicum-Wald von der Periploca-Lichtung
abgelöst werden. Diese Ablösung lässt sich in folgenden drei Schritten skizzieren (Abb.5.9):
1. Schon in geschlossenen Baumbeständen bringen Smilax und Periploca die Bäume und
Sträucher im Unterstand durch Beschattung zum Absterben.
2. Pappelüberhalter sterben altersbedingt ab, und deren Stümpfe dienen als Gerüst für
die Lianen. (siehe Abb.4.38 rechts)
Diskussion
63
1218510 874163840N =
Origanum - W
ald
Alliaria - Wald
Tilia - Wald
Vincetoxicum - W
ald
Populus - Wha
Tamarix - W
ha
Alter
in J
ahre
n
100
80
60
40
20
0
Populus
Quercus
0
20
40
60
80
Populus -Gebüsch inTamarix -
Weichholzaue
Populus -Weichholzaue
Vincetoxicum -Wald
Tilia - Wald Alliaria - Wald Origanum - Wald
Gru
ndfläc
he
(m²/
ha)
gesamt Pappeln Ulme/EicheWildobst Sonstige
3
0
50
100
150
200
250
300
350
400
450
Populus -Weichholzaue
Vincetoxicum - Wald Tilia - Wald Alliaria - Wald Origanum - Wald
Dic
hte
(Bäu
me
je H
ekta
r)
Weichhölzer Ulme Eiche Wildobst Sonstige2
4
Abb.5.8: Kennzahlen der Auwälder. 1 Wichtigkeit (I) 2 Bestandesdichte in Bäumen je ha 3 Grundflächen der Bestände und
Gehölzartengruppen 4 Alter der Pappeln und Eichen (Boxplot mit 25-75% Quantilen ; Wha = Weichholzaue)
0
50
100
150
200
250
300
Populus -Weichholzaue
Vincetoxicum - Wald Tilia - Wald Alliaria - Wald Origanum - Wald
Wic
htigke
it (
I)
Weichhölzer Ulme/Eiche Wildobst Sonstige1
Diskussion
64
3. Alle Bäume sind abgestorben und die Lianen bilden ein eigenes Gerüst, wodurch sie
die Fläche mit einer 2 m hohen Decke überziehen, welche das Wachstum von Kräu-
tern und Gehölzen einschränkt oder ganz unterbindet.
Ähnliche Lichtungen aus Smilax erwähnt Stojanoff (1926) aus Bulgarien und Schnitzler (1997)
beschreibt Lücken in Wäldern der Rheinaue, auf denen Clematis vitalba und Vitis vinifera den
Aufwuchs von Bäumen verlangsamen. Diese Lianen bilden an der Kura aber keine Domi-
nanzbestände. Ob die Periploca-Lichtung wieder von Wäldern abgelöst wird, oder ein sehr
langandauerndes Stadium darstellt, konnte nicht geklärt werden.
Auf trockeneren Standorten bildet bei wachsendem Weidedruck der Alliaria-Wald das Fol-
gestadium des Vincetoxicum-Waldes. Als Weidezeiger tritt z.B. Cynoglossum germanicum auf.
Hinzukommt das Ausscheiden der hohen breitkronigen Pappeln. Die Grundfläche der Be-
stände nimmt ab (74 m²/ha) und die Standorte werden lichter und trockener.
Diese Abfolge ist anhand der ermittelten Zahlen für die Pappeln ableitbar (Abb.5.8) Die
Wichtigkeit der Pappel fällt auf 51 unter die von Eiche und Ulme (I=89), da auch Wurzelbrut
der Pappel sich nicht behaupten kann. Altersbedingtes Absterben reduziert die Pappeldichte
unter 50 Stück je ha, wohingegen jetzt 116 durchschnittlich 32 Jahre alte Eichen je ha stocken.
Die Bedeutung von Wildobst steigt über I=100. Auffallend ist die Altersverteilung der Eichen:
Unter 17jährige Bäume fehlen und 50 % der Bäume sind zwischen ca. 22 und 40 Jahren alt.
In der topographischen Karte von 1976 (Skworzow 1976b) waren die Wälder von großen
Lichtungen durchzogen. Entweder konnte die Lichtbaumart sich damals natürlich ansiedeln,
oder es sind Reste alter Anpflanzungen, deren Ursprung heute im Gelände nicht mehr sicht-
bar ist. Neben Robinia, Diospyrus und Populus x canadensis (Alijew & Chalilov 1976) wurden
eventuell um 1970 auch Eichen eingebracht. Heute fehlt Eichenjungwuchs sowohl im Vinceto-
xicum- als auch im Alliaria-Wald. In anderen dichten Auwäldern scheint die Vermehrung der
Eiche ohne Auflichtungen auch nicht mehr möglich (Kühne 2004).
Abb.5.9: Entstehung einer Periploca-Lichtung: 1. Alter Vincetoxicum-Wald. 2. Vincetoxicum-Wald in der Zerfallsphase, die Lianen überziehen die Fläche. 3. Die Lianen bilden ein eigenes Gerüst und bedecken die Fläche komplett – Bäume und Sträucher werden unterdrückt.
Diskussion
65
Wenn Flächen des Auwaldes über längere Zeiträume vom Vieh als Ruheplätze genutzt wer-
den stellen sich Nitrophyten ein. Bäume und Sträucher werden beschädigt, so dass die Be-
stände sich auflichten (280 Bäume je ha). Auf diesen bis 0,5 ha großen Flächen wächst dann
der Carduus-Wald. Nach einem Ausbleiben des Viehs würde sich sicher wieder die Kraut-
schicht des Alliaria-Waldes einfinden.
Flächiges Absterben der Ulmen und die Entnahme von Bäumen, gekoppelt mit Beweidung
führen zu den Verbascum-Lichtungen. Solche Bedingungen wurden auch durch Anlage der
Plantagen geschaffen. Heute sind die Lichtungen fast nur noch auf kiesig-sandigen Standor-
ten anzutreffen, doch würden sich auf Schluffen sicher ähnliche Gesellschaften einstellen.
Durch besseres Wasserhaltevermögen des Bodens drangen jedoch schon hohe Gebüsche vor.
Auf höheren Kies- und Sandbänken verläuft die Sukzession etwas anders, da hier die was-
serhaltenden Schluff- und Tonlagen nur sehr geringmächtig ausgeprägt sind. Auf die Popu-
lus-Weichholzaue mit Dominanz der Schwarzpappel folgt hier der Origanum-Wald, dem alle
älteren Wälder auf sandig-kiesigem Subtrat zuzuordnen sind. Nur auf jungen Standorten
wachsen noch Pappeln, die aber durch die Trockenheit meist schon stark geschwächt sind
und zusammenbrechen. Die große Altersspanne des Waldes zeigt sich besonders in der Al-
tersverteilung der Eiche. Jungpflanzen unter Pappeln als auch alte Hudebäume sind in die-
sem Vegetationstyp zu finden. Diese Wälder sind wohl die einzigen Flächen mit erfolgreicher
Eichennaturverjüngung. Deutlich prägt die Beweidung das Bild, indem Wildobst hier zur
Dominanz (I=147) gelangt und auch in der Krautschicht viele vom Vieh geschmähte Arten
(z.B.: Polygala anatolica, Orchis militaris, Equisetum variegatum) wachsen. Dabei unterscheidet
sich die Krautschicht in jungen und alten Beständen kaum.
Kiesbänke
Tamarix-Weichholzaue
Populus-Weichholzaue P. nigra P. x canescens
Verbascum-Lichtung
Origanum-Wald
Tilia-Wald
Periploca-Lichtung
Alliaria-Wald
Vincetoxicum-Wald
Carduus-Wald
Sand - Kies Schluff - Ton
Abb.5.10: Sukzessionsschema der Auenwälder
Diskussion
66
Bei Auflichtung der Bestände durch Holzentnahme entstehen auch hier Verbascum-
Lichtungen. Ähnliche artenreiche Lichtungen sind aus der Donauaue unter der Bezeichnung
„Heißlände“ bekannt (Ellenberg 1996). Momentan dringen auf den Verbascum-Lichtungen
trotz des Viehbesatzes von 0,7 GVE/ha Weißdorngebüsche vor und leiten, ähnlich wie auf der
1. Terrasse die Entwicklung von Wäldern ein (Kap. 5.2.2). Die Beweidung verzögert diesen
Prozess nur. Eine dauerhafte Offenhaltung dieser Flächen wäre einzig durch ständiges auf
Stock setzten und evtl. Abbrennen der Gebüsche gewährleistet. Zwar verändert das Vieh die
Struktur und Artenzusammensetzung des Auwaldes, doch es verdrängt ihn unter heutigen
Bedingungen nicht.
5.3.1 Die Rolle der nichteinheimischen Gehölzarten
Im Schutzgebiet sind durch Pflanzungen und über Vertriftung im Fluss nichteinheimische
Gehölzarten eingeführt worden. Viele dieser Arten finden hier nur sehr ungünstige Bedin-
gungen vor und sind dem Konkurrenzdruck der autochtonen Gehölze unterlegen. Diese Ar-
ten sind in Tab.5.3 aufgeführt. Entlang der Gewässer gelingt es aber der aus Amerika einge-
schleppten Amorpha fruticosa stellenweise Gebüsche auf feuchten Standorten zu bilden. Spo-
radisch tritt auch Acer negundo am Flussufer auf, gelangt aber nie zur Dominanz. Eine größere
Rolle spielt der Maulbeerbaum. Er hat sich hier zu einer Begleitart der Auwälder auf feuchte-
ren Standorten entwickelt. Seine Früchte reifen bereits Ende Mai und werden von vielen Tie-
ren, darunter Wildschweinen und Schwärmen von Rosenstaren bevorzugt gefressen. In den
Beständen spielt Morus quantitativ keine Rolle. Mit einer Ausbreitung ist nicht zu rechnen.
Am Auffälligsten sind die beiden Fabaceen Robinia und Gleditsia. Als dornige Lichtbaumarten
werden sie durch die Beweidung begünstigt und erreichen die höchsten Anteile dementspre-
chend in degradierten Beständen. Oft gelingt es den Jungpflanzen aber nicht, sich im Schatten
der Pappeln und Eichen zu entwickeln.
Es ist nicht zu erwarten, dass die Neophyten die Auwälder grundlegend verändern. Viel-
mehr ist ein Einnischen zu beobachten. Auf Dauer werden diese Gehölze nur eine randliche
Rolle in den Wäldern spielen. Naturschutzfachlich ergibt sich kein Grund irgendwelche
Maßnahmen gegen diese Arten einzuleiten. Falls die Holzentnahme aus diesem Gebiet un-
umgänglich ist, sollten freilich zuerst diese Arten entnommen werden.
Eingeführte Arten ohne Reproduktion Eingeführte Arten mit Reproduktion
Diospyros lotus
Juglans regia; Morus nigra
Parrotia persica
Populus nigra var. italica
Populus x canadensis
Quercus castaneifolia
Prunus armeniaca, P. avium
Amorpha fruticosa
Acer negundo
Gleditsia caspica
Robinia pseudoacacia
Morus alba
Tab.5.3: In das Schutzgebiet neu eingeführte Gehölzarten
Diskussion
67
5.4 Die Kura-Niederung ohne Nutzung Bisher wurde die reale Vegetation beschrieben, ihre Standortsansprüche dargelegt und Ent-
wicklungen aufgezeigt. Wie würde sich aber die Vegetation bei völliger Einstellung der Nut-
zung verändern? Die Konstruktion solcher potentieller Szenarien weist immer große Un-
schärfen auf, da die Wechselwirkungen zwischen einzelnen Standortfaktoren bei Verände-
rung der Landnutzung sehr vielfältig und schwer vorherzusagen sind (Scherzinger 1996).
Solche Szenarien sind jedoch geeignet tatsächliche oder vermutete landschaftsökologische
Zusammenhänge zu verdeutlichen. Sie sind mindestens als Arbeitshypothesen wertvoll. Eine
solche Hypothese ist die folgende Darstellung (Abb.5.11).
Ohne Nutzung wäre die Kura-Niederung von mehr oder weniger geschlossenen Wäldern
bestanden, in denen ein ausgeglicheneres Mikroklima herrschen würde als heute. Rotwild
und Wildschweine wären die wichtigsten Pflanzenfresser, sie würden aber nicht die Wirkung
des heutigen hohen Viehbestandes substituieren. Weiterhin ist damit zu rechnen, dass die
Höhe des Jahresniederschlages sich aufgrund der höheren Transpirationsleistung des Waldes
positiv verändern würde.
Weichholzaue:
Das Bild wäre dem jetzigen ähnlich, da die Flussdynamik auch heute noch weitgehend unge-
stört abläuft. Nur verblieben größere Mengen Treibholz im Flussbett und die Tamarix-
Gebüsche sowie die Weichholzwälder wären ohne Beweidung dichter.
Hartholzaue:
Der Auwald ähnelte dem heutigen Vincetoxicum-Wald. In älteren Stadien würden Linden und
Hainbuchen eine größere Rolle spielen. Ob Ulmen dominieren würden, ist aufgrund der Hol-
ländischen Ulmenkrankheit fraglich (Dister 1985). Eichen und Weißdorne würden weitgehen
fehlen.
Gebüsche Dichter Auwald Feuchte Niederungswälder und Moore
Trockene Niederungswälder
Trockengebüsche Steppe Vegetation ohne
Nutzung
Abb.5.11: Hypothetische Darstellung der Vegetation der Kura-Niederung nach Einstellung aller Landnutzungen.
Diskussion
68
1. bis 3.Terrasse:
Der lianenreiche mesophile Laubwald ähnelte dem Hartholzauenwald, worauf schon jetzt
ablaufende Sukzessionen hinweisen (Tab.5.1). An Quellen und Schlenken könnten evtl. Er-
lenwälder wachsen. Die Moorfläche nähme evtl. ab und aufgrund der stärkeren Bodenbe-
schattung würd die Versalzung auf heute offenen Standorten gestoppt.
4. Terrasse:
Sommertrockenheit limitiert die Ausbreitung vieler Laubgehölze. Trockene Eichen-Ulmen-
wälder mit einer Strauchschicht aus Rhamnus, Crataegus, Paliurus, und Mespilus, wie sie aus
der Karabach-Region beschrieben werden (Prilipko 1970), könnten mindestens bis an den Fuß
der Schotterterrassen wachsen.
Schotterterrassen:
Die Südhänge der Schotterterrassen sind heute von Erosionsrinnen zerfurcht, die auf einen
starken Oberflächenabfluss hinweisen. In diesen Hangrunzen kann wenigstens mit geschlos-
senen Gebüschen aus Paliurus spina-christi gerechnet werden. Gulisaschvili et al. (1975) neh-
men an, dass die heutigen Schibljak-Gebüsche aus lichten Pistacia mutica-Wäldern hervorgin-
gen, die z.T. noch heute anzutreffen sind (Abb.2.4). Stellenweise treten an den Hängen deut-
lich sichtbar kleine Quellen aus, die auch Eichenwälder mit Wasser versorgen könnten. Auf
den Hangschultern dürften sich anstelle der kurzrasigen Artemisia-Steppen Federgrassteppen
ausbreiten. Die potentiell natürliche untere Grenze der Eichen-Hainbuchenwälder wird am
Mittellauf bei 600 m NN (Gulisaschvili et al. 1976), bei 500 m NN (Henning 1972) oder sogar
bei nur 400 m NN (Prilipko 1954) vermutet. Somit würde sich nur ein schmaler Steppenstrei-
fen an den Hängen der Niederung zwischen den zonalen und azonalen Wäldern entlangzie-
hen.
Steilufer im Süden:
Hier wächst heute ein Reinbestand des giftigen Peganum harmala als Resultat starker Bewei-
dung (Titelfoto oben). Bei ausbleibender Nutzung ist auch mit Gebüschen zu rechnen.
Das aktuelle Bild, ein Auwald inmitten kurzrasiger Artemisia-Steppe, entspricht demnach
nicht den natürlichen Verhältnissen. Vielmehr müsste die Region als Grenze einer Laubwald-
zone betrachtet werden, welche vom Großen Kaukasus über die Kolchis-Niederung zum
Kleinen Kaukasus hufeisenförmig das aserbaidschanische Tiefland umschließt (Grossheim
1936). So erreicht beispielsweise Tilia begoniifolia als Art der mesophilen Laubwälder in der
Aue bei Muganli ihre östliche Grenze in der Kura-Niederung (Grossheim 1962). Schon Radde
(1899) bemerkte, dass Wälder in diesem Raum durch Übernutzung in Schibljak und Steppen
umgewandelt wurden.
Diskussion
69
5.5 Vergleich mit anderen Auwäldern
5.5.1 Tugai-Wälder am Kura-Mittellauf? Die Auwälder im Tiefland Aserbaidschans werden von vielen Autoren als „Tugai“ bezeich-
net (Rubner & Reinhold 1953; Alijew & Chalilov 1976; Prilipko 1954; Prilipko 1970; Grossheim
1948), ohne dass diese den Begriff näher charakterisieren. Togai, Tokai und Tugay (Thevs
2005) sind weniger gebräuchliche Bezeichnungen, auch „Tugai-Vegetation“ und „Tugai-
Wald“ wird benutzt. Was verbirgt sich dahinter, und ist diese Einordnung für die untersuch-
ten Wälder begründet?
Der Begriff „Tugai“ hat seine Ursprung in den Turksprachen und steht für Auenvegetation
arider Gebieten (vgl. Thevs 2005). Die Verbreitung der Tugai-Vegetation wird von Walter
(1968), Korowin (1961) und Tian (1991) geographisch auf Mittel- und Zentralasien beschränkt.
Im weiteren Sinne werden darunter Pappelwälder, Tamarix- und Elaeagnus-Gebüsche sowie
Grasfluren aus Phragmites australis und Calamagrostis spp. verstanden, wobei die Keimung
aller Pflanzen nur nach Hochwässern an Spülsäumen von Flüssen stattfindet und die weitere
Vermehrung vegetativ erfolgt (Korowin 1961; Treshkin 2001). Wenn sich der Fluss verlagert,
sinkt der Grundwasserspiegel und die Tugai-Vegetation degradiert aufgrund des Trocken-
stresses zu Steppen und Wüsten. Die Regeneration ist von Überflutungen abhängig (Treshkin
2001).
Im engeren Sinne bestehen Tugai-Wälder aus Pappeln der Sektion Turanga (Populus euphrati-
ca, P. pruinosa), Tamarisken und Ölweiden (Tian 1991; Thevs 2005).
Nur in der aserbaidschanischen Literatur (z.B. Prilipko 1970) werden zusätzlich Eichen-
Ulmenwälder den Tugai-Wäldern zugerechnet, obwohl hier die meisten Arten nicht auf eine
Keimung am Flussufer angewiesen sind und die natürliche Entwicklung nicht in Steppen
oder Wüstenformationen endet. Nur die Tamarix-Weichholzaue auf den Extremstandorten im
Flusslauf trägt Züge des mittelasiatischen Tugai-Waldes, aber die Wälder auf den Terrassen
sind nicht einmal Auwälder. Erst die Auwaldreste im ariden Osten der Kura-Niederung (Ali-
jew & Chalilov 1976) entsprechen Tugai-Wäldern im weiteren Sinne. Diesen Umstand be-
rücksichtigen als einzige Gulisaschvilli et al. (1976) und sprechen schlicht von Niederungs-
wäldern.
Um Irritationen und falsche Assoziationen zu vermeiden, sollte der Begriff Tugai für die
Wälder im Garayazi Schutzgebiet nicht verwendet werden. Die Bezeichnung als Auen- und
Niederungswälder ist exakter.
Diskussion
70
5.5.2 Vergleich mit anderen Auwäldern Eurasiens Aus sehr vielen Auwäldern Europas und Asiens existieren umfangreiche Vegetationsauf-
nahmen und Beschreibungen, so dass eine grobe Einordnung der Kura-Wälder möglich ist.
Referenzaufnahmen vom kühl-gemäßigten Mitteleuropa (Jäger 2004; Seibert 1987; Dister
1985; Reichhoff et al. 2004) über die subhumide Schwarzmeerküste (Stojanoff 1926), das aride
Mittelasien (Treshkin 2001; Korowin 1961) bis in die Vollwüste Taklamakan (eigene Aufnah-
men von 2004) wurden dafür einbezogen (Abb.5.12).
Der Vergleich (Tab.5.4) soll anhand des Vorkommens von Gehölzarten und -gattungen in den
Auen geführt werden, wobei Stetigkeiten und Deckungsgrade unberücksichtigt bleiben. Die
Auenwälder am Kura-Mittellauf ähneln in hohem Maße denen der temperaten und subtem-
peraten Zone Europas. Sie tragen sowohl in der Weichholzaue mit Populus nigra und Salix
alba, als auch in der Hartholzaue mit Quercus robur, Ulmus minor und strauchigen Rosaceen
deren typische Artengarnitur. Durch das Fehlen oder die Seltenheit von feuchtigkeitslieben-
den Arten wie Prunus padus und Viburnum opulus sowie Fraxinus excelsior und Frangula alnus
Fluss Mittelelbe Oberrhein Kamtschija mittlere Kura Amu Darya Tarim
Staat Deutschland Deutschland Bulgarien Aserbaidschan Usbekistan Xinjiang/China Breitengrad (° Nord) 52 49 43 41,5 43 41 Längengrad (° Ost) 12 8,5 27,5 45 59 83 Autor Jäger;
Reichhoff (2004)Dister (1985) Seibert (1987)
Stojanoff (1926)
eigene Aufnah-men (2005)
Treshkin (2001) Korowin (1961)
eigene Aufnah-men (2004)
Jahresniederschlag [mm] 564 770 471 395 106 34 Jahresdurchschnittstemperatur [°C] 8,7 10,3 12,1 13,2 10,6 12,3 Prunus padus X X Sambucus nigra X X X Viburnum opulus X X X Acer campestre X X X X Carpinus betulus X X X X Cornus sanguinea X X X X Corylus X X X X Crataegus X X X X Euonymus europaeus X X X X Frangula alnus X X X X Fraxinus excelsior X X X X Malus X X X X Populus nigra X X X X Prunus spinosa X X X X Pyrus X X X X Quercus robur X X X X Salix alba X X X X Salix triandra X X X Tilia X X X Ulmus minor X X X X Populus alba X X Clematis vitalba X X X Hedera helix X X X Ligustrum vulgare X X X Populus x canescens X X X Rhamnus cathartica X X Vitis vinifera X X X Cornus mas X X Paliurus spina-christi X X Periploca graeca X X Smilax excelsa X X Cynanchum acutum X X X X Tamarix X X X Elaeagnus X X X Halimodendron halodendron X X Lycium ruthenicum X X Populus euphratica X X
Tab.5.4: Vergleich eurasischer Auwälder anhand des Vorkommens verschiedener Gehölze. (Klimadaten nach Mühr 2005)
Diskussion
71
wird aber schon der Einfluss des trockeneren Klimas deutlich. Besonders die milden Winter
und hohen Sommertemperaturen begünstigen Lianen mit submeridionalem Verbreitungs-
schwerpunkt wie Vitis vinifera, Smilax excelsa und Periploca graeca. Diese Arten sind typisch für
Auwälder der südlichen Schwarzmeerküste und des Balkans (Stojanoff 1926).
Für Populus alba bildet der Große Kaukasus eine Verbreitungsgrenze, doch ist der ähnliche
Hybrid mit Populus tremula, Populus x canescens vertreten. Die halophytischen Arten der mit-
telasiatischen Auen Lycium ruthenicum und Halimodendron halodendron, sowie die typische
„Tugai-Art“ Populus euphratica fehlen. Tamarix, Cynanchum acutum und Elaeagnus leiten aber
schon zu den Galeriewäldern der Wüsten und Halbwüsten über.
Somit ist das untersuchte Gebiet ein südöstlicher Ausläufer der Auwälder europäischen
Typs, und bildet floristisch mit den Auen der südlichen Schwarzmeerregion eine Einheit.
Damit erscheint auch aus rein floristischer Sicht die Bezeichnung als „Tugai-Wald“ nicht zu-
treffend.
Abb.5.12: Lage der verglichenen Auwälder: 1: Mittelelbe; 2: Oberrhein; 3: Kamtschija; 4: Kura; 5: Amu Darya; 6: Tarim. Kartengrundlage: Weltkarte der ariden Gebiete (UNESCO 1977).
Managementempfehlungen
72
6 MANAGEMENTEMPFEHLUNGEN
6.1 Einleitung Schon der Vegetationskundler Radde (1899) erkannte die Probleme des Naturschutzes in den
Kaukasusländern: „Man hat hier keine Pietät weder für den Wald, noch überhaupt für den
Reichtum der Natur. Raubwirtschaft überall trotz vorzüglicher Gesetze, welche wenn befolgt,
der oft schon sehr erschöpften Natur aufhelfen könnten.“ Zwar wird auch damals weniger
mangelnde Pietät, als die Armut das größte Problem gewesen sein. Doch auch heute bestehen
gute Gesetze zum Schutz der Naturgüter, doch werden sie nur selten befolgt. Gerade in ei-
nem Reservat mit hoher Nutzungskonkurrenz ist Naturschutzarbeit nur unter Berücksichti-
gung der Lebensumstände der Bevölkerung erfolgreich umsetzbar.
Momentan fehlen Konzeptionen für das Schutzgebiet und Handlungsanweisungen für die
Gebietsbetreuung. Deshalb wird im folgenden ein Schutzziel aufgestellt und unter Einbezie-
hung der landschaftsökologischen und sozioökonomischen Analysen dann Gefahren aufge-
zeigt, um schlussendlich Schutzempfehlungen zu geben.
6.2 Schutzziele Das oberste Schutzziel für Zapovedniks ist der Ablauf natürlicher Dynamik, wofür alle Nut-
zungen per Gesetz verboten, und Eingriffe nicht gestattet sind (Umweltministerium Aserbai-
dschan 2006). Wenn aber das Schutzgebiet den Status eines Zapovedniks behalten soll, kann
es daneben keine anderen Schutzziele geben, es sei denn diese ordnen sich unter und lassen
sich im Kielwasser des Prozessschutzes erreichen. Als Schutzziel für Garayazi wurde den-
noch immer konkret der „Waldschutz“ und nicht natürliche Prozesse genannt (UN 2003).
Weitere Schutzziele könnten Artenschutz, Biotopschutz oder der Erhalt der heutigen sehr
diversen Weidelandschaft sein – ein Ziel was momentan besonders in Europa stark diskutiert
wird (Assmann & Falke 1997; Hüppe 1997). Einige Autoren halten sogar eine Beweidung für
essentiell um eine angeblich ursprüngliche Naturlandschaft mit ihren Prozessen wiederher-
zustellen (Bunzel-Drüke 1997). Welche Lösungen sind denkbar?
Schutz dynamischer Prozesse:
Die Aue mit dem verwilderten Flusslauf und den Auwäldern ist noch in einem weitgehend
natürlichen Zustand. Derartig unberührte und dynamische Auensysteme existieren in Euro-
pa und Mittelasien kaum noch (Dister 1998; Treshkin 2001; Volk 1994). Des weiteren sollte in
Waldschutzgebieten die natürliche Dynamik nicht bewusst beeinflusst werden (Klein 1998).
Als Folge des Prozessschutzes würde das Szenario aus Kap.5.4 einsetzen. Naturereignisse wie
Managementempfehlungen
73
Kalamitäten, Extremhochwässer oder Brände könnten auftreten und zeitweilig Offenland
schaffen.
Waldschutz:
Der Schutz der Wälder stand bei der Einrichtung des Reservates im Vordergrund. In den letz-
ten 20 Jahren schrumpfte die Waldfläche Aserbaidschans von 13,6 auf 10 % (Verdiyev 2004).
Mit einem Aufforstungsprogramm möchte die Regierung nun den Anteil auf 20 % erhöhen.
Leider fehlt es an Forstexperten im Land, da die Forstwirtschaft früher von Moskau und Tiflis
aus geleitet wurde (UN 2003). Generell sind Auwälder durch vielfältige Nutzungen ver-
drängt worden, so dass deren Erhaltung und Wiederherstellung oberste Priorität haben sollte
(Scherzinger 1996). Durch den Schutz dynamischer Prozesse wäre dem Waldschutz in Gebiet
ausreichend Rechnung getragen.
Artenschutz:
Ein Ziel des Naturschutzes ist der Schutz weltweit gefährdeter Arten, die zum großen Teil in
der Roten Liste der IUCN geführt werden (IUCN 2004). Besonders die Kaukasusregion weist
dabei sehr viele Endemiten auf (Schmidt 2005). In der Kura-Niederung gibt es jedoch nur
zwölf endemische Pflanzenarten (Grossheim 1936), die nicht im Schutzgebiet vorkommen.
Gleditsia caspica und Diospyros lotus sind zwar Kaukasusendemiten, wurden aber erst künst-
lich in die Wälder eingebracht. Einige Arten wie Populus nigra sind auf die Flussdynamik an-
gewiesen und deswegen in vielen Bereichen ihres ehemaligen Verbreitungsgebietes nur noch
durch aufwendige Maßnahmen zu erhalten (Joachim 2004). An der Kura regenerieren sich
die Pappelbestände hingegen noch ohne Unterstützung.
Mehrere weltweit gefährdete Tierarten leben im Gebiet, darunter Fischotter, Griechische
Landschildkröte, Europäische Sumpfschildkröte, Großer Eichenbock und Kaiseradler (siehe
Anh.1+2). Diese Arten würden durch einen Nutzungsverzicht nicht gefährdet, eventuell aber
sogar gefördert werden. Der Bestand des Rothirsches in Aserbaidschan schrumpfte von 2500
Stück um 1976 auf 1000 Stück um 1991 (UN 2003). Mit Einstellung der Nutzung könnte sich
die verbliebene Restpopulation auch wieder erholen. Im Gebiet kommen 24 Vogelarten der
EU-Vogelschutzrichtlinie (EWG 1979) vor, deren Lebensräume erhalten werden sollen, um
ein Aussterben zu verhindern. Davon sind 21 Arten auf Wälder, Feuchtgebiete oder Gewäs-
ser angewiesen. Der Schutz dieser Arten würde also auch durch Prozesschutz und/oder
Waldschutz gewährleistet werden.
Schutz von lokaler Biodiversität und der Weidelandschaft:
Durch Beweidung und Holzentnahme stieg der Strukturreichtum im Gebiet. So entstanden
Tümpel, Quellfluren, Trittrasen, Gebüsche und Lichtungen auf Kosten des Waldes und die
Zahl an Pflanzen- und Tierarten stieg (allein 103 Vogelarten wurden in Anh.1 nebenbei er-
Managementempfehlungen
74
fasst). Viele dieser Offenlandarten haben ein großes Verbreitungsareal und sind weltweit
nicht bedroht. Der Erhalt der Weidestrukturen könnte durch Fortsetzung der jetzigen Land-
nutzung erhalten werden, greift aber stark in die natürlichen Prozesse ein. Dieses Ziel sollte
dem Schutz der Wälder untergeordnet werden, zumal die Beweidung auch außerhalb des
Gebietes derartige Strukturen schafft, und eine Einstellung der Nutzung im Gebiet sowieso
nur nach einer langen Übergangsphase zu realisieren ist. In Dorfnähe werden Weidewälder
noch lange Zeit Bestand haben.
Somit sollte das prioritäre Ziel die natürliche Entwicklung der Auendynamik und der Wäl-
der sein. Ersteinrichtende Maßnahmen sollten nur in Ausnahmefällen durchgeführt werden.
6.3 Gefährdungen
Langfristige Gefährdungen:
1. Potentiell kann eine Veränderung des Flussregimes und der Stofffracht durch
Staustufenbau an georgischen Abschnitten der Kura verursacht werden. Momentan
ist die Stofffrachtbilanz ausgeglichen, so dass sich der typische verwilderte Flusslauf
erhält. Durch Staustufen würde die Geröllfracht verringert, die Frachtabfuhr über-
wiegen und eine Eintiefung des Flussbettes einsetzen (Ahnert 1996). In der Folge
würde sich die Fläche der Kies- und Sandbänke verkleinern, die Aue seltener überflu-
tet, weniger Sediment abgelagert und der Grundwasserstand des Talbodens sinken.
Die Zahl der potentiellen Standorte für die Weichholzaue würde zurückgehen und
die Aue insgesamt trockener werden, wodurch der typische „dschungelartige“ Au-
wald bedroht wäre.
2. Am Südufer existieren alte Eindeichungen und Regulierungssysteme, die jedoch ver-
fallen sind. Ihre Instandsetzung könnte ähnliche Folgen wie in Punkt 1 hervorrufen.
3. Durch den Eisenbahndamm bei Poily tritt die beschriebene Versalzung auf
(Kap.4.5.2). Hiervon ist langfristig der Wald bis ca. 4 km flussaufwärts betroffen.
4. Die Verschmutzung des Flusses mit toxischen gelösten Stoffen kann eventuell die
Wasserfauna schädigen. Das Treibmüllaufkommen ist dem mitteleuropäischer Flüsse
ähnlich und beeinträchtigt das Erscheinungsbild des Schutzgebietes, dürfte aber ge-
ringe Wirkungen auf das Ökosystem haben.
Managementempfehlungen
75
Mittel- und kurzfristige Gefährdungen:
1. Durch Gräben werden besonders Flächen auf der 3. Terrasse und die gesamte 4. Ter-
rasse entwässert. Die Standorte des Quercus-Waldes wurden dadurch trockener und
die mit Rieden bestandenen Flächen nahmen ab. Der Auwald ist weniger betroffen.
2. Feuerholzwerbung ist in dorffernen Wäldern noch kein großes Problem, doch ist der
dorfnahe Wald extrem gefährdet. Steigender Bedarf dürfte zur ernsten Gefahr der
Niederungswälder anwachsen. Illegaler kommerzieller Holzeinschlag scheint dage-
gen für die schlecht erschlossenen und krummwüchsigen Bestände keine Gefahr.
3. Momentan ist die Ackerfläche im Gebiet noch gering. Eine Ausdehnung auf heutige
Grünlandstandorte ist denkbar, zumal ein Hektar Acker jährliche Erlöse von über
1000 US$ bringt (Kap.4.4.2).
4. Wie beschrieben, kann die Weidewirtschaft trockene Wälder vernichten und auf
feuchten Standorten die Bewaldung verzögern. Auf den ersten Blick erscheint sie als
offensichtlichste Gefahr, doch wäre es verkehrt, wenn die Schutzbemühungen einzig
auf ihre Abschaffung fokusiert würden.
5. Grundsätzlich besteht eine Gefahr im mangelnden landwirtschaftlichen Fachwissen
der Anwohner, die ihre Subsistenzbetriebe auf Kosten des Schutzgebietes zum Teil
völlig ineffizient führen.
6. Auch das Defizit an fachlicher Bildung der Schutzgebietsbetreuer führt dazu, das die-
se ihr Augenmerk auf Lappalien richten und notwendige Maßnahmen nicht umset-
zen, oder sogar guten Willens verheerende Eingriffe, wie den Bau eines Schutzkanals
planen.
6.4 Maßnahmenkatalog
Die vielfältigen Gefährdungsursachen erfordern Maßnahmen auf verschiedenen administra-
tiven, zeitlichen und örtlichen Ebenen, und müssen von unterschiedlichen Akteuren durchge-
führt werden. Zum Teil ist nur das koordinierte Handeln der Schutzgebietsbetreuung ge-
fragt, manchmal aber auch größerer finanzieller Aufwand von Nöten. Vielleicht können da-
für Ausgleichsmittel aus dem Pipelinebau, welcher das Gebiet tangiert, oder Gelder des staat-
lichen Ölfonds zur Förderung strukturschwacher Räume verwendet werden.
Maßnahmen im Schutzgebiet:
1. Die Äcker im Gebiet müssen aufgegeben, und der natürlichen Wiederbewaldung
zugeführt werden. Eventuelle Entschädigungsansprüche sind zu begleichen.
Managementempfehlungen
76
2. Alle Gräben und Kanäle (Abb.4.54), die nicht zur Wasserversorgung der Dörfer die-
nen, müssen mit dem alten, zumeist noch vorhandenen Grabenaushub verfüllt wer-
den. Dadurch werden vernässte nutzungsfreie Flächen entstehen.
3. Stark degradierte Baumbestände in Dorfnähe sind großräumig einzuzäunen um das
Weidevieh abzuhalten und die Waldregeneration zu fördern. Als Zaunpfähle können,
wenn nötig, Robinien verwendet werden. Diese Pfähle sind wiederverwendbar (Göh-
re 1952).
4. Durch die Ranger ist im Gebiet befindlicher Müll, insbesondere große Mengen
Schrott, kaputte Fahrzeuge, unzählige Wodkaflaschen etc. zu beräumen.
5. Das illegale Fällen lebender Bäume ist zu bestrafen. Wenn die Energie- und Wärme-
versorgung der Dorfbewohner gewährleistet ist, sollte das Entnahmeverbot auch auf
Totholz ausgeweitet werden.
6. Momentan erscheint ein Beweidungsverbot illusorisch. Dies sollte jedoch als mittel-
bis langfristiges Ziel angestrebt werden. In der Übergangszeit sollten von den Hirten
stetig steigende Weidegebühren an die Schutzgebietsverwaltung gezahlt werden, um
den Tierbestand langsam zu verkleinern. Als Markierung können Ohrmarken ver-
wendet werden. Zur Vermeidung von Korruption sind diese Zahlungen exakt abzu-
rechnen, zu prüfen und zu veröffentlichen. Als Referenzwährung ist der US Dollar zu
verwenden, um eine inflationsbedingte Wirkungslosigkeit der Gebühren zu verhin-
dern. Folgende Jahresgebühr, die jährlich um ein Zehntel des Ausgangswertes erhöht
werden soll, scheint angemessen:
Gebührenpflichtige Haustiere Höhe der Weidegebühren [US$ pro Jahr]
Rinder, Wasserbüffel, Pferde; älter als ein Jahr 10
Jungrinder, -büffel, Fohlen, Esel 5
Schafe, Ziegen; älter als ein Jahr 2
Geflügel und Lämmer Kostenfrei
Die Gelder sind von der Verwaltung zweckgerichtet für Schutzmaßnahmen, beson-
ders aber Bildung, Aufforstungen und behutsame touristische Erschließung aus-
zugeben. So kommen die Abgaben den Dörfern wieder zugute.
Verbesserung der Gebietsbetreuung:
1. Nur durch bessere Entlohnung wird die Arbeitsmoral der Ranger steigen und die
Notwendigkeit, eigene Landwirtschaft im Schutzgebiet zu betreiben, verringert.
2. Die Mitarbeiter sind über die Bedeutung des Schutzgebietes, Zielstellung, Maßnah-
men und weitere naturschutzfachliche Sachverhalte zu unterrichten und weiterzubil-
den.
3. Eine Veränderung der Struktur der Verwaltung und der Verzicht auf nicht notwendi-
ge Stellen ist zur Effizienzsteigerung zu prüfen.
Tab. 6.1: Empfohlene Höhe der Weidegebühren
Managementempfehlungen
77
4. Die Grenzen des Schutzgebietes sind im Gelände zu kennzeichnen. Des weiteren
müssen exakte Karten mit Grenzen und Eigentumsverhältnissen bereitgestellt wer-
den.
5. Mit einem einfachen Monitoringsystem sind die Ausdehnung der Waldflächen und
Lichtungen sowie das Vorkommen wichtiger Arten (z.B.: Kaiseradler, Schwarzstorch)
zu erfassen.
6. Zur Sensibilisierung der Bewohner empfiehlt sich die Durchführung von Projekttagen
an den örtlichen Schulen.
Maßnahmen im Umfeld:
1. Als Hauptproblem erweist sich die Energieversorgung. Durch Instandsetzung der
Erdgas- und Elektrizitätsleitungen, sowie eines Förderprogramms für moderne Gas-
öfen ist dieser landesweite Schwachpunkt zu lösen.
2. Broschüren und Schulungen mit landwirtschaftlichen Inhalten (Umtriebsweide,
Stallhygiene, Maschineneinsatz, Bienenzucht) können zur Produktionssteigerung vor
Ort führen, und Acker- bzw. Grünlandflächen im Schutzgebiet entbehrlich machen.
3. Soweit möglich sind neue Waldflächen außerhalb des Schutzgebietes durch einge-
zäunte, anfangs bewässerte Pflanzungen zu schaffen. Die Standorte der Terrassen und
des Talbodens sind potentielle Waldstandorte, auf denen eine Neubegründung nied-
rige Kosten und hohen Erfolg verspricht. Dem Staatsziel von 20 % Waldfläche käme
man so näher. Zum Erhalt der genetischen Vielfalt ist nur Saatgut aus dem Gebiet zu
verwenden. Auf trockenen Standorten ist ein Mischbestand aus Stieleiche, Feldulme,
Pistazien, Wildbirnen und Wildäpfeln zu begründen. Auf feuchten Standorten emp-
fiehlt sich die Pflanzung von Graupappel, Schwarzpappel, Weiden und Feldulmen.
Ölweiden können auf versalzte Flächen gepflanzt werden. Bei ordnungsgemäßer
Pflege lässt sich schon nach wenigen Jahren Brennholz und später auch Bauholz wer-
ben, der Druck auf das Schutzgebiet würde sinken. Potentielle Flächen sind im Nor-
den die Gebiete zwischen der Bahnlinie und dem Schutzgebiet mit einer Größe von
ca. 2000 ha (hier gibt es bei Kätschbelli schon eine ca. 5 ha große, vitale Eichenkultur).
Im Süden, zwischen Juchari Salachli und Poily, gibt es über 1000 ha ausgedeichtes
Land. Durch Schlitzung der Dämme und Initialpflanzungen könnte sich der Auwald
wieder ausdehnen.
4. Wenn die Eisenbahnquerung bei Poily erneuert wird, sollte der Damm rückgebaut
werden und durch eine das gesamte Tal überspannende Brücke ersetzt werden.
Managementempfehlungen
78
Administrative Grundlagen:
1. Die Länder mit Anteilen am Kura-Einzugsgebiet sollten nicht durch wasserbauliche
Maßnahmen die Abflussverhältnisse des Flusses verändern.
2. Langfristig erscheint die Einrichtung eines großen Biosphärenreservates denkbar, in
dem sowohl die nutzungsfreien Zapovedniks, große Steppenweidegebiete und neu-
begründete Wälder eine Koexistenz führen würden. Dabei könnte die gesamte dünn-
besiedelte Fläche nördlich der Kura bis an den Iori und die georgische Grenze einbe-
zogen werden. Kernbereiche wären dann das Garayazi-Zapovednik, weitere Au-
waldreste an der Kura, die Auwälder am Iori, die Eldarkiefernwälder, Pistazienrest-
wälder in der Steppe und der Grenzsee Tschandargöl als Wasservogelrastgebiet. Da-
zwischen liegen große Gebiete mit Artemisia- und Stipa-Steppen die mit einer nachhal-
tigen Weidewirtschaft erhalten werden könnten.
6.5 Touristische Nutzung Als „letzte Dschungel Europas“ (Hofrichter & Herzer-Schmidt 2000) werden Auwälder im-
mer mehr das Ziel von Naturtouristen. In Österreich wurde extra der Nationalpark Donau-
Auen gegründet um den Wäldern wieder mehr Raum zu verschaffen und Menschen mit die-
sem Ökosystem vertraut zu machen. Östliche Transformationsländer wie Aserbaidschan rü-
cken zunehmend in den Blickpunkt des Ökotourismus, welcher in Zukunft sich vielleicht zu
einem bedeutenderen Wirtschaftsfaktor entwickelt. Wäre das Garayazi-Schutzgebiet als Rei-
seziel lohnend und ist solch eine Nutzung überhaupt denkbar?
Gesetzlich ist das Betreten von Zapovedniks ohne Genehmigung verboten, was sich wenig
mit der Realität deckt. Solange Ruhezonen um besonders sensible Bereiche eingehalten wer-
den, steht aber einem Betreten naturschutzfachlich nichts im Wege. Da das Gebiet aber nur
sehr schwer erreicht werden kann, ist die Anziehungskraft auf Touristen gering. Im Reisefüh-
rer wird die Gegend als finsteres Hinterland mit miserablen Straßen bezeichnet, in dem man
höchstens Schmuggler und Militär trifft (Elliott 2004). Momentan erschwert bei Poily ein mit
vielen bewaffneten Uniformierten ausgestatteter Kontrollpunkt ohne erkennbaren Grund die
Reise ans Nordufer der Kura. Nur wenn sich diese befremdlichen Umstände ändern, ist dort
mit Touristen zu rechnen. Dann wird es auch kein Problem sein, einen Rundweg durch die
Wälder anzulegen und Unterkünfte in den Dörfern einzurichten.
Viel besser eignet sich das Südufer mit seinen steilen Kliffen bei Schichli I an der Hauptstraße
Baku – Tiflis. Hier kann der Durchreisende eine Rast einlegen und den beeindruckenden
Blick über die Niederung mit ausgedehnten Wäldern und der Kura genießen. Es müsste nur
ein Parkplatz an der Straße angelegt werden, von dem ein Pfad bis zu einer Plattform auf
dem 140 m hohen Steilufer führt. Eine Hinweistafel würde dies abrunden.
Fazit
79
7 FAZIT UND AUSBLICK Im Zapovednik Garayazi existieren noch Auwälder, welche einem kaum anthropogen beein-
flusstem Überflutungsregime unterliegen. Auf angrenzenden Niederterrassen tritt Grund-
wasser zu tage, welches vermutlich in den großen pleistozänen Schotterterrassen weiter
nördlich gebildet wird. Es ermöglicht im semiariden Klima das Wachstum von Eichen-
Ulmenwäldern und speist sogar Moore mit Cladium mariscus.
Durch Beweidung, Holzeinschlag und stellenweise Drainage degradierten die Wälder zu
Hudewäldern, Weiderasen und vegetationsfreien Flächen. Tümpel und Schlenken mit
Schlammfluren entstanden durch Viehtritt.
Sowohl in den Auen- als auch in den Niederungswäldern dominieren Sträucher und Bäume
des beweidungstoleranten Weißdornes die Waldbestände. Dieser und schnellwüchsige Lia-
nen schützen die verbliebenen Wälder vor dem Eindringen von Rindern und Wasserbüffeln.
Die Aue lässt sich in drei Zonen, das verwilderte Flussbett mit offenen Kies- und Sandbän-
ken, die Weichholzaue aus Weiden, Pappeln und Tamarisken sowie eine Hartholzaue mit
Eichen und Feldulmen gliedern, welche sich anhand der Gehölzartenzusammensetzung in
einer Sukzessionsreihe anordnen lassen. Dabei läuft die Entwicklung auf Sandböden anders
als auf schluffigen bis tonigen Böden ab. Die Wälder besitzen damit typische Eigenschaften
südosteuropäischer Auwälder und weisen nur wenige Gemeinsamkeiten mit den Tugai-
Wäldern Mittelasiens auf.
In dem momentan nicht ausreichend gesicherten Schutzgebiet sind schnellstmöglich Schutz-
maßnahmen zu ergreifen. Dazu zählen die Verfüllung von Gräben, das Offenlassen von
Äckern und eine Reduzierung der Beweidung sowie Feuerholzwerbung. Durch Verbesse-
rung der Infrastruktur und gezielte Weiterbildung der Anwohner lassen sich der Nutzungs-
druck auf das Gebiet reduzieren, und die wirtschaftlichen Verluste der Kleinbauern kompen-
sieren. Der Erhalt des letzten großen Auwaldgebietes Aserbaidschans ist möglich!
Folgende Fragestellungen sollten zukünftig im Gebiet bearbeitet werden:
1. Wie groß ist die Ausdehnung der Moore und welche Eigenschaften besitzen diese?
2. Wie verändert sich die Struktur der Wälder und der Wildbestand nach Einstellung der
Weidenutzung? Wären Linden und Hainbuchen die prägenden Arten der Hartholzaue?
Wie entwickeln sich die eingeführten Gehölzarten?
3. Erfüllen durchgeführte Schutzmaßnahmen die Zielvorgaben?
4. Der Einfluss von Großsäugern auf die Landschaftsentwicklung steht im Mittelpunkt vie-
ler Versuche und Dispute. Einige Fragen könnten im Garayazi-Schutzgebiet geklärt wer-
den, wo schon seit Jahrhunderten der Erhalt halboffener Landschaften mit Großsäugern
praktiziert wird.
Zusammenfassung
80
8 ZUSAMMENFASSUNG Am Mittellauf der Kura, im Westen Aserbaidschans, existieren noch Au- und Niederungs-
wälder im 97 km² großen Zapovednik (Naturschutzgebiet) Garayazi. Seit über 30 Jahren
standen diese azonalen Wälder inmitten des Steppengebietes der Kura-Niederung nicht mehr
im Blickpunkt der Forschung. Auch war der Zustand des als Totalreservat geführten Schutz-
gebietes nicht bekannt. Um sowohl einen Beitrag zur Erforschung von Auwäldern im Kauka-
sischen Raum zu leisten und gleichzeitig den Schutz dieser seltenen Landschaft zu verbes-
sern, ergaben sich im Vorfeld der Diplomarbeit folgende Fragestellungen:
1. Welche Vegetationstypen mit welchen Standortsansprüchen sind vorhanden?
2. Wie prägen die einzelnen Gehölzarten die Struktur der Wälder?
3. Lässt sich anhand der Daten eine Sukzessionsreihe von einer Weichholz- zu einer
Hartholzaue ableiten, oder existiert nur eine Weichholzaue wie in den Tugai-Wäldern
Mittelasiens?
4. In welchem Zustand befindet sich das Zapovednik Garayazi, und welche Maßnahmen
sind nötig um einen dauerhaften Schutz zu gewährleisten?
Um diese Fragen zu beantworten bedurfte es zuerst einer landschaftsökologischen Analyse
mit vegetationsökologischem Schwerpunkt. In einem 5 km langen, senkrecht zum Fluss ver-
laufenden Korridor wurden 126 Vegetationsaufnahmen durchgeführt. Um den jeweiligen
Standort zu charakterisieren wurden Bodenprofile angelegt, das Terrassenniveau und die
Entfernung vom Dorf bestimmt, die Nutzungsintensität geschätzt sowie im Auwald die Höhe
der Überflutung nach einem Hochwasser gemessen. Durch Tabellenarbeit und DCA – Analy-
sen wurden sozio-ökologische Artengruppen gebildet und schließlich Vegetationstypen aus-
gegliedert.
Besonderes Augenmerk galt der Bestandesstruktur der Wälder. An den 59 Aufnahmepunk-
ten im Wald wurden je 20 Bäume per Point-Centered Quarter Method (Cottam & Curtis 1956)
vermessen. Alle Aufnahmen eines Vegetationstyps wurden zusammengefasst. Das Alter von
Eichen und Pappeln konnte näherungsweise durch ein Wachstumsmodell ermittelt werden,
welches auf eigenen Jahresringanalysen von Baumstümpfen basiert.
Im Schutzgebiet liegen die Aue und vier Terrassenniveaus, welche nicht vom Flussregime
geprägt werden. Das ganze Gebiet wird täglich durch große Viehherden aus Wasserbüffeln,
Rindern und in Dorfnähe Schafen beweidet. Auf den Terrassen stocken auf tonigen Böden
durch Beweidung und Holzentnahme stark degradierte Eichen-Ulmenwälder, die aber schon
großflächig durch Grünland verdrängt wurden. Nur in dorffernen Bereichen breitet sich der
Wald mit Hilfe von Weißdorngebüschen wieder aus. Das Offenland ist durch kurze Rasen,
vegetationsfreie Triften, Schlammfluren, Gräben und wassergefüllte Senken mit Rieden sowie
Zusammenfassung
81
eutrophe Tümpel geprägt. In den Senken bildeten sich Moore aus. Der Wasserhaushalt wird
durch permanent zuströmendes Quellwasser aus höheren Schotterterrassen und Haftwasser
im tonigen Boden bestimmt.
Auch die Auwälder mit ihren großen Graupappeln sind durch Weidenutzung degradiert.
Neben dichten Wäldern sind besonders auf hohen Kiesbänken Lichtungen und Gebüsche
anzutreffen. Eine Besonderheit sind Erlensäume entlang von kleinen Bächen am Rande der
Aue.
Bei jedem Hochwasser werden alte Wälder zerstört und neue Standorte für eine Wiederbe-
siedlung geschaffen. Mithilfe der ermittelten Bestandesdaten lässt sich folgendes Sukzes-
sionsschema ableiten: Im verwilderten Flussbett werden Kiesbänke von Ephemeren und spä-
ter von Tamarisken besiedelt. Fast zeitgleich stellen sich Jungpappeln ein und verdrängen die
Tamarisken schon nach zehn Jahren. In der Zwischenzeit sedimentieren Schluffe und Sande
und die Bestände dünnen aus. Es folgen von starken Pappeln dominierte Wälder, in welche
Ulmen und Eichen einwandern. Durch Beweidung wird besonders der Weißdorn gefördert.
Auf feuchten schluffigen Standorten entwickeln sich dann entweder dichte Lianenschleier,
die alle Bäume und Sträucher unterdrücken, oder Linden und Hainbuchenwälder. Andere
Bestände, besonders auf sandigen Böden werden durch Beweidung und Holzentnahme auf-
gelichtet, bis offene Wälder mit nitrophiler Krautschicht oder Lichtungen entstehen. Somit
entwickeln sich die Auwälder über ein Stadium der Weichholzaue zu Hartholzauenwäldern,
sofern diese Entwicklung nicht durch Flussbettverlagerungen abgebrochen wird. Die Wälder
entsprechen in ihrer Artenzusammensetzung europäischen Auwäldern und haben nur weni-
ge Gemeinsamkeiten mit den zentralasiatischen Tugai–Wäldern.
Die für Zapovedniks festgesetzte Nutzungsfreiheit ist in Garayazi nicht gewährleistet und
somit ist auch das Ziel, diese Auwälder in einem möglichst naturnahen Zustand zu erhalten,
gefährdet. Momentan ist das Flussregime nur durch einen Eisenbahndamm unterhalb des
Gebietes beeinträchtigt. Andere Gefahren stellen Entwässerungsgräben, Feuerholzwerbung,
illegale Äcker, Beweidung und vor allem mangelndes landwirtschaftliches Fachwissen der
Bevölkerung sowie schlechte fachliche Bildung der Schutzgebietsbetreuung dar.
Wichtige ersteinrichtende Schutzmaßnahmen wären das Verfüllen von Gräben und Kanälen,
die Aufgabe von Äckern, die Reduzierung der Beweidung durch Abgaben und die Sicherstel-
lung der Energieversorgung der Dörfer. Auch ist die Anlage neuer Wälder außerhalb des
Schutzgebietes mit autochtonem Pflanzenmaterial voranzutreiben. Gleichzeitig sollte in die
Bildungsarbeit der Schulen und der Schutzgebietsverwaltung investiert werden. Wenn dieses
Maßnahmenbündel durchgeführt wird, ist sehr schnell mit einer Regeneration der Au- und
Niederungswälder zu rechnen. Der Erhalt der Wälder inmitten der Steppe ist möglich.
Summary
82
9 SUMMARY
Large floodplain and lowland forests exist in the Zapovednik (strict nature reserve) Garayazi
in Western Azerbaijan. Here at the middle reaches of the Kura river the forests survived the
water regulation programme of the Soviet Era. That means, that they are one of the last near
natural forests in the Kura lowlands. A first description of the area was given by Radde in
1899. Later, Grossheim (1948), Prilipko (1970) and some forestry researchers (Alijew &
Chalilov 1976) investigated and recorded the vegetation of these forests. Within the last 30
years no scientific work was dedicated to this area. Thus, a lack of knowledge about the cur-
rent state of this reserve arose. The aim of the diploma thesis was to close this gap by answer-
ing the following questions:
1. What are the existing vegetation types and how are they correlated with which site
conditions?
2. How do the different woody species form the stands?
3. Is it possible to describe a succession line from softwood to hardwood forests, typical
for European floodplains, or are the forests comparable to Central Asian Tugai forma-
tions?
4. What is the current state of the Zapovednik and what arrangements should be consid-
ered to improve the conservation regime?
Between March and June 2005 field investigations on a 5 km long transect from the Kura river
to the adjacent village Muganli and on gravel bars, next to the village Garayazi, were taken.
To classify vegetation and site conditions 126 plots were sampled. Here the species abun-
dance, distance from the river and the village, elevation, carbon, humus and moisture content
of the soil, substrate and soil horizons were recorded by field methods. The Point-Centered
Quarter Method (Cottam & Curtis 1956) was used on the 59 plots in the forest to describe the
different stands. Also the age of poplars and oaks was estimated by a regression model based
on own tree ring analyses of cut trunks. After Dierschke (1994) and Koska et.al. (2001) vegeta-
tion types were generated with the help of socio ecological species groups. During the field
work and excursions the current situation of the reserve with its administration was noticed.
Also risks for conservation were evaluated.
The lowland near Muganli consists of a 2 km wide floodplain with a braided river system
and four terraces. From April to June short inundation events with a duration of two to four
days are typical. The floodplain system is not disturbed by regulations, thus the high river
Summary
83
dynamic leads on the one hand to a destruction of old forests, on the other hand to a deposi-
tion of new gravel bars.
Forests, pastures and fens on the terraces were continuously fed by groundwater from large
brash terraces in the north. Therefore they are independent of the Kura inundation regime.
Remnants of dry oak forests (Quercus robur) with 20 to 150 years old trees exist on cher-
nosemic soils of the 4th terrace next to the villages. This forests are used as pastures and wood
supply. A mosaic of moist oak elm forests and pastures with nine different vegetation types
can be found on the three lower terraces. The pastures are degradation states of the forests.
Here water buffalos, cattle, horses and sheep graze all over the year with an average density
of 0.7 cattle units per hectare. The results are short lawns on terrestrial sites, sparse mud vege-
tation under wetter conditions and disturbed reeds on sides with water above ground. Fea-
tures are little eutrophic ponds, irregular systems of trenches, little spring mires at the foot of
the 4th terrace and groundwater rise mires with Cladium mariscus. The extend of wetlands
with reed vegetation near Muganli is about 400 hectare. Possibly, most of the wetland is even
peatland.
By the use of the measured forest stand data and vegetation records it was possible to clarify
succession lines on the floodplain. The starting point are the gravel and sandy bars, next to
the river, where ephemeral plants and stress tolerant shrubs like Tamarix ramosissima and
Salix triandra grow. Additionally young poplars (Populus nigra, P. x canescens) occur. They
domineer the stands after 10 years with about 9600 trees per ha. Twenty years later only 400
trees survived and the first oaks and elms are mixed in this stands. Also hawthorn (Crataegus
riphidophylla) as a typical indicator of wood pastures appears. On sandy soils this state is sta-
ble for a long time. Only due to wood cutting and strong grazing this forests can transform
into glades with a xerophilous herb layer. On silty soils the water support is better, so lots of
lianas can grow. After approximately 40 years the poplars begin to die back. Stands can de-
grade into sparse forests with a dominance of hawthorn, oaks and elms caused by a strong
grazing regime. Here further degradation leads to glades, similar to that on sandy soils. On
less disturbed sites, a rare forest type with linden, hornbeam and maple develops. Further-
more it is also possible, that after the collapse of big poplar trees lianas cover the site and in-
hibit the growth of new trees.
The resulting succession scheme shows lines from softwood dominated stands on new bars to
hardwood forests. Due to this fact and an additional floristical comparison to Eurasian flood-
plain forests, the forests next to the Kura belong to the South-Eastern European floodplain
forests like in Bulgaria. There are only few similarities to Central Asian Tugai forests.
The aim of Zapovedniks is to conserve a landscape by the elimination of all utilisation. This is
contrary to the current state of the Garayazi Zapovednik. There hundreds to thousands of
livestock grazes, wood is used by the villagers, trenches drainage rare wetlands and acres can
Summary
84
be found. This state is a result of the bad economical situation of the adjacent villages with
low salaries, high unemployment and an insufficient education of the self-supplying farmers.
One of the most urgent problems is the availability of energy. To improve the state of the re-
serve, a couple of arrangements should be done. Examples are the filling up of old channels,
the fencing of endangered forest stands near the villages, sanctions for wood cutting and a fee
system to confine the grazing. Essential is the guarantee of power and gas supply. An im-
proved education of the farmers and the rangers should be taken into account. If all the ar-
rangements are accomplished, the forests in the Garayazi step can be conserved. It is possible,
that they become a highlight for ecotourism in future times.
Literatur
85
10 LITERATURVERZEICHNIS AG Boden 1994. Bodenkundliche Kartieranleitung. Hannover: E. Schweizerbart`sche Ver-
lagsbuchhandlung.
AG Boden 2005. Bodenkundliche Kartieranleitung. Stuttgart: E. Schweitzerbart`sche Ver-lagsbuchhandlung.
Ahnert, F. 1996. Einführung in die Geomorphologie. Stuttgart: Ulmer-Verlag.
Alijew, G. A. & Chalilov, M. Ju. 1976. Prikurinskije Tugainije Lesa Aserbaidschana. Baku: Elm.
Assmann, T. & Falke, B. 1997. Bedeutung von Hudelandschaften aus tierökologischer und naturschutzfachlicher Sicht. Schriftenreihe für Landschaftspflege und Naturschutz 54: 129-144.
Billwitz, K. 1997. Allgemeine Geoökologie. In Hendl, M. & Liedtke, H. (Hrsg.) Lehrbuch der Allgemeinen Physischen Geographie (635-720). Gotha: Justus Perthes Verlag.
Bridge, J. S. 2003. Rivers and Floodplains. Oxford: Blackwell Publishing.
Brinson, M. M. & Verhoeven, J. 1999. Riparian forests. In Hunter, M. L. (Hrsg.) Maintaining Biodiversity in Forest Ecosystems (265-299). Cambridge: University Press.
Bryant, D. M., Ducey, M. J., Innes, J. C., Lee, T. D., Eckert, R. T. & Zarin, D. J. 2005. Forest community analysis and the point-centered quarter method. Plant Ecology 175: 193-203.
Bunzel-Drüke, M. 1997. Großherbivore und Naturlandschaft. Schriftenreihe für Landschafts-pflege und Naturschutz 54: 109-128.
Bunzel-Drüke, M., Drüke, J., Hauswirth, L. & Vierhaus, H. 1999. Großtiere und Landschaft-Von der Praxis zur Theorie. Natur- und Kulturlandschaft 3: 210-229.
Cottam, G. & Curtis, J. T. 1956. The use of distance measures in phytosociological sampling. Ecology 37: 451-460.
Czerepanov, S. K. 1995. Sosydistye rastenija Rossii i sopredelnich gosydarstv. Sankt Peters-burg: ʺMir i Semja-95ʺ.
Dierschke, H. 1994. Pflanzensoziologie. Stuttgart: Eugen Ulmer.
Dister, E. 1985. Zur Struktur und Dynamik alter Hartholzauenwälder (Querco-ulmetum Issl. 24) am nördlichen Oberrhein. Verhandlungen der Zoologisch-Botanischen Gesell-schaft Österreich 123: 13-32.
Literatur
86
Dister, E. 1998. Die Bedeutung natürlicher Flußdynamik am Beispiel von Loire und Allier. Schriftenreihe für Landschaftspflege und Naturschutz 56: 67-78.
Dolginow, J. & Kropatschjow, S. 1994. Abriß der Geologie Rußlands und angrenzender Staa-ten. Stuttgart: E.Schweitzerbart`sche Verlagsbuchhandlung.
Ellenberg, H. 1996. Vegetation Mitteleuropas mit den Alpen. Stuttgart: Ulmer Verlag.
Elliott, M. 2004. Azerbaijan. Surrey: Trailblazer Publications.
Encyclopaedia Britannica 1997. The new Encyclopaedia Britannica. Chicago.
EWG 1979. Richtlinie des Rates vom 2.April 1979 über die Erhaltung der wildlebenden Vo-gelarten (79/409/EWG). Amt für amtliche Veröffentlichungen der Europäischen Ge-meinschaften.
Frahm, J.-P. & Frey, W. 1992. Moosflora. Stuttgart: UTB-Verlag.
Franz, H.-J. 1973. Physische Geographie der Sowjetunion. Gotha/Leipzig: VEB Hermann Haack.
Glavac, V. 1996. Vegetationsökologie. Jena: Gustav Fischer Verlag.
Göhre, K. 1952. Die Robinie und ihr Holz. Berlin: Deutscher Bauernverlag.
Grossheim, A. A. 1936. Analis Flori Kavkas. Baku: Aserbaidschanskowo filiala akademii nauk SSSR.
Grossheim, A. A. 1948. Rastitelny Pokrow Kavkasa. Moskau.
Grossheim, A. A. 1949-1962. Flora Kavkasa. Moskau, Leningrad: Isdatelstwo Akademii Nauk SSSR. (8 Bände)
Gulisaschvili, V. S., Machatadse, L. B. & Prilipko, L. I. 1976. Rastitelnostch Kavkasa. Mos-kau: Nauk.
Henning, I. 1972. Die dreidimensionale Vegetationsanordnung in Kaukasien. Erdwissen-schaftliche Forschung 4: 182-204.
Hinterholzer, J. 1999. Produktionserfolge im Österreichischen Maisanbau. Bericht über die 50.Arbeitstagung 1999 der Vereinigung österreichischer Pflanzenzüchter 147-151.
Hofrichter, R. & Herzer-Schmidt, K. 2000. Auwälder Die letzten Dschungel Europas. Stein-furt: Tecklenborg Verlag.
Honkong Observatory 2005. Climatological Information for Eastern Part of Turkey and Its Neighbouring Countries. www.weather.gov.hk/wxinfo/climat/world/eng/europe/gr_tu/tu_az_e.htm (15.01.06)
Literatur
87
Hüppe, J. 1997. Vegetationsdynamik in ʺhalboffenen Hudelandschaftenʺ-Abhängigkeit von Nutzungsintensität und natürlichen Ausgangsbedingungen sowie Anforderungen an künftige Naturschutzziele-. Schriftenreihe für Landschaftspflege und Naturschutz 54: 145-159.
IUCN 2004. Red List of Threatened Species. www.redlist.org (28.02.06).
Jäger, U. G. 2004. Standort, Struktur und Dynamik von Weichholzauengesellschaften an der Mittleren Elbe. Veröffentlichungen der LPR Landschaftsplanung Dr. Reichhoff GmbH 2: 39-54.
Joachim, H.-F. 2004. Zur Erhaltung der Schwarz-Pappel (Populus nigra L.). Naturschutz und Landschaftspflege in Brandenburg 13: 64-69.
Karjagin, I. I. 1950-1961. Flora Aserbaidschana. Baku: Isdatelstwo Akademii Nauk Aserbaid-schanskoi SSR. (8 Bände)
Klein, M. 1998. Walddynamik und ʹWildnisgebieteʹ. Schriftenreihe für Landschaftspflege und Naturschutz 56: 97-105.
Korowin, E. P. 1961. Rastitelnost Srednei Asii i Juschnowo Kasachstana. Taschkent: Isda-telstwo Akademii Nauk Usbekskoi SSR.
Koska, I., Succow, M. & Clausnitzer, U. 2001. Vegetationskundliche Kennzeichnung von Mooren. In Succow, M. & Joosten, H. (Hrsg.) Landschaftsökologische Moorkunde (112-184). Stuttgart: E. Schweitzerbart`sche Verlagsbuchhandlung.
Kovalev, V. 2000. Die Natur und ihr Schutz in Aserbaidschan. unveröffentlicht. Kramer, H. 1988. Waldwachstumslehre. Hamburg und Berlin: Parey.
Kühne, C. 2004. Verjüngung der Stieleiche (Quercus robur L.) in oberrheinischen Auenwäl-dern. Göttingen 2004: Dissertation (Georg-August-Universität Göttingen).
Mamedaliew, Ju. G. 1963. Atlas Aserbaidschanskoi SSR. Baku - Moskau: Gosudarstwennogo Geologitscheskowo Komiteta SSSR.
Mayer, H. 1986. Europäische Wälder. Stuttgart: Gustav Fischer.
Meusel, H., Jäger, E. & Weinert, E. 1965. Vergleichende Chorologie der zentraleuropäischen Flora. Jena: VEB Gustav Fischer Verlag.
Mitchell, K. 2001. Quantitative Analysis by the Point-Centered Quarter Method. http://people.hws.edu/mitchell/PCQM.pdf (14.01.06)
Mühr, B. 2005. Klimadiagramme weltweit. www.klimadiagramme.de.(27.02.06)
Musajev, M.H. 1984. Sovremennoje sostojanie fauno-floristitscheskovo kompleksa Kara-jaskovo Gosapovednika i ich vosstanoblenie. unveröffentlicht
Literatur
88
NASA 2006. Landsat Scene. ftp://ftp.glcf.umiacs.umd.edu/glcf/Landsat (14.01.06) Neef, E. 1956. Das Gesicht der Erde. Leipzig: VEB F.A. Brockhaus Verlag.
Nitsche, S. 1994. Extensive Grünlandnutzung. Radebeul: Neumann Verlag.
Prilipko, L. I. 1954. Lesnaja Rastitelnost Aserbaidschana. Baku: Isdatelstwo Akademi Nauk Aserbaidschanskoi SSR.
Prilipko, L. I. 1970. Rastitelny Pokrow Aserbaidschana. Baku: Elm.
Prodan, M. 1951. Messung der Waldbestände. Frankfurt am Main: J.D.Sauerländer`s Verlag.
Pykälä, J. 2003. Effects of restoration with cattle grazing on plant species composition and richness of semi-natural grasslands. Biodiversity and Conservation 12: 2211-2226.
Radde, G. 1899. Die Vegetation der Erde III. Grundzüge der Pflanzenverbreitung in den
Kaukasusländern. Leipzig: Wilhelm Engelmann.
Reichhoff, L., Patzak, U. & Warthemann, G. 2004. Ursprüngliche und heutige Baumarten-zusammensetzung der Hartholzauenwälder und ihre standörtlich-vegetations-kundliche Gliederung im Mittelelbegebiet. Veröffentlichungen der LPR Landschaftspla-nung Dr.Reichhoff GmbH 2: 29-38.
Robertson, D. F. 1993. Timber volume estimator handbook FSH 2409.12a. Washington: Uni-ted States Department of Agriculture; Forest Service.
Rothmaler, W., Jäger, E. & Werner, K. 2002. Exkursionsflora von Deutschland Gefäßpflan-zen: Kritischer Band. Heidelberg-Berlin: Spektrum Verlag.
Rubner, K. & Reinhold, F. 1953. Das natürliche Waldbild Europas als Grundlage für einen europäischen Waldbau. Hamburg / Berlin: Parey.
Scherzinger, W. 1996. Naturschutz im Wald. Stuttgart: Ulmer Verlag.
Schley, L. & Leytem, M. 2004. Extensive Beweidung mit Rindern im Naturschutz: Eine kur-ze Literaturauswertung hinsichtlich der Einflüsse auf die Biodiversität. Bulletin de la Societe des Naturalistes Luxembourgeois 105: 65-85.
Schmidt, P. A. 2002-2005. Bäume und Sträucher Kaukasiens. Mitteilungen der Deutschen Dendrologischen Gesellschaft Ausgaben 87-90 (4 Teile)
Schmidt, P. A. 2005. Biologische Vielfalt und ihr Schutz in der Kaukasusregion. In Erdmann, K. H. & Bork, H.-R. (Hrsg.) Zukunftsfaktor Natur - Blickpunkt Berge und Gebirge (159-177). Bonn-Bad Godesberg: Bundesamt für Naturschutz.
Schnitzler, A. 1997. River Dynamics as a Forest Process: Interaction between Fluvial Sytems and Alluvial Forests in Large European River Plains. The Botanical Review 63: 40-63.
Schober, R. 1995. Ertragstafeln wichtiger Baumarten bei verschiedener Durchforstung. Frankfurt am Main: J.D. Sauerländer.
Literatur
89
Seibert, P. 1987. Der Eichen-Ulmen-Auwald (Querco-Ulmetum Issl.24) in Süddeutschland. Natur und Landschaft 62: 347-352.
Skworzow, G. A. 1976a. Topographische Karte 1:100 000 K-39-103 Kasach. Generalstab des Sowjetischen Militärs.
Skworzow, G. A. 1976b. Topographische Karte 1:100 000 K-38-91 Rustavi. Generalstab des Sowjetischen Militärs.
SSCAR 2006. Estimation of poverty statistics in Azerbaijan Republic. www.nscb.gov.ph/poverty/conference/papers/11azerbaijan.pdf (06.03.06)
Stojanoff, N. 1926. Der Longos-Wald in Bulgarien. Botanische Jahrbücher 62: 502-524.
Stolbovoi, V. 2000. Soils of Russia: Correlated with the Revised Legend of the FAO Soil Map of the World and WorldReference Base for Soil Resources. Laxenburg.
Succow, M. 2001. Ökologisch(-phytozoenologische) Moortypen. In Succow, M. & Joosten, H. (Hrsg.) Landschaftsökologische Moorkunde (229-234). Stuttgart: Schweizerbart`sche Verlagsbuchhandlung.
Thevs, N. 2005. Tugay vegetation in the middle reaches of the Tarim River - Vegetation ty-pes and their ecology Archiv für Naturschutz und Landschaftsforschung Nr. 44: 63-84.
Tian, Y. 1991. Tokai on the delta at the lower reach of the Keriya River. Zeitschrift der Gesell-schaft für Erdkunde zu Berlin Ergänzungsheft 6: 99-112.
Thomasius, H. & Schmidt, P. A. 1996. Wald, Forstwirtschaft und Umwelt. Bonn: Economica Verlag.
Treshkin, S. Y. 2001. The Tugai Forests of Floodplain of the Amudarya River. In Breckle, S.-W., Veste, M. & Wucherer, W. (Hrsg.) Sustainable Land Use in Deserts (95-102). Ber-lin-Heidelberg: Springer.
Umweltministerium Aserbaidschan 2006. Law of the Azerbaijan Republic on specially pro-tected natural territories and objects. http://www.eco.gov.az/v2.1/en/ministry/toplu/eco13.doc (07.03.06)
UN 2003. Draft Environmental Performance Reviews of Azerbaijan -First Review-. Genf: United Nations.
UNESCO 1977. World distribution of arid regions. Paris. (Karte)
Urushadze, A.T. 2005. Alluvial Soils in Eastern Georgia. Eurasian Soil Science 1: 38-46
Verdiyev, R. 2004. The role of ecosystems of Azerbaijan - forests and wetlands as water sup-pliers. Genf: Seminar on the role of ecosystems as water suppliers.
Volk, H. 1994. Wie naturnah sind die Auewälder am Oberrhein? Naturschutz und Land-schaftsplanung 26: 25-31.
Literatur
90
Walter, H. 1974. Die Vegetation Osteuropas, Nord- und Zentralasiens. Stuttgart: Gustav Fischer Verlag.
Walther, H. 1968. Die Vegetation der Erde in öko-physiologischer Betrachtung. Jena: VEB Gustav Fischer Verlag.
Weber, H. E. 2003. Gebüsche, Hecken, Krautsäume. Stuttgart: Ulmer Verlag.
Weibull, A. C., Östman, Ö. & Granqvist, A. 2003. Species richness in agroecosystems: the effect of landscape, habitat and farm management. Biodiversity and Conservation 12: 1335-1355.
World Sites Atlas 2005. Physical map of Transcaucasia. www.sitesatlas.com/Maps/Maps/605r.htm. (18.12.05)
WWF 2005. Ecoregional conservation plan for the Caucasus - Fifth Draft.
Anhangsverzeichnis:
Anhang 1 Liste der im Untersuchungsgebiet bei Muganli beobachteten Vögel
Anhang 2 Liste der im Untersuchungsgebiet bei Muganli beobachteten Tiere (außer
Vögel)
Anhang 3 Liste der im Untersuchungsgebiet angetroffenen Gehölze und Lianen
Anhang 4 Liste der im Gebiet angetroffenen krautigen Pflanzen
Anhang 5 Bestandeskenndaten aus der PCQ-Analyse
Anhang 6 Protokolle der Bodenschürfe
Anhang 7 Vegetationsaufnahmen der Tümpel
Anhang 8 Vegetationsaufnahmen des Grünlandes und Cladium-Riedes
Anhang 9 Vegetationsaufnahmen der Wälder
Anhang 1: Liste der im Untersuchungsgebiet bei Muganli beobachteten Vögel
(März-Juni 2005)
Wissenschaftlicher Name Englischer Name Deutscher Name Bemerkungen Schutzkategorie
Kormorane / Phalacrocoracidae Phalacrocorax pygmeus Pygmy Comorant Zwergscharbe Einzeltiere IUCN: NT / EU-VSR:
Reiher / Ardeidae Ardea cinerea Grey Heron Graureiher Ardea purpurea Purple Heron Purpurreiher EU-VSR: Anh.1 Egretta alba Great Withe Egret Silberreiher
Störche / Ciconiidae Ciconia ciconia White Stork Weißstorch 1 BP EU-VSR: Anh.1 Ciconia nigra Black Stork Schwarzstorch mehrere BP EU-VSR: Anh.1
Entenvögel / Anatidae Anas platyrhynchos Mallard Stockente häufig Mergus merganser Goosander Gänsesäger Durchzügler
Habichtartige / Accipitridae Accipiter brevipes Levant Sparrowhawk Kurzfangsperber selten EU-VSR: Anh.1 Accipiter gentilis Goshawk Habicht Accipiter nisus Sparrowhawk Sperber Aquila heliaca Imperial Eagle Kaiseradler mehrere BP IUCN: VU / EU-VSR: Aquila pomarina Lesser Spotted Eagle Schreiadler Brutverdacht EU-VSR: Anh.1 Buteo buteo Common Buzzard Mäusebussard Buteo rufinus Long-legged Buzzard Adlerbussard EU-VSR: Anh.1 Circus aeruginosus Marsh Harrier Rohrweihe mehrere BP EU-VSR: Anh.1 Circus cyaneus Hen Harrier Kornweihe Durchzügler EU-VSR: Anh.1 Milvus migrans Black Kite Schwarzmilan EU-VSR: Anh.1 Pernis apivorus Honey Buzzard Wespenbussard viele Durchzügler EU-VSR: Anh.1
Falken / Falconidae Falco naumanni Lesser Kestrel Rötelfalke Durchzügler EU-VSR: Anh.1 Falco subbuteo Hobby Baumfalke mehrere BP Falco tinnunculus Kestrel Turmfalke
Glattfußhühner / Phasianidae Coturnix coturnix Quail Wachtel häufig Perdix perdix Partidge Rebhuhn Phasanius colchicus Pheasant Jagdfasan einzelne Tiere
Rallen / Rallidae Gallinula chloropus Moorhen Teichhuhn
Kraniche / Gruidae Anthropoides virgo Demoiselle Crane Jungfernkranich Durchzügler
Brachschwalben / Glareolidae Glareola pratincola Collared pratincole Rotflügel-Brachschwalbe EU-VSR: Anh.1
Regenpfeifer / Charadriidae Charadrius dubius Little Ringed Plover Flussregenpfeifer auf Kiesbänken
Schnepfenvögel / Scolopacidae Vanellus vanellus Lapwing Kiebitz
Seeschwalben / Sternidae Chlidonias leucopterus White-winged Black Tern Weißflügelseeschwalbe
Tauben / Columbidae Columba livia f. domestica Rock Dove Straßentaube Columba oenas Stock Dove Hohltaube Columba palumbus Woodpigeon Ringeltaube Streptopelia decaocto Collared Dove Türkentaube Streptopelia turtur Turtle Dove Turteltaube
Kuckucke / Cuculidae Cuculus canorus Cuckoo Kuckuck
Eulen / Strigidae Athene noctua Little Owl Steinkauz Bubo bubo Eagle Owl Uhu EU-VSR: Anh.1 Otus scops Scops Owl Zwergohreule
Nachtschwalben / Caprimulgidae Caprimulgus europaeus Nightjar Nachtschwalbe EU-VSR: Anh.1
Segler / Apopidae Apus apus Swift Mauersegler
Rackenvögel / Coraciidae s.l. Alcedo atthis Kingfisher Eisvogel EU-VSR: Anh.1 Coracias garrulus Roller Blauracke häufig EU-VSR: Anh.1 Merops apiaster Bee-eater Bienenfresser häufig Upupa epops Hoopoe Wiedehopf sehr häufig
Spechte / Picidae Dendrocopos major Great Spotted Woodpecker Buntspecht Dendrocopos medius Middle Spotted Woodpecker Mittelspecht EU-VSR: Anh.1 Dendrocopos minor Lesser Spotted Woodpecker Kleinspecht Dendrocopos syriacus Syrian Woodpecker Blutspecht EU-VSR: Anh.1 Picus viridis Green Woodpecker Grünspecht
Sperlingsvögel / Passeriformes Alauda arvensis Skylark Feldlerche Melanocorypha calandra Calandra Lark Kalanderlerche
Hirundo rustico Swallow Rauchschwalbe Riparia riparia Sand Martin Uferschwalbe Motacilla alba White Wagtail Weiße Bachstelze Motacilla flava feldegg Black-headed Wagtail Maskenstelze Motacilla flava flava Blue-headed Wagtail Schaftstelze Motacilla citreola Citrine Wagtail Zitronenstelze Durchzügler Acrocephalus arundinaceus Great Reed Warbler Drosselrohrsänger Acrocephalus schoenobaenus Sedge Warbler Schilfrohrsänger Erithacus rubecula Robin Rotkehlchen Luscinia megarhynchos Nightingale Nachtigall Luscinia svecica Red-spotted Bluethroat Rotsterniges Blaukehlchen Durchzügler EU-VSR: Anh.1 Oenanthe oenanthe Wheatear Steinschmätzer Phoenicurus ochruros Black Redstart Hausrotschwanz Saxicola rubetra Whinchat Braunkehlchen Saxicola torquata Stonechat Schwarzkehlchen Turdus merula Blackbird Amsel Turdus philomenos Song Thrush Singdrossel Locustella naevia Grasshopper Warbler Feldschwirl Phylloscopus collybita Chiffchaff Zilpzalp Phylloscopus trochilus Willow Warbler Fitislaubsänger Durchzügler Sylvia atricapilla Blackcap Mönchsgrasmücke Sylvia borin Garden Warbler Gartengrasmücke Sylvia curruca Lesser Whitethroat Klappergrasmücke Ficedula hypoleuca Pied Flycatcher Trauerfliegenschnäpper Durchzügler Ficedula semitorquata Semi-collared Flycatcher Halbringfliegenschnäpper Ficedula parva Red-breasted Flycatcher Zwergfliegenschnäpper EU-VSR: Anh.1 Musicapa striata Spotted Flycatcher Grauschnäpper Aegithalos caudatus Long-tailed Tit Schwanzmeise Parus caeruleus Blue Tit Blaumeise Parus major Great Tit Kohlmeise Remiz pendulinus Penduline Tit Beutelmeise Sitta europaea Nuthatch Kleiber Oriolus oriolus Golden Oriole Pirol Lanius collurio Red-backed Shrike Neuntöter EU-VSR: Anh.1 Lanius minor Lesser Grey Shrike Schwarzstirnwürger EU-VSR: Anh.1 Lanius excubitor Great Grey Shrike Raubwürger Durchzügler Corvus corax Raven Kolkrabe Corvus corone cornix Hooded Crow Nebelkrähe Corvus frugilegus Rook Saatkrähe Garrulus glandarius Jay Eichelhäher Pica pica Magpie Elster Sturnus roseus Rose-coloured Starling Rosenstar Sturnus vulgaris Starling Star Passer domesticus House Sparrow Haussperling Carduelis carduelis Goldfinch Stieglitz Fringilla coelebs Chaffinch Buchfink Fringilla montifringilla Brambling Bergfink Durchzügler Emberiza calandra Corn Bunting Grauammer Emberiza melanocephala Black-headed Bunting Kappenammer Emberiza schoeniclus Reed-Bunting Rohrammer
Abkürzungen: BP Brutpaar EU-VSR: Anh.1 EU-Vogelschutzrichtlinie Anhang 1 IUCN World Conservation Union – Red List NT Near threatened VU Vulnerable
Anhang 2: Liste der im Untersuchungsgebiet bei Muganli beobachteten Tiere (außer Vögel)
Wissenschaftlicher Name Deutscher Name Nachweis Kategorie Bemerkungen
Säugetiere
Canis aureus Goldschakal SB häufig bis ins Dorf
Canis lupus Wolf Spuren FFH: Anh. 2 regelmäßig anzutreffen
Cervus elaphus Rothirsch Spuren selten im Auwald
Erinaceus concolor Ostigel Uhugewöll mehrere Funde
Felis chaus Rohrkatze SB häufig bis ins Dorf
Felis silvestris Wildkatze SB wenig Nachweise
Lepus europaeus Feldhase SB selten im Auwald
Lutra lutra Fischotter Spuren IUCN: NT / FFH: Anh.2 an der Kura
Martes martes Baummarder Spuren häufig im Auwald
Meles meles Dachs Spuren; Bau nur vereinzelt
Myocastor coypus Nutria Fraßspuren vereinzelt Fraßplätze
Rattus norvegicus Wanderratte Totfund häufig in Dorfnähe
Sus scrofa Wildschwein Spuren selten im Auwald
Talpa caeca Blindmaulwurf Totfund im Auwald
Amphibien
Rana spp. Grünfrösche SB überall häufig
Bufo viridis Wechselkröte SB Bewässerungskanäle
Hyla arborea Laubfrosch SB IUCN: NT häufig
Reptilien
Emys orbicularis Europäische Sumpfschildkröte SB IUCN: NT / FFH: Anh.2 an Nebenarmen
Mauremys caspica Kaspische Wasserschildkröte SB FFH: Anh. 2 an Nebenarmen
Testudo graeca Maurische Landschildkröte SB IUCN: VU / FFH: Anh.2 ca. 10 je ha
Vipera sp. Otter SB häufig an Gewässern
Natrix natrix Ringelnatter SB häufig
Lacerta spp. Eidechse SB sehr häufig im Kulturland
Anguis fragilis colchicus Blindschleiche SB im Auwald
Pseudopus apodus Scheltopusik SB im lichten Auwald
Insekten
Aegeria apiformis Großer Hornissenschwärmer SB
Argynnis parphia Kaisermantel SB
Calopteryx xanthostoma Südliche Prachtlibelle SB
Cerambyx cerdo Großer Eichenbock SB IUCN: VU alle alten Eichen befallen
Cetonia speciosissima Großer Goldkäfer SB
Gryllotalpa gryllotalpa Maulwurfsgrille SB
Typhoeus typhoeus Stierkäfer SB
Abkürzungen: SB Sichtbeobachtung FFH: Anh.2 Richtlinie 97/62/EG Anhang 2 IUCN World Conservation Union – Red List NT Near threatened VU Vulnerable
Anhang 3: Liste der im Untersuchungsgebiet angetroffenen Gehölze und Lianen
Familie Art Bemerkungen Bäume Aceraceae Acer campestre L. Acer negundo L. Neophyt Anacardiaceae Pistacia mutica Fisch.& Mey. Pflanzung; keine Reproduktion Betulaceae Alnus glutinosa ssp. barbata (C.A.Mey.) Yaltirik Carpinus betulus L. Ebenaceae Diospyros lotus L. Pflanzung, keine Reproduktion Elaeagnaceae Elaeagnus caspica (Sosn.) Grossh. Fabaceae Gleditsia caspica Desf. Pflanzung + Reproduktion Robinia pseudoacacia L. Pflanzung + Reproduktion Fagaceae Quercus castaneifolia C.A.Mey. Pflanzung; keine Reproduktion Quercus robur pedunculiflora (K.Koch) Menitsky Hamamelidaceae Parrotia persica (DC.) C.A.Meyer Pflanzung; keine Reproduktion, selten Juglandaceae Juglans regia L. Pflanzung; keine Reproduktion Moraceae Morus nigra L. nur im Dorf Morus alba L. Pflanzung + Reproduktion Oleaceae Fraxinus excelsior L. Pflanzung; keine Reproduktion Rosaceae Malus orientalis Ugl. Prunus armeniaca L. Pflanzung; keine Reproduktion Prunus avium (L.)L. Pflanzung, keine Reproduktion Pyrus caucasica An.Fed. Salicaceae Populus x canescens (Ait.) Sm. Populus nigra (var. sosnowskyi)(Grossh.) Makaschwili Populus nigra var. italica Münchh. Pflanzung; keine Reproduktion Populus x canadensis Moench Pflanzung; keine Reproduktion Salix alba L. Salix triandra L. nur am Fluß Tiliaceae Tilia begoniifolia Steven Ulmaceae Ulmus minor Mill. em. Richens Ulmus laevis Pallas selten im Auwald Sträucher Berberidaceae Berberis vulgaris L. Betulaceae Corylus avellana L. Celastraceae Euonymus europaeus L. Cornaceae Cornus mas L. Cornus sanguinea australis (C.A.Mey.) Jav. Fabaceae Amorpha fruticosa L. Neophyt Caragana arborescens Lam. Pflanzung Oleaceae Ligustrum vulgare L. Rhamnaceae Frangula alnus Mill. Paliurus spina-christi Mill. Rhamnus pallasii Fisch.&Mey. Rhamnus cathartica L. Rosaceae Crataegus rhipidophylla Gand. z.T. als Baum Cydonia oblonga Mill. Mespilus germanica L. Pyrus sp. Prunus divaricata Ledeb. Prunus persica (L.) Batsch Pflanzung; keine Reproduktion Prunus spinosa L. Rosa canina L. Rubus canescens DC. Salicaceae Salix caprea L. Tamaricaceae Tamarix hohenackeri Bge. Tamarix ramosissima Ledeb. Thymelaceae Daphne axilliflora (Keissl.) Pobed. Ulmaceae Celtis sp. selten Lianen Araliaceae Hedera helix L. Asclepiadaceae Periploca graeca L. Cynanchum acutum L. Cannabaceae Humulus lupulus L. Caprifoliaceae Lonicera caprifolium L. Convolvulaceae Calystegia sepium (L.) R. Br. Ranunculaceae Clematis vitalba L. Smilacaceae Smilax excelsa L. Vitaceae Vitis vinifera sylvestris (C.C.Gmel.) Hegi
Anhang 4: Liste der im Gebiet angetrof-fenen krautigen Pflanzen
Familie Art Alismataceae Alisma plantago-aquatica L. Amaranthaceae Amaranthus sp. Apiaceae Visnaga daucoides Gaertn. Anthriscus cerefolium (L.) Hoffm. Anthriscus sylvestris var. nemorosa (Bieb.)
Berula erecta (Huds.) Coville Bifora radians Bieb. Conium maculatum L. Coriandrum sativum L. Daucus carota L. Eryngium caucasicum Nevski Eryngium campestre L. Falcaria vulgaris Bernh. Macrosciadium alatum (Bieb.)Tichomirov Pimpinella sp. Torilis nodosa (L.) Gaertn. Asclepiadaceae Vincetoxicum scandens S.et L. Asteraceae Achillea micrantha Willd. Achillea millefolium L. Anthemis altissima L. Arctium tomentosum Mill. Artemisia vulgaris L. Carduus crispus L. Centaurea calcitrapa L. Cichorium intybus L. Cirsium arvense (L.) Scop. Conyza canadensis (L.) Cronquist Erigeron annuus (L.) Pers. Filago arvensis L. Inula helenium L. Lactuca serriola L. Lappsana communis L. Leucanthemum vulgare Lam. Onopordum acanthium L.
Scorzonera parviflora Jacq. Senecio vernalis Waldst. et Kit. Silybum marianum (L.)Gaertn. Sonchus arvensis L. Sonchus asper (L.) Hill Sonchus oleraceus L. Taraxacum officinale Wgg. Tragopogon dubius Scop. Tragopogon graminifolius DC. Xanthium strumarium L. Boraginaceae Anchusa azurea Mill. Buglossoides purpurocaerulea (L.) I.M.Johnst. Cynoglossum germanicum Jacq. Cynoglossum officinaleL. Myosotis scorpioides L. Brassicaceae Lepidium crassifolium W. et K. Alliaria petiolata (M.Bieb.) Cavara et Grande Allyssum sp. Barbarea vulgaris W.T.Aiton Capsella bursa-pastoris (L.) Medik. Cardaria draba (L.) Desv. Descurainia sophia (L.) Webb ex Prantl Hymenolobus procumbens (L.) Nutt. ex Torr et
Myagrum perfoliatum L. Nasturtium officinale W.T. Aiton Rorippa palustris (L.) Besser Rorippa sylvestris (L.) Besser Sinapis arvensis L. Sisymbrium loeselii L. Thlaspi perfoliatum L. Butomaceae Butomus umbellatus L. Campanulaceae Campanula sp. Cannabaceae Cannabis sativa spontanea (Vavilov) Serebr. Capparidaceae Capparis spinosa L. Caprifoliaceae Sambucus ebulus L. Caryophyllaceae Arenaria serpyllifolia L. Cerastium semidecandrum L. Cucubalus baccifer L. Holosteum umbellatum L. Moehringia trinervia (L.) Clairv. Myosoton aquaticum (L.) Moench Scleranthus annuus L. Silene wallichiana Klotzsch. Spergularia salina J.Presl et C.Presl Stellaria media (L.) Vill Chenopodiaceae Chenopodium album L. Kochia sp. Salsola sp. Convolvulaceae Convolvulus arvensis L.
Convolvulus lineatus L. Cuscutaceae Cuscuta sp. Cyperaceae Bolboschoenus maritimus (L.) Palla Carex acutiformis Ehrh. Carex diluta M.B. Carex distans L. Carex disticha Huds. Carex divulsa Stokes Carex duriuscula C.A.Mey. Carex elata Bell. Carex melanostachya M.B. Carex muricata L.s.str. Carex otrubae Podp. Carex pseudocyperus L. Carex remota L. Carex riparia Cutis Carex sylvatica Huds. Carex tomentosa L. Cladium mariscus (L.) Pohl Cyperus flavescens L. Cyperus longus L. Cyperus rotundus L. Eleocharis palustris (L.) Roem. Et Schult. Eleocharis uniglumis (Link) Schult. Schoenoplectus lacustris (L.) Palla Schoenoplectus tabernaemontani (C.C.Gmel.) Palla Dipsacaceae Dipsacus laciniatus L. Equisetaceae Equisetum ramosissimum Desf. Equisetum variegatum Schleich.ex Webe et D.
Euphorbiaceae Euphorbia helioscopa L. Euphorbia stricta L. Euphorbia villosa Waldst. et Kit. Euphorbia virgata Waldst.et Kit. Fabaceae Alhagi pseudoalhagi (M.B.) Dsv. Astragalus hamosus L. Astragalus glycyphyllos L. Astragalus sp. Hedysarum sericeum M.B. Lathyrus aphaca L. Lotus tenuis Waldst. et Kit ex Willd. Medicago lupulina L. Medicago minima L. Medicago sativa L. Melilotus officinalis (L.) Lam. Trifolium dubium Sibth. Trifolium hybridum L. Trifolium repens L. Trigonella caerulea (L.) Ser. Vicia sativa L. Vicia villosa Roth Fumariaceae Fumaria schleicheri Soy.-Will. Gentianaceae Centaurium pulchellum (Sw.) Druce Geraniaceae Erodium cicutarium (L.) L'Her. Geranium dissectum Juslen Geranium pusillum L. Haloragaceae Myriophyllum spicatum L. Hypericaceae Hypericum perforatum L. Iridaceae Iris carthaliniae Fomin Iris pseudacorus L. Juncaceae Juncus articulatus L. em. Richt. Juncus compressus Jacq. Juncus inflexus L. Juncaginaceae Triglochin palustre L. Lamiaceae Ajuga genevensis L. Ballota nigra meridionalis (Beg.) Beg. Ballota nigra nigra L. Phlomoides laciniata (L.) R.Kam.& Machmedov Glechoma hederacea L. Lamium amplexicaule L. Lamium purpureum L. Leonurus cardiaca L. Lycopus exaltatus L. Melissa officinalis L. Mentha aquatica L. Mentha longifolia (L.) L. Mentha suaveolens Ehrh. Origanum vulgare L. Prunella laciniata (L.) L. Prunella vulgaris L. Salvia nemorosa L. Salvia viridis L. Lemnaceae Lemna minor L. Liliaceae Asparagus verticillatus L. Asparagus officinalis L. Ornithogalum sp. Gagea sp. Hemerocallis fulva (L.) L. Linaceae Linum austriacum L.
Linum orientale Boiss. Lythraceae Lythrum salicaria L. Malvaceae Abutilon theophrasti Med. Alcea rosea L. Althaea hirsuta L. Lavathera thuringiaca L. Malva neglecta Wallr. Malva sylvestris L. Orchidaceae Anacamptis pyramidalis (L.) Rich. Cephalanthera damasonium (Mill.) Druce Dactylorhiza incarnata (L.) Soo Listera ovata (L.) R.Br. Orchis militaris L. Oxalidaceae Oxalis fontana Bunge Papaveraceae Papaver dubium L. Papaver rhoeas L. Plantaginaceae Plantago lanceolata L. Plantago major L. Plumbaginaceae Limonium scoparium (Pall.) Klok. Poaceae Aegilops triuncialis L. Agropyrum cristatum (L.) Gaertn. Agrostis gigantea Roth Agrostis sp. Alopecurus pratensis L. Alopecurus tiflisiensis (Westb.) A.Grossh. Arundo donax L. Bellardiochloa polychroa (Trautv.) Roshev. Brachypodium sylvaticum (Huds.) P.Beauv. Bromus arvensis L. Bromus commutatus Schrader Bromus sterilis L. Bromus tectorum L. Calamagrostis pseudophragmites (Haller) Koeler Catabrosa aquatica (L.) P.Beauv. Cenchrus catharticus Delile. Cynodon dactylon (L.) Pers. Dactylis glomerata L. Echinaria capitata (L.) Dsf. Elytrigia repens (L.) Desv. Ex Nevski Festuca arundinacea Schreb. Festuca gigantea (L.) Vill. Festuca pratensis Huds. Hordeum leporinum Link Imperata cylindrica (L.) Raeusch. Lolium perenne L. Phalaris arundinacea L. Phalaris canariensis L. Phleum paniculatum Huds. Phragmites australis (Cav.) Steud. Poa angustifolia L. Poa annua L. Poa bulbosa L. Poa compressa L. Poa nemoralis L. Poa pratensis L. Poa trivialis L. Puccinellia distans (Jacq.) Parl. Sclerochloa dura (L.) P.Beauv. Setaria viridis (L.) P.Beauv. Trisetum sp. Vulpia ciliata Dumort. Polygalaceae Polygala anatolica Boiss.et Held. Polygonaceae Fallopia convolvulus (L.) A.Love Persicaria maculosa Gray Polygonum arenastrum Boreau Polygonum aviculare L. Rumex crispus L. Portulacaceae Portulaca oleracea L. Potamogetaceae Potamogeton crispus L. Potamogeton natans L. Primulaceae Anagallis arvensis L. Samolus valerandi L. Ranunculaceae Ranunculus chius D.C. Adonis aestivalis L. Consolida hispanica (Costa) Greuter et Burdet Ranunculus acris L. Ranunculus arvensis L. Ranunculus bulbosus L. Ranunculus illyricus L. Ranunculus repens L. Ranunculus sceleratus L. Ranunculus trichophyllus rionii (Lagger) Soo Thalictrum minus L. Rosaceae Agrimonia eupatoria (L.) Fragaria viridis (Duchesne) Weston Geum urbanum L. Potentilla recta L. Potentilla reptans L.
Rubiaceae Galium rivale (Sibth. et Sm.) Griseb. Galium mollugo L. Galium parisiense L. Galium spurium L. Galium tricornutum Dandy Rubia tinctorum L. Sherardia arvensis L. Scrophulariaceae Scrophularia umbrosa Dumort. Verbascum blattaria L. Verbascum phoeniceum L. Verbascum thapsus L. Veronica arvensis L. Veronica catenata Pennell Veronica hederifolia L. s.str. Veronica polita Fr. Solanaceae Datura stramonium L. Hyoscyamus niger L. Lycopersicon esculentum Mill. Physalis algekengi L. Solanum nigrum L. em. Mill. Solanum persicum W. Sparganiaceae Sparganium erectum erectum L.em. Rchb. Typhaceae Typha angustata Bory et Chaub. Typha angustifolia L. Typha latifolia L. Urticaceae Urtica dioica L. Valerianaceae Valerianella sp. Verbenaceae Verbena officinalis L. Violaceae Viola alba Besser Viola arvensis Murray Viola odorata Ldb. Viola sieheana Beck. Zannichelliaceae Zannichellia palustris L. Zygophyllaceae Peganum harmala L. Algen und Moose Characeae Chara sp. Ricciaceae Riccia fluitans L. Ricciocarpos natans (L.) Corda Amblystegiaceae Drepanocladus aduncus (Hedw.) Warnst.
Anhang 5: Bestandeskenndaten aus der PCQ-Analyse Quercus-Wald
Bestand Crataegus Pyrus Quercus Robinia Anzahl 80 2 1 73 4 Mittlere Entfernung [m] 12,9 Mittlere Höhe [m] 6 6 16 14 Standartabweichung der Höhe 1,0 0,0 4,0 2,5 Mittleres Alter [a] 67 Mittlerer Durchmesser [cm] 18,8 21,6 70,9 40,6 Anteil am Bestand [%] 2,5 1,3 91,3 5,0 Anzahl je Hektar 61 2 1 55 3 Summe der Grundflächen [cm² ] 573 368 321053 5320 Mittlere Grundfläche [cm²] 287 368 4398 1330 Grundfläche je Hektar [m²/ha] 24,8 0,0 0,0 24,3 0,4 Anteil an Bestandeskreisfläche [%] 0,2 0,1 98,1 1,6 Absolute Frequenz 130 10 5 100 15 Relative Frequenz [%] 7,7 3,8 76,9 11,5 Wichtigkeit [I] 10 5 266 18 Origanum-Wald
Bestand Crataegus Diospyros Elaeagnus Gleditsia Malus Pop can Pop nig Quercus Robinia Ulmus Anzahl 120 72 2 2 2 3 5 3 12 3 16Mittlere Entfernung [m] 4,2 Mittlere Höhe [m] 5 8 9 6 6 25 24 11 8 6Standartabweichung der Höhe 1,6 2,5 3,0 1,0 2,4 1,5 0,5 5,1 4,5 2,6Mittleres Alter [a] 38 35 45 Mittlerer Durchmesser [cm] 9,2 16,2 22,3 13,2 8,7 72,9 56,4 47,1 15,7 9,6Anteil am Bestand [%] 60,0 1,7 1,7 1,7 2,5 4,2 2,5 10,0 2,5 13,3Anzahl je Hektar 578 347 10 10 10 14 24 14 58 14 77Summe der Grundflächen [cm² ] 38955 539 923 329 204 20951 7515 31711 1050 1582Mittlere Grundfläche [cm²] 541 269 462 164 68 4190 2505 2643 350 99Grundfläche je Hektar [m²/ha] 49,9 18,8 0,3 0,4 0,2 0,1 10,1 3,6 15,3 0,5 0,8Anteil an Bestandeskreisfläche [%] 52,4 0,7 1,2 0,4 0,3 28,3 10,1 42,8 1,4 2,2Absolute Frequenz 200 97 7 3 3 10 10 7 37 10 43Relative Frequenz [%] 48,3 3,3 1,7 1,7 5,0 5,0 3,3 18,3 5,0 21,7Wichtigkeit [I] 161 6 5 4 8 37 16 71 9 37 Alnus-Bachsaum
Bestand Alnus Corn san Crataegus Morus Quercus Anzahl 16 9 2 2 2 1 Mittlere Entfernung [m] 5,7 Mittlere Höhe [m] 17 4 7 12 16 Standartabweichung der Höhe 6,3 0,5 1,4 7,0 0,0 Mittleres Alter [a] 59 Mittlerer Durchmesser [cm] 34,2 6,5 22,4 25,5 65,3 Anteil am Bestand [%] 56,3 12,5 12,5 12,5 6,3 Anzahl je Hektar 311 175 39 39 39 19 Summe der Grundflächen [cm² ] 11385 67 794 1214 3344 Mittlere Grundfläche [cm²] 1265 34 397 607 3344 Grundfläche je Hektar [m²/ha] 32,6 22,1 0,1 1,5 2,4 6,5 Anteil an Bestandeskreisfläche [%] 68 0 5 7 20 Absolute Frequenz 250 100 50 50 25 25Relative Frequenz [%] 40,0 20,0 20,0 10,0 10,0 Wichtigkeit [I] 164 33 37 30 36 Populus-Weichholzaue
Bestand Pop nig Salix alba Tamarix Anzahl 40 38 1 1 Mittlere Entfernung [m] 5,1 Mittlere Höhe [m] 11 4 2 Standartabweichung der Höhe 3,0 0,0 0,0 Mittleres Alter [a] 15,69121 Mittlerer Durchmesser [cm] 24,7 8,0 4,5 Anteil am Bestand [%] 95,0 2,5 2,5 Anzahl je Hektar 388 368 10 10 Summe der Grundflächen [cm² ] 20494 50 16 Mittlere Grundfläche [cm²] 539 50 16 Grundfläche je Hektar [m²/ha] 19,90 19,87 0,05 0,02 Anteil an Bestandeskreisfläche [%] 99,7 0,2 0,1 Absolute Frequenz 120 100 10 10 Relative Frequenz [%] 83,3 8,3 8,3 Wichtigkeit [I] 278 11 11
Carduus-Wald
Bestand Cor mas Crataegus Elaeagnus Gleditsia Malus Morus Pop can Pyrus Quercus Robinia Ulmus
Anzahl 132 1 39 2 14 4 3 4 7 36 8 13
Mittlere Entfernung [m] 6,0
Mittlere Höhe [m] 3 5 4 9 4,25 7 15 5 17 11 7
Standartabweichung der Höhe 0,0 2,1 0,0 2,6 0,8 2,5 6,4 2,7 3,7 3,2 2,8
Mittleres Alter [a] 33 60
Mittlerer Durchmesser [cm] 3,8 10,5 6,5 11,4 9,9 11,7 63,1 12,7 62,8 15,9 12,8
Anteil am Bestand [%] 0,8 29,5 1,5 10,6 3,0 2,3 3,0 5,3 27,3 6,1 9,8
Anzahl je Hektar 281 2 83 4 30 9 6 9 15 77 17 28
Summe der Grundflächen [cm² ] 11 102551 68 1729 2329 354 22083 23170 138278 1848 25625
Mittlere Grundfläche [cm²] 11 2630 34 124 582 118 5521 3310 3841 231 1971
Grundfläche je Hektar [m²/ha] 67,6 0,0 21,8 0,0 0,4 0,5 0,1 4,7 4,9 29,4 0,4 5,4
Anteil an Bestandeskreisfläche [%] 0,0 16,9 0,0 0,9 0,6 0,2 0,4 3,9 71,3 1,0 4,9
Absolute Frequenz 230 3 61 6 15 12 9 6 15 58 15 30
Relative Frequenz [%] 1,3 26,3 2,6 6,6 5,3 3,9 2,6 6,6 25,0 6,6 13,2
Wichtigkeit [I] 2 73 4 18 9 6 6 16 124 14 28
Tilia-Wald
Bestand Acer Cor mas Crataegus Malus Morus Pop can Pop nig Quercus Robinia Tilia Ulmus
Anzahl 80 2 1 45 1 3 3 1 5 5 4 10
Mittlere Entfernung [m] 3,9
Mittlere Höhe [m] 9 4 6 8 8 28 24 13 12 11 6
Standartabweichung der Höhe 4,5 0,0 2,0 0,0 5,4 2,4 0,0 4,0 2,8 3,8 2,8
Mittleres Alter [a] 52 58 34
Mittlerer Durchmesser [cm] 10,7 7,3 11,6 13,1 17,5 112,7 85,9 38,5 27,4 20,5 14,5
Anteil am Bestand [%] 2,5 1,3 56,3 1,3 3,8 3,8 1,3 6,3 6,3 5,0 12,5
Anzahl je Hektar 669 17 8 376 8 25 25 8 42 42 33 84
Summe der Grundflächen [cm² ] 252 42 26118 134 1047 33359 5801 6364 3796 1581 1845
Mittlere Grundfläche [cm²] 126 42 580 134 349 11120 5801 1273 759 395 184
Grundfläche je Hektar [m²/ha] 67,1 0,2 0,0 21,8 0,1 0,9 27,9 4,8 5,3 3,2 1,3 1,5
Anteil an Bestandeskreisfläche [%] 0,3 0,1 32,5 0,2 1,3 41,5 7,2 7,9 4,7 2,0 2,3
Absolute Frequenz 260 10 5 95 5 10 15 5 25 20 20 50
Relative Frequenz [%] 3,8 1,9 36,5 1,9 3,8 5,8 1,9 9,6 7,7 7,7 19,2
Wichtigkeit [I] 7 3 125 3 9 51 10 24 19 15 34
Alliaria-Wald Bestand Carpinus Crataegus Elaeagnus Euonymus Gleditsia Malus Morus Pop can Pyrus Quercus Robinia Ulmus Anzahl 1 62 1 1 1 3 1 7 2 18 5 18Mittlere Entfernung [m] 3,6 Mittlere Höhe [m] 7 8 3 4 13 8 12 26 5 14 8 8Standartabweichung der Höhe 0,0 3,4 0,0 0,0 0,0 1,4 0,0 2,6 1,0 2,7 2,6 3,2Mittleres Alter [a] 42 32 Mittlerer Durchmesser [cm] 9,9 12,7 4,8 5,4 10,2 14,2 58,9 83,5 6,2 36,5 9,4 13,9Anteil am Bestand [%] 0,8 51,7 0,8 0,8 0,8 2,5 0,8 5,8 1,7 15,0 4,2 15,0Anzahl je Hektar 775 6 400 6 6 6 19 6 45 13 116 32 116Summe der Grundflächen [cm² ] 76 44131 18 23 81 597 2724 40637 69 22246 399 3090Mittlere Grundfläche [cm²] 76 712 18 23 81 199 2724 5805 35 1236 80 172Grundfläche je Hektar [m²/ha] 73,7 0,0 28,5 0,0 0,0 0,1 0,4 1,8 26,2 0,0 14,4 0,3 2,0Anteil an Bestandeskreisfläche [%] 0,1 38,7 0,02 0,02 0,1 0,5 2,4 35,6 0,1 19,5 0,4 2,7Absolute Frequenz 243 3 87 3 3 3 10 3 23 7 40 10 50Relative Frequenz [%] 1,4 35,6 1,4 1,4 1,4 4,1 1,4 9,6 2,7 16,4 4,1 20,5Wichtigkeit [I] 2 126 2 2 2 7 5 51 4 51 9 38
Vincetoxicum-Wald Bestand Cor san Crataegus Diospyros Fraxinus Morus Pop can Pru div Pyrus Quercus Robinia Ulmus Anzahl 140 1 58 1 1 1 36 1 1 11 9 20 Mittlere Entfernung [m] 4,2 Mittlere Höhe [m] 3 7 3 10 8 25 5 10 17 9 9 Standartabweichung 0,0 2,0 0,0 0,0 0,0 5,7 0,0 0,0 3,8 1,8 4,6 Mittleres Alter [a] 31 43 Mittlerer Durchmesser [cm] 4,8 12,7 4,8 20,4 11,1 54,1 6,0 19,1 45,3 9,7 16,9 Anteil am Bestand [%] 0,7 41,4 0,7 0,7 0,7 25,7 0,7 0,7 7,9 6,4 14,3 Anzahl je Hektar 559 4 232 4 4 4 144 4 4 44 36 80 Summe der Grundflächen [cm² ] 18 59452 18 326 97 103608 29 286 27752 780 5646 Mittlere Grundfläche [cm²] 18 1025 18 326 97 2878 29 286 2523 87 282 Grundfläche je Hektar [m²/ha] 80,1 0,0 24,1 0,0 0,1 0,0 41,9 0,0 0,1 11,2 0,3 2,3 Anteil an Bestandeskreisfläche [%] 0,01 30,0 0,01 0,2 0,0 52,3 0,02 0,1 14,0 0,4 2,9 Absolute Frequenz 234 3 77 3 3 3 54 3 3 23 20 43 Relative Frequenz [%] 1,2 32,9 1,2 1,2 1,2 23,2 1,2 1,2 9,8 8,5 18,3 Wichtigkeit [I] 2 104 2 2 2 101 2 2 32 15 35
Abkürzungen: Cor mas Cornus mas Cor san Cornus sanguineaPop can Populus x canescens Pop nig Populus nigra Pru div Prunus divaricata
Anhang 6: Protokolle der Bodenschürfe Nr. K1 Datum 02.04.2005 Höhe NN [m] 254 Terrasse 4
Hochwert 41°20'16,6'' Rechtswert 45°11'16,9'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 3.50
Quercus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L
35 Tu3 3 dbn 4 4 Axh
45 Tu2 2-3 gebn 1 5 Axh/lCc Pseudomycel
60+ Ts2 2 hgebn 0-1 5 lCc
Bodentyp Normtschernosem
Substrattyp Tu3/Ts2
Nr. K2 Datum 02.04.2005 Höhe NN [m] 262 Terrasse 4
Hochwert 41°20'09,1'' Rechtswert 45°11'10,2'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 3.00
Quercus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L
35 Tu3 3 dbn 4 3 Axh
50+ Ts2 1 gebn 1 4 Axh/lCc Durchwurzelung
Bodentyp Normtschernosem
Substrattyp Tu3/Ts2
Nr. K3 Datum 04.04.2005 Höhe NN [m] 253 Terrasse 3
Hochwert 41°20'05,7'' Rechtswert 45°10'44,6'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 0.40
Carex otrubae Rasen
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
10 Tu3 4 dgrbn 4 4 Ah
40 Tl 5 grsw 4 3 Ah-Sg Rostflecken
60+ Ts2 5 gr 2 3 Ah-Go-Sg
Bodentyp Humus-Gley-Haftpseudogley
Substrattyp Tu3/Ts2
Nr. K4 Datum 04.04.2005 Höhe NN [m] 254 Terrasse 3
Hochwert 41°19'58,3'' Rechtswert 45°10'40,1'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 0.30
Carex otrubae Rasen
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
10 Tl 4 dgrbn 4 4 Ah
50 Ts3 5 swbn 3 4 Ah-Sg
55+ Ts3 5 ge/sw 2 4 Go-Sg marmoriert
Bodentyp Humus-Gley-Haftpseudogley
Substrattyp Tl\Ts3
Nr. K5 Datum 05.04.2005 Höhe NN [m] 254 Terrasse 3
Hochwert 41°19'44,3'' Rechtswert 45°10'11,7'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.00
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Eichenlaub
+1 Of
7 Tl 3 dsw 4 3 Axh
35 Ts2 5 dgr 3 4 Axh-Sg
45+ Tu3 5 grge 0 4 Sg Rostflecken
Bodentyp Humushaftpseudogley
Substrattyp Ts\Ts2/Tu3
Nr. K6 Datum 05.04.2005 Höhe NN [m] 256 Terrasse 1
Hochwert 41°19'32,2'' Rechtswert 45°09'48,1'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.00
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+0.5 L
30 Ts2 3 swbn 4 4 Ah
40 Ts2 5 bnge 1 4 Ah-Sg
50+ Ts3 5 ge 0 4 Go-Sg
Bodentyp Gley-Haftpseudogley
Substrattyp Ts2/Ts3
Nr. K7 Datum 05.04.2005 Höhe NN [m] 261 Terrasse 1
Hochwert 41°19'33,2'' Rechtswert 45°09'36,6'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 1.20
Convolvulus Rasen
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
15 Ts3 2 swbn 4 3 Ah
30 Ts3 3 grbn 1 4 Ah-M
60 St3 3 gebn 0 4 M
80 Ts3 4 dbngr 2 4 II fAh-Go
115 Ts3 5 gr / oc 0 4 Go
120+ Ts2 5 gr 0 4 Gr
Bodentyp Gley-Kolluvisol Substrattyp Ts3/St3//Ts3
Bemerkungen Bachufer
Nr. K8 Datum 05.04.2005 Höhe NN [m] 266 Terrasse 1
Hochwert 41°19'34,8'' Rechtswert 45°09'32,9'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.20
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Eichenlaub
+1 Of F-Mull
25 Ts3 3 swbn 3 3 Ah
40 Ts3 3 gegr / swbn 1 4 Ah-lCc
70+ St3 5 gegr / oc 0 4 Go
Bodentyp Pararendzina-Gley
Substrattyp Ts3/St3
Nr. K9 Datum 05.04.2005 Höhe NN [m] 254 Terrasse 0
Hochwert 41°19'29,2'' Rechtswert 45°09'21,6'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.20
Vincetoxicum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+2 L Eichen+Pappellaub
3 Ts4 3 swbn 3 3 aAh F-Mull
30 Tu4 3 grbn 1 4 aM
80+ mSu2 4 gegr 0 4 II aM
Bodentyp Vega
Substrattyp Tu4/mSu2
Nr. K10 Datum 06.04.2005 Höhe NN [m] 244 Terrasse 0
Hochwert 41°19'24,5'' Rechtswert 45°09'21,5'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.50
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Eichen+Pappellaub
+1 Of F-Mull
3 Ut4 3 swbn 4 3 aAh
30 Ut3 3 grge 1 4 aM Wurzeln
75+ Ls4 4 grge 1 5 IIaMc Pseudomycel
Bodentyp Vega
Substrattyp Ut3/Ls4
Nr. K11 Datum 06.04.2005 Höhe NN [m] 254 Terrasse 0
Hochwert 41°19'22,8'' Rechtswert 45°09'14,0'' Vegetationseinheit
Nutzungsgrad 1.5 GW-Tiefe [m] 2.00
Vincetoxicum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Eichen+Pappellaub
+2 Of F-Mull
3 Ut3 3 grbn 3 3 aAh
30 Ut2 3 gegr 1 4 aM Wurzeln
60+ Ts2 3 gegr 1 5 IIaMc Pseudomycel
Bodentyp Vega
Substrattyp Ut3/Ts2
Nr. K12 Datum 06.04.2005 Höhe NN [m] 233 Terrasse 0
Hochwert 41°19'18,6'' Rechtswert 45°09'09,2'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 2.00
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+2 L Eichen+Pappellaub
+1 Of F-Mull
3 Ut3 3 grdbn 3 3 aAh
30 Ut2 3 grbn 1 4 aM Wurzeln
70+ Ls3 3 grbn 1 5 IIaMc Pseudomycel
Bodentyp Vega Substrattyp Ut3/Ls3
Nr. K13 Datum 07.04.2005 Höhe NN [m] 268 Terrasse 0
Hochwert 41°18'41,4'' Rechtswert 45°08'49,7'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 2.00
Vincetoxicum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L
2 Ut3 2 dbngr 3 3 aAh
40 Ut3 3 grbn 1 4 aM
60+ Us 3 gegrbn 0 4 II aM
Bodentyp Vega Substrattyp Ut3/Us
Nr. K14 Datum 07.04.2005 Höhe NN [m] 270 Terrasse 0
Hochwert 41°18'46,1'' Rechtswert 45°08'48,7'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 2.00
Vincetoxicum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+2 L
+1 Of
8 Ut2 3 grbn 2 4 aAh
50 Uu 3 gebn 1 4 aM
60+ Ut2 4 gebn / ok 0 5 aM-Go Pseudomycel
Bodentyp Gley-Vega Substrattyp Uu/Ut2
Nr. K15 Datum 08.04.2005 Höhe NN [m] 260 Terrasse 0
Hochwert 41°19'08,3'' Rechtswert 45°09'40,7'' Vegetationseinheit
Nutzungsgrad 1.5 GW-Tiefe [m] 2.00
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L
+1 Of
6 Ut3 3 bngr 2 3 aAh
35 Ut3 3 gr 1 4 aM viele Wurzeln
50+ Ut2/mG 3 gr 1 4 II aM
Bodentyp Vega
Substrattyp Ut3/mG
Nr. K16 Datum 08.04.2005 Höhe NN [m] 259 Terrasse 0
Hochwert 41°18'56,0'' Rechtswert 45°09'35,3'' Vegetationseinheit
Nutzungsgrad 2.5 GW-Tiefe [m] 2.00
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+0.5 L
18 Ut3 2 dgrbn 4 4 aAh
35 Us 2 grbn 2 4 aAh/aM
53 Us 2 gebn 1 4 aM
70+ Ut3 1 hgr/ok 0 5 aM/Go
Bodentyp Gley-Vega
Substrattyp Ut3\Us/Ut3
Nr. K17 Datum 08.04.2005 Höhe NN [m] 263 Terrasse 0
Hochwert 41°18'50,5'' Rechtswert 45°09'35,4'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.00
Vincetoxicum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Eichen+Pappellaub
+2 Of
9 Tu3 3 bnsw 3 3 aAh
55 Tu3 3 grbn 1 5 aM Pseudomycel
75+ Sl3 4 gegr / ok 0 4 Go
Bodentyp Gley-Vega Substrattyp Tu3/Sl3
Nr. K18 Datum 10.04.2005 Höhe NN [m] 246 Terrasse 0
Hochwert 41°19'00,5'' Rechtswert 45°09'45,3'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.50
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L Eichenlaub
+0.5 Of
3 Tu3 3 swbn 3 4 aAh
35 Tu4 3 gr 1 4 aM
45+ Sl3/gG 3 gr 1 4 II aM Wurzeln
Bodentyp Vega Substrattyp Tu4/gG
Nr. K19 Datum 10.04.2005 Höhe NN [m] 252 Terrasse 0
Hochwert 41°19'01,5'' Rechtswert 45°09'50,9'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 2.00
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+0.5 L Pappellaub
5 Lu 3 swbn 3 4 aAh
40 Lts 3 gegr 1 4 aM
70 Su3 4 gegr 1 4 II aM
80+ Uls/gG 4 gegr 1 4 III aM
Bodentyp Vega Substrattyp Lts/Su3/gG
Nr. K20 Datum 10.04.2005 Höhe NN [m] 257 Terrasse 0
Hochwert 41°18'59,1'' Rechtswert 45°09'51,6'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.00
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+4 L Pappellaub
+3 Of
+1 Oh
4 Tu3 3 swbn 4 3 aAh
32 Lu 3 dgegr 1 4 aM
50 Lu 4 dgegr/ok 1 4 aM-Go
55+ Tl/gG 4 gr/ok 1 4 Go
Bodentyp Vega-Gley Substrattyp Lu/gG
Nr. K21 Datum 10.04.2005 Höhe NN [m] 259 Terrasse 0
Hochwert 41°19'02,7'' Rechtswert 45°09'51,3'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.50
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
11 Ut3 2 grbn 2 4 aAh
30 Lu 3 gegr 1 4 aM Wurzeln
60+ Lu 4 gegr/ok 1 4 aM-Go
Bodentyp Vega-Gley Substrattyp Ut3\Lu
Nr. K22 Datum 11.04.2005 Höhe NN [m] 250 Terrasse 0
Hochwert 41°19'00,6'' Rechtswert 45°09'38,5'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 2.50
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+0.5 L
4 Ut4 2 dgrbn 3 4 aAh
25 Ut3 3 grbn 1 4 aM Wurzeln
40 Sl2 3 grbn 1 4 IIaM
60+ mSu2/gG 3 grbn 1 4 IIIaM
Bodentyp Vega Substrattyp Ut3/Sl2/gG
Nr. K23 Datum 11.04.2005 Höhe NN [m] 267 Terrasse 0
Hochwert 41°18'41,6'' Rechtswert 45°08'54,7'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 2.00
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L
2 Ut3 2 dgrbn 3 3 aAh
40 Tu4 3 grbn 1 4 aM
70+ Sl2 3 grbn / ok 1 4 aM-Go
Bodentyp Gley-Vega Substrattyp Tu4/Sl2
Nr. K24 Datum 11.04.2005 Höhe NN [m] 251 Terrasse 0
Hochwert 41°18'31,2'' Rechtswert 45°09'08,8'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.00
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Pappellaub + Holz
2 Tu4 2-3 dbn 2 4 aAh
55 Sl2 3 gegr/ok 1 4 aM-Go
60+ Sl2/gG 4 gegr 1 4 II aM-Go
Bodentyp Vega-Gley
Substrattyp Sl2/gG
Nr. K25 Datum 12.04.2005 Höhe NN [m] 255 Terrasse 1
Hochwert 41°19'25,6'' Rechtswert 45°09'45,6'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 2.00
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L Eichenlaub
18 Tu3 2-3 dswbn 3-4 3 Axh
27 Tu4 3 swbn/gegr 2 4 Axh-Sg
40 Tu4 3 gegr 1 4 Sg
60+ Tu2 4 gr 1 4 Sg-Go
Bodentyp Gley-Haftpseudogley
Substrattyp Tu4/Tu2
Nr. K26 Datum 13.04.2005 Höhe NN [m] 264 Terrasse 0
Hochwert 41°19'28,6'' Rechtswert 45°09'26,5'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.50
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1.5 L
+0.5 Of
35 Tu3 2-3 swgr 4 3 aAxh
43 Tu4 3 gegr/swgr 1 4 aAxh-aM
55+ Tu4 3 gegr 0 4 aM
Bodentyp Normtschernitza
Substrattyp Tu3/Tu4
Nr. K27 Datum 13.04.2005 Höhe NN [m] 257 Terrasse 0
Hochwert 41°19'35,8'' Rechtswert 45°09'24,6'' Vegetationseinheit
Nutzungsgrad 1.5 GW-Tiefe [m] 1.00
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+3 L Eichenlaub
+2 Of
12 Tu4 3 swgr 3 3 aAh
40 Tu4 3-4 gr 1 4 aM
75+ Su4 4 gegr/ok 1 4 aM-Go
Bodentyp Gley-Vega
Substrattyp Tu4/Su4
Nr. K28 Datum 13.04.2005 Höhe NN [m] 264 Terrasse 0
Hochwert 04°11'91,4'' Rechtswert 45°09'33,0'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.00
Vincetoxicum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+2 L
17 Tu4 2-3 bn 2-3 4 aAh
43 Tu4 3 gr 3 5 aM Pseudomycel
60+ Tu2 4 gegr/ok 4 5 aM-Go
Bodentyp Gley-Vega
Substrattyp Tu4/Tu2
Nr. K29 Datum 13.04.2005 Höhe NN [m] 265 Terrasse 0
Hochwert 41°19'13,4'' Rechtswert 45°09'33,4'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 0.35
Alnus-Bachsaum
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
5 Tu2 4 sw 4 3 Ah-Go
32 Tu3 5 gr/ok 1 3 Go
45+ Tu3 5 gr 1 3 Gr
Bodentyp Normnassgley Substrattyp Tu3
Nr. K30 Datum 15.04.2005 Höhe NN [m] 257 Terrasse 1
Hochwert 41°19'29,0'' Rechtswert 45°09'44,3'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 1.20
Convolvulus-Rasen
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
20 Tu4 2 swbn 4 4 Axh 1x gepflügt
40 Tu4 3 gegr/swbn 2 4 Axh-Sg
55 Tu4 4 gegr/ok 0 4 Sg
65+ Tu4 5 gr/ok 0 4 Sg-Go
Bodentyp Gley Haftpseudogley Substrattyp Tu4
Nr. K31 Datum 15.04.2005 Höhe NN [m] 253 Terrasse 1
Hochwert 41°19'25,1'' Rechtswert 45°09'49,8'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 0.80
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
25 Tu4 2 swbn 4 4 Axh
38 Tu3 3 gegr/swbn 3 4 Axh-lCc (Sg)
42 Tu4 3 gegr 1 4 lCc (Sg)
75 Tl 4 gegr/ok 0 4 Go
80+ Tu4 5 gr/ok 0 4 Go-Gr
Bodentyp Normgley Substrattyp Tu4/Tl
Nr. K32 Datum 15.04.2005 Höhe NN [m] 254 Terrasse 1
Hochwert 41°19'27,9'' Rechtswert 45°09'50,4'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 0.40
Carduus-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
25 Tu2 3 swgr 4 3 Axh
35 Tu4 5 gr/ok 1 4 Go-Sg
40+ Tu4 5 gr 1 4 Go-Gr
Bodentyp Haftpseudogley-Gley
Substrattyp Tu2/Tu4
Nr. K33 Datum 17.04.2005 Höhe NN [m] 256 Terrasse 0
Hochwert 41°19'03,3'' Rechtswert 45°09'27,9'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 0.40
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+1 L Eichenlaub
30 Ut2 2 dbn 4 4 aAxh
38 Ut3 2 bngr 2 5 aAhe-aMe Pseudomycel
60+ Ut2 3 gegr 1 5 aMe
Bodentyp Vega
Substrattyp Ut2/Ut3
Nr. K34 Datum 20.04.2005 Höhe NN [m] 258 Terrasse 1
Hochwert 41°19'36,7'' Rechtswert 45°09'51,8'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.00
Alliaria-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
32 Tu3 3 swbn 4 4 Axh
41 Tu2 3 grbn/ok 2 4 Axh-Go
60+ Tu4 4 gegr/ok 1 4 Go
Bodentyp Tschernosem-Gley
Substrattyp Tu3/Tu4
Nr. K35 Datum 24.05.2005 Höhe NN [m] 242 Terrasse 0
Hochwert 41°16'42,3'' Rechtswert 45°13'35,2'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 2.00
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
14 Uu 2 dbn 4 4 aAh
50+ Uu 3 gebn 1 4 aM
Bodentyp Vega
Substrattyp Uu
Nr. K36 Datum 24.05.2005 Höhe NN [m] 241 Terrasse 0
Hochwert 41°16'37,5'' Rechtswert 45°13'36,1'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 2.00
Origanum-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
7 Sl2 2 bn 3 4 aAh
37+ mS/gG 3 hbn 1 4 aM
Bodentyp Vega Substrattyp Sl2/gG
Nr. K37 Datum 24.05.2005 Höhe NN [m] 240 Terrasse 0
Hochwert 41°16'48,8'' Rechtswert 45°12'57,3'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.50
Tilia-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
13 Sl3 3 dbn 4 4 aAh
40 Sl3 3 grbn 1 4 aM
45+ Ut3 4 gr/ok 1 4 aM-Go
Bodentyp Gley-Vega Substrattyp Sl3/Ut3
Nr. K41 Datum 24.04.2005 Höhe NN [m] 260 Terrasse 0
Hochwert 41°19'01,2'' Rechtswert 45°08'28,5'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.20
Tilia-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
1 Ut2 3 dbn 2 3 aA(i)h
46 Uu 3 bn 1 4 aM
60 mS 4 grbn 1 4 IIaM
65+ mS/gG 4 grbn 1 4 IIIaM
Bodentyp Vega Substrattyp Uu/mS
Nr. K42 Datum 24.04.2005 Höhe NN [m] 256 Terrasse 0
Hochwert 41°19'13,4'' Rechtswert 45°08'21,3'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 1.50
Tilia-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
2 Ut3 3 bn 3 3 aA(i)h
15 Ut3 3 grbn 2 4 aAh-aM
55+ Ut2 3 grbn 1 4 aM
Bodentyp Vega
Substrattyp Ut3/Ut2
Nr. K43 Datum 24.04.2005 Höhe NN [m] 250 Terrasse 0
Hochwert 41°19'20,1'' Rechtswert 45°08'08,5'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.50
Tilia-Wald
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
1 Ut3 2 dbn 3 3 aA(i)h
58+ Ut3 3 grbn 1 4 aM
Bodentyp Vega
Substrattyp Ut3
Nr. K44 Datum 08.05.2005 Höhe NN [m] 255 Terrasse 2
Hochwert 41°19'33,2'' Rechtswert 45°10'02,6'' Vegetationseinheit
Nutzungsgrad 3 GW-Tiefe [m] 1.00
Convolvulus-Rasen
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
15 Ut4 Axh
Bodentyp Gley-Haftnässepseudogley
Substrattyp Ut4
Nr. K47 Datum 28.05.2005 Höhe NN [m] 236 Terrasse 0
Hochwert 41°16'14,8'' Rechtswert 45°14'06,6'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 1.00
Populus nigra Weichholzaue
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
4 Us 2 hgr 1 4 aAi
7 mS 2 bn 2 4 fAih
25+ mS-gG 2 grbn 1 4 aelC
Bodentyp Normrambla Substrattyp mS
Nr. K50 Datum 28.05.2005 Höhe NN [m] 238 Terrasse 0
Hochwert 41°16'24,9'' Rechtswert 45°13'46,3'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 0.40
Tamarix-Weichholzaue
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
45 Su3 2 hgr 1 4 aAi
50+ mS-gG 3 gegr 1 4 aelC
Bodentyp Normrambla Substrattyp Su3/gG
Nr. K51 Datum 28.05.2005 Höhe NN [m] 238 Terrasse 0
Hochwert 41°16'22,9'' Rechtswert 45°13'41,1'' Vegetationseinheit
Nutzungsgrad 1 GW-Tiefe [m] 0.40
Tamarix-Weichholzaue
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
30 Su3 3 gegr 1 4 aelC frisch aufgespült
45+ Su4 4 bngr 1 4 aelC
Bodentyp (Rambla), Auenrohboden Substrattyp Su3/Su4
Nr. K110 Datum 09.05.2005 Höhe NN [m] Terrasse 3
Hochwert 41°19'58,7'' Rechtswert 45°11'01,3'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 0.10
Nasturtium-Sparganium Ried
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
5 Hnr,t 5 robn 5 4 nH Quellkuppe
20+ Tu2 5 gr 1 4 Gr
Bodentyp Nassgley Substrattyp H\Tu2
Nr. K111 Datum 09.05.2005 Höhe NN [m] Terrasse 3
Hochwert 41°19'59,3'' Rechtswert 45°11'02,1'' Vegetationseinheit
Nutzungsgrad 2 GW-Tiefe [m] 0.00
Nasturtium-Sparganium Ried
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
+0.5 L Eichenlaub
35 Hnr,t 5 robn 5 4 nHc Kalkkonkretio.
40+ Tu2 5 swgr 2 4 Gr
Bodentyp Moor-Gley
Substrattyp H/Tu2
Nr. K125 Datum 22.05.2005 Höhe NN [m] Terrasse 3
Hochwert 41°19'56,5'' Rechtswert 45°10'33,9'' Vegetationseinheit
Nutzungsgrad 1.5 GW-Tiefe [m] 0.40
Scorzonera-Wiese
Tiefe [cm] Bodenart Feuchte Farbe Humus CaCO3 Horizont Bemerkungen
34 Tu2 4 swgr 4 4 Ah-Sg
40+ Tu2 4 gr-ok 1 4 Sg-Go Rostflecken
Bodentyp Haftpseudogley-Gley
Substrattyp Tu2
Anhang 7: Vegetationsaufnahmen der Tümpel
Nr.: 69 65 74 63 68 67 61 62 64 70 71 72 73 60 66 DurchschnittDeckung [%] 95 100 50 75 80 95 80 75 20 80 70 30 70 95 100 74Krauthöhe [m] 0,2 0,4 0,2 0,2 0,3 0,3 0,3 0,2 0,3 0,3 0,9 0,2 0,2 0,4 0,2 0,3
Wassertiefe [cm] 30 20 40 30 40 20 40 35 35 35 20 15 15 35 30 29
Stetigkeit [%]
Zannichellia palustris 5 5 1 1 1 4 5 4 2 4 2 + 5 87Carex disticha + 1 2 1 + 1 1 1 1 2 + + 80Agrostis sp. + + 2 + + 1 + + 1 1 67Chara sp. + 1 2 4 4 1 1 4 + 5 67Ranunculus trichophyllus 2 2 5 + + 2 2 1 2 2 67Phragmites australis + 1 + + 2 33Puccinellia distans + + + + + 33Trifolium repens + + + + 27Schoenoplectus tabernaemontani + + 2 2 27Lemna minor + + + 20Ranunculus sceleratus + + + 20Juncus articulatus 1 + 13Catabrosa aquatica + + 13Eleocharis palustris + 7Alopecurus pratensis + 7Eleocharis uniglumis + 7Scorzonera parviflora + 7Sparganium erectum + 7Carex acutiformis + 7Bolboschoenus maritimus + 7Veronica catenata + 7
Related Documents