Philipps-Universität Marburg 03.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf: Vorbereitung: 2 Minuten Durchführung: max. 5 Minuten Nachbereitung: 2 Minuten Reaktionsgleichungen: C H 3 H H OH -I 3 + Cr 2 O 7 2- +VI + 8H + 3 C H 3 O H +I + 2 Cr 3+ +III + H 2 O 7 Chemikalien: Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz: Kaliumdichromatlösung K 2 Cr 2 O 7 (w = 5%) 10 mL 36/37/38- 43-46-49- 50 22-28-45- 53-61 T + ,N Lehrerversuch! Vermutlich cancerogene Wirkung! Schwefelsäure H 2 SO 4 (konz.) 5 mL 35 26-30-45 C Sek. II Ethanol C 2 H 5 OH Ca. 10 mL 11 7-16 F Sek.I www.chids.de: Chemie in der Schule

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

Philipps-Universität Marburg 03.01.2008
Organisches Grundpraktikum (LA)
Katrin Hohmann
Assistent: Beate Abé
Leitung: Dr. Ph. Reiß
WS 2007/08
Gruppe 6, Alkohole
Versuch: Alkoholtest mit Dichromat
Zeitbedarf:
Vorbereitung: 2 Minuten
Durchführung: max. 5 Minuten
Nachbereitung: 2 Minuten
Reaktionsgleichungen:
CH3
H
H
OH-I3 + Cr2O7
2-+VI
+ 8 H+ 3 CH3
O
H
+I + 2 Cr3++III
+ H2O7
Chemikalien:
Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz:
Kaliumdichromatlösung
K2Cr2O7 (w = 5%)
10 mL 36/37/38-
43-46-49-
50
22-28-45-
53-61
T+, N Lehrerversuch!
Vermutlich
cancerogene
Wirkung!
Schwefelsäure H2SO4
(konz.)
5 mL 35 26-30-45 C Sek. II
Ethanol C2H5OH Ca. 10 mL 11 7-16 F Sek.I
www.chids.de: Chemie in der Schule

Geräte:
Petrischale
Pinzette
Becherglas
Spatel
Rundfilter
Versuchsdurchführung:
Zu 10 mL Kaliumdichromatlösung (A) in einem Becherglas gibt man 5 mL konzentrierte
Schwefelsäure. Die entstehende heiße Lösung wird in eine Petrischale gegossen. Zur besseren
Sichtbarkeit der Effekte stellt man diese entweder auf den Overheadprojektor oder auf ein
weißes Blatt Papier. Anschließend tränkt man den Rundfilter in Ethanol, lässt ihn abtropfen
und hält ihn mit der Pinzette dicht über die Petrischale (B).
(A) (B)
Beobachtung:
Die orangene Dichromatlösung verfärbt sich nach intensiv
dunkelgrün:
Entsorgung:
Die Lösungen werden neutralisiert in die anorganischen Schwermetallabfälle gegeben.
www.chids.de: Chemie in der Schule

Fachliche Analyse:
Alkohole sind oxidierbar. Hält man zum Beispiel ein mit schwarzem Kupferoxid überzogenes
Kupferblech in Ethanol, so wird das Blech wieder rot glänzend. Kupfer(II)-Ionen wurden also
reduziert, Ethanol wurde oxidiert zu Ethanal:
CH3
OH+ CuO CH3
O
H+ Cu
-I +II +I 0
+ OH2
Analog wird 2-Propanol zu Aceton oxidiert:
CH3
CH3
OH
+ CuO CH3
CH3
O
+ + OH2Cu0 +II +II 0
Tertiäre Alkohole können ohne Bindungsbruch nicht oxidiert werden:
CH3
CH3
CH3
OH + CuO
Im Versuch fand die Oxidation zu Ethanal mit Dichromat statt, die man rein formal so
formulieren kann:
Oxidation:
CH3
H
H
OH CH3
O
H
+ 2 H+ 2 e
-+
+I
+I
+I
-II-I
-II
+I
+I
Ethanol Ethanal
www.chids.de: Chemie in der Schule

Reduktion:
Cr2O72- + 6 e
-14 H
++ 2 Cr3+
H2O7++VI-II +III
Dichromatorange
Chrom (III)grün
Redox:
CH3
H
H
OH-I3 + Cr2O7
2-+VI
+ 8 H+
3 CH3
O
H
+I + 2 Cr3+
+III+ H2O7
Hinter dieser Redoxreaktion steckt ein zweistufiger Reaktionsmechanismus. Durch die
Reaktion von Ethanol mit Chromsäure entsteht ein Chromsäureester:
CH3
OH+ Cr OH
O
OH
O +VICH3
O+ CrOH
O
H OH
O- CH3
O Cr
OH
O
O+ OH2
ChromsäureChromsäureester
Zwischenstufe
+VI
Im zweiten Schritt fungiert das gebildete Wasser als milde Base und spaltet das dem
Sauerstoffatom benachbarte Wasserstoffatom ab. Es entsteht dabei eine instabile Chrom(IV)-
Verbindung, die zu Chrom(III) und Chrom(V) disproportioniert oder weiter zu vollständig zu
Chrom(III) reduziert wird. Bei diesem Reaktionsschritt handelt es sich formal um eine
Eliminierung (E2):
CH3
O Cr
OH
O
O
HH
OH2
CH3
O
H+ H3O
+ ++I
Ethanal
O-
Cr O
OH
+IV
www.chids.de: Chemie in der Schule

Durch Angriff von Wasser wird das Ethanal hydratisiert und kann dann analog zum obigen
Reaktionsmechanismus zur Carbonsäure oxidiert werden:
CH3
O
H+ OH2 CH3
H
OH
OHH2CrO4
CH3
O
OH+III
Ethansäure
Eigentlich wurde Kaliumdichromat verwendet. Das Dichromation steht bei einem pH-Wert
zwischen 2 und 6 mit dem HCrO4- -Ion im Gleichgewicht. Bei einem pH = 1 liegt
überwiegend die Chromsäure H2CrO4 vor. Der saure pH-Wert entsteht durch die Zugabe von
konzentrierter Schwefelsäure.
Dieses Verfahren fand früher unter dem Namen „Alcotest“ in Verkehrskontrollen zur
Messung des Blutalkoholspiegels Verwendung.
Mit Hilfe einer Messskala konnte die Konzentration abgelesen werden.
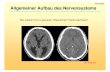
Heute werden sie kaum noch verwendet, da elektronische Alkotester
genauer arbeiten. Durch Pusten in das Röhrchen verfärbt sich das
orangene Dichromat deutlich grün, wie auch im Bild links zu erkennen
ist.
Schon geringer Alkoholkonsum hat Auswirkungen auf den Körper.
Schon bei Konzentrationen von unter 0,2 ‰ ist eine verstärkte Redseligkeit zu verzeichnen,
bis hin zu Gleichgewichtsstörungen,
Erbrechen, Herz-Kreislauf-Problemen und sogar zum Tod (über 4 ‰).
Alkohol wird schon im Mund über die Mundschleimhaut resorbiert und durch den
Blutkreislauf im Körper verteilt. Die weitere Resorption erfolgt über den gesamten
Verdauungstrakt. Das Enzym Alkoholdehydrogenase in der Leber erledigt den Abbau zu
Acetaldehyd, der wiederum durch die Acetaldehyddehydrogenase zu Essigsäure oxidiert wird.
Die Essigsäure wird durch die Atmungskette und den Citratzyklus im Körper
verstoffwechselt.
www.chids.de: Chemie in der Schule

Methodisch-didaktische Analyse:
Einordnung:
Die Oxidation der Alkohole gehört als wichtige Reaktion zum Themenkomplex Alkanole.
Dieser Komplex kann alternativ zu den Alkanen als Einstieg in die Kohlenstoffchemie in
Klasse 10 behandelt werden, wird jedoch spätestens in der Kohlenstoffchemie I in der 11.
Jahrgangsstufe angesprochen.
Dieser Versuch und die damit verbundenen fachlichen Hintergründe stehen wohl eher am
Ende der Unterrichtseinheit und bieten eine ideale Überleitung zur Chemie der Aldehyde und
Ketone. Als Vorwissen benötigen die Schüler Kenntnisse über die Redoxchemie, die jedoch
ausreichend vorher in Klasse 10 behandelt werden sollte. Ungewöhnlich wird zunächst die
Erkenntnis sein, dass auch organische Verbindungen oxidiert oder reduziert werden können,
was aber mit dem bereits Bekannten gut verknüpft werden kann. Als kleiner Vorversuch oder
als Demonstration könnte die im fachlichen Hintergrund genannte Reaktion mit Kupferoxid
dienen, da hier die bekannte Reduktion des Kupferions deutlich zu sehen ist und somit nur
den Schluss auf Oxidation des Alkohols zulässt.
Wichtig ist hier vor allem auch die Erwähnung der praktischen Anwendung in Form von
Alkotests. Spätestens hier sollten die physiologischen Wirkungen von Alkohol besprochen
werden, was auch gut in Form von Referaten oder Gruppenarbeiten bei ausreichender Zeit
geschehen kann.
Aufwand:
Dieser Versuch ist sehr gut geeignet für den Einsatz in der Schule, da er unkompliziert
vorzubereiten ist und auch schnell durchgeführt werden kann. Die Verfärbung des Dichromats
erfolgt deutlich und schnell, sodass bei diesem Versuch eigentlich nichts schiefgehen dürfte.
Zu beachten ist hier allerdings, dass dieser Versuch aufgrund des Einsatzes von
Kaliumdichromat nur als Lehrerversuch durchgeführt werden darf, da von diesem Stoff
vermutlich eine cancerogene Wirkung ausgeht!
Es werden für den Versuch keine außergewöhnlichen Chemikalien verwendet und er ist
denkbar einfach in der Durchführung.
www.chids.de: Chemie in der Schule

Durchführung:
Wie schon angesprochen, ist dieser Versuch aufgrund seiner Effekte der ideale Schulversuch,
der allerdings nur als Lehrerversuch durchgeführt werden darf!
Von diesem Versuch gibt es einige Variationen, wie zum Beispiel der Versuch „Pulsierende
Amöben“ oder auch das Bauen eines eigenen Alkoteströhrchens, die ähnlich gut
funktionieren. Sinnvoll wäre im Unterricht die Demonstration der Funktionsweise eines
Alkoteströhrchens, zum Beispiel an einem Schüler, der vorher ein Mon Chéri gegessen hat.
Dies kann sowohl als Einführung vorher oder auch als praktische Anwendung nachher stehen.
Problematisch wird dabei wohl eher die Beschaffung des Röhrchens sein, da diese heute
kaum noch erhältlich sind.
Literaturangaben:
http://dc2.uni-bielefeld.de/
http://www.axel-schunk.de/ experiment/edm0607.html
www.chempage.de (Bild)
Vollhardt, K.P.C., Schore, N.E., Organische Chemie, 4. Aufl., Wiley-VCH Weinheim, 2005
Soester Liste
Hessischer Lehrplan Chemie für den gymnasialen Bildungsgang, Klasse 7G bis 12G
www.chids.de: Chemie in der Schule
Related Documents