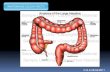
Trato Gastrointestinal Esôfago / Estômago Cólon-reto Dr Fabio Kater

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

Trato GastrointestinalEsôfago / Estômago
Cólon-reto
Dr Fabio Kater

De quem estamos falando?

Cancer de esôfago
Keynote 028
• Estudo de fase Ib
• 83 pacientes selecionados para expressão PD-L1 ( critério de inclusão)
• N= 23 pacientes PD-L1+
• Endpoint primário: taxa de resposta
Doi T, J Clin Oncol 2018, 36: 61-7

Cancer de esôfago
Keynote 028
Doi T, J Clin Oncol 2018, 36: 61-7

Cancer de esôfago
Keynote 028
Doi T, J Clin Oncol 2018, 36: 61-7
Tempo para resposta de 3,7 mesesDuração de resposa de 15 meses
Taxa de resposta: 30%

Câncer de esôfago
• Fase 2, multicêntrico, aberto e de braço único ( n=65)
• Avaliou a eficácia de Nivolumab 3mg/kg a cada 2 semanas
• Espinocelular de esôfago
• 68% ≥ 3linhas
• Endpoint primário: taxa de resposta
ONO-4538
Kang T, Lancet Oncol 2017, 18: 631-9
Taxa de resposta: 17%

Câncer de esôfagoKeynote-180
Shah MA, ASCO 2018 #
• Pacientes em 3ªlinha de esôfago metastático• Espino / Adeno / Adeno Siewert 1 de JEG
• Diferente do KN-28 – pacientes não selecionados para PD-L1 e após 2 linhas de tratamento
• Endpoint primário: taxa de resposta

Câncer de esôfagoKeynote-180
Shah MA, ASCO 2018 #
52% CEC48% Adeno
CPS>10: 48%
85% 3ªlinha
N= 121
KN28: 75%CEC

Câncer de esôfagoKeynote-180
Shah MA, ASCO 2018 #
Taxa de resposta: 10%

Câncer de esôfagoKeynote-180
Shah MA, ASCO 2018 #

Câncer de esôfagoKeynote-180
Shah MA, ASCO 2018 #
• Repostas duráveis em população altamente tratada
• Benefício independe:• Tipo histológico • Status PD-L1

Caracterização molecular - TCGA

Keynote -12 : Cancer Gástrico
57% 3 ou mais linhas

Keynote -12 : Cancer Gástrico

Attraction -2
Kang YK, The Lancet 2017, 360: 2461-71

Attraction -2
Kang YK, The Lancet 2017, 360: 2461-71
82%3 ou mais linhas

Attraction -2
Kang YK, The Lancet 2017, 360: 2461-71

Attraction -2
Kang YK, The Lancet 2017, 360: 2461-71
Taxa de resposta 11,2%37%

Checkmate-032 – combinação N1/I3
Janjigian Y et al. ASCO 2017; Le D et al. ASCO GI 2016

Checkmate-032
Janjigian Y et al. ASCO 2017; Le D et al. ASCO GI 2016
1/3 para 1,2 ou 3 linhas

Checkmate-032
Janjigian Y et al. ASCO 2017; Le D et al. ASCO GI 2016

Checkmate-032
Sobrevida global conforme status do PD-L1
Janjigian Y et al. ASCO 2017; Le D et al. ASCO GI 2016

Keynote-059
Fase II multicoorte de pembrolizumab em Cancer gástrico / JEG

Keynote-059
≥2ªLinha mono
Coorte 1
Fuchs C, JAMA Oncol. 2018;4(5):e180013
Estudo de 3ªlinha

Keynote-059: ≥2ªLinha mono
- 42,6% de redução no tamanho da lesão- Tempo para resposta 2,1 meses- Duração mediana de resposta de
8,4 meses
Fuchs C, JAMA Oncol. 2018;4(5):e180013

Keynote-059: ≥2ªLinha mono
Sobrevida livre de progressão Sobrevida Global
2 meses 5,6 mesesSG12m: 23,4%
Fuchs C, JAMA Oncol. 2018;4(5):e180013

Keynote-059
Coorte 2 – 1ª Linha com quimio

Keynote-059
Coorte 2 – 1ª Linha com quimio – taxa de resposta

Keynote-059
Coorte 3 – 1ªlinha mono

Keynote-059
Coorte 3 – 1ªlinha mono
Catenacci DV, Annals of Oncology, Volume 28, Issue suppl_3, 1 June 2017

Pembrolizumab vs Paclitaxel for Previously Treated Advanced Gastric or Gastroesophageal Junction Cancer: Phase 3 KEYNOTE-061 Trial

Slide 21

KEYNOTE-061 Study Design (NCT02370498)
2ªlinha

Baseline Characteristics
Presented By Kohei Shitara at 2018 ASCO Annual Meeting

Overall Survival, CPS ≥1
Co-primary end-point

Overall Survival by ECOG PS
Presented By Kohei Shitara at 2018 ASCO Annual Meeting

Overall Survival by PD-L1 CPS
Presented By Kohei Shitara at 2018 ASCO Annual Meeting
18% of patients

Response Rate and Duration, CPS ≥1<br />(RECIST v1.1, BICR)

OS, ORR, and DOR for MSI-H Tumorsa

Summary of Exposure and Adverse Events:<br />Total Population
Presented By Kohei Shitara at 2018 ASCO Annual Meeting

Em resumo – uso em linhas subsequentes
• KN28
• CEC
• PDL1+
• KN180
• CEC
• All comers
Esôfago
• KN12 – basket trial
• KN59 – fase 2
• 3 coortes
• Benefício em 2ªlinha mono PD-L1+
• ONO 4538 – fase 2 ( Nivo)
• CM32 – fase 2
• Nivo e Nivo + Ipi
• Attraction – fase 3
• Nivo ≥ 2ª linha
• Vs placebo
• KN61 – fase 3
• Pembro ≥ 2ª linha
• Vs paclitaxel
Estômago
RG30%
RG10%
RG22%
RG11,5%(22%)
RG11,2%
RG12% e 24%
RG11,2%
RG15%

Câncer Cólon-retal

Imunogenicidade da instabilidade MS
• Instabilidade determina células com mutações
→ não reconhecidas como self : imunogênico

Slide 6

Câncer Colorretal
• Mutações somáticas levam à proteínas mutantes que sãoreconhecidas como antígenosimunogênicos “não-próprios”
• Tumores com deficiência MMR tem10 – 100 mais mutações somáticasque os proficientes
• Infiltração linfocitária proeminente
• Postulou-se que tumores deficientesem MMR teriam maiorsuscetibilidade à bloqueioimunológico de chekpoint
N Engl J Med. 2015 Jun 25;372(26):2509-20

Câncer Colorretal
Câncer Colorretal Câncer não-Colorretal
Coorte ADeficient in Mismatch
Repair* (n = 11)
Coorte BProficient in Mismatch Repair
(n = 21)
Coorte CDeficient in Mismatch Repair
(n = 9)
• Anti-PD1 (Pembrolizumabe) 10 mg/kg a cada 2 semanas
• Endpoint primário: SLP imune e taxa de resposta
N Engl J Med. 2015 Jun 25;372(26):2509-20
Desenho do estudo
*avaliação por PCR

Keynote 16 – características da população
Le D at al. NEJM; ASCO Annual Meeting 2016.
jovens
Predominante hepáticoPolitratado
Hereditário

Câncer ColorretalResultados
N Engl J Med. 2015 Jun 25;372(26):2509-20
MMR-deficiente CRC
MMR-proficiente CRC
MMR-deficiente non-CRC
N 10 18 7
ORR 40% 0% 71%
DCR 90% 11% 71%

Câncer Colorretal
N Engl J Med. 2015 Jun 25;372(26):2509-20
NR
2,2m
NR
5,0m
5,4mNR

Keynote 16 – Avaliação de reposta Dados atualizados
Le D at al. NEJM; ASCO Annual Meeting 2016.
(50)



ORR=32%


Resposta independente da expressão do PD-L1

Durability of Nivolumab Benefit in dMMR mCRC





Resposta independente do status do PD-L1


Checkmate 142
Redução da lesão alvo em pacientes com MSI - H



Keynote 164
Caracterísitcas dos pacientes

Keynote 164
Taxa de resposta: 32%

Keynote 164
Sobrevida livre de progressão: 4,1 meses Sobrevida global: não alcançada Sobrevida em 1 ano: 76%

Slide 22

Conclusão
Estudos Taxa de resposta
Keynote 16 (Pembro) 40 ( 50)%
Keynote 164 (Pembro) 32%
Checkmate 142 (Ipi + Nivo) 55%
• Em pacientes com alta taxa de instabilidade de microssatélite
• Após falha de quimio

Obrigado
Related Documents