Ministère de l'Enseignement Supérieur République de Côte d' Ivoire Union - Discipline - Tr a vail , 1' 1\ . l:.J-t ,..11 L:. NANGUIABROGO Université Nangui Abrogoua U F R d e s Science s d e l a N a t ure DEA de Gestion et Valorisation des Ressources Naturelles Option : Biologie et Protec t ion des végétaux Thème: Diversité moléculaire et phylogénie de Cucumi s mel o subsp. agresti s (L.) Naudin (Cucurbitaceae) Présenté par Angui Chia Michelle VaJérie Mémoire soutenu le 04 Janvier 20 l3 devant le jury composé de : Président: Directeur Scientifique: Examinateur: Rapporteur : Prof esseur Tra Bi Fezan Honora Prof esseur Zoro Bi I rié Arsène Prof esseur D jè Koffi Marcellin Prof esseur Adépo-Gourène A B.

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

Ministère de l'Enseignement Supérieur République de Côte d'Ivoire Union - Discipline - Travail
, 1'1\. l:.J-t,..11 L:. NANGUIABROGO
Université Nangui Abrogoua
UFR des Sciences de la Nature
DEA de Gestion et Valorisation des Ressources Naturelles
Option : Biologie et Protection des végétaux
Thème:
Diversité moléculaire et phylogénie de Cucumis melo subsp. agrestis (L.) Naudin
(Cucurbitaceae)
Présenté par Angui Chia Michelle VaJérie
Mémoire soutenu le 04 Janvier 20 l3 devant le jury composé de :
Président:
Directeur Scientifique:
Examinateur:
Rapporteur :
Professeur Tra Bi Fezan Honora
Professeur Zoro Bi Irié Arsène
Professeur Djè Koffi Marcellin
Professeur Adépo-Gourène A B.

DEDICACE
A tous ceux qui m'ont transmis leur savoir et leur passion.
Il

REMERCIEMENTS
Ce document est un mémoire réalisé en vue de l'obtention du Diplôme d'Etudes
Approfondies de Biologie et Protection des Végétaux. Il rentre dans le cadre d'un projet de
recherche intitulé "Valorisation des cultures vivrières mineures de la Côte d'Ivoire : cas des
pistaches (Cucurbitacée à graines consommées en sauce)". Supervisé par la Commission
Universitaire pour le Développement (CUD) et financé par la Coopération Belge au
Développement (DGCD), ce projet est piloté par l'Université Nangui Abrogoua (UFR des
Sciences de la Nature) en partenariat avec la Faculté Universitaire des Sciences
Agronomiques de Gembloux (UER de Phytotechnie Tropicale et d'Horticulture). Que les
autorités de ces institutions soient remerciées.
Au terme de la rédaction, je tiens à exprimer ma reconnaissance à toutes les personnes
qui, de près ou de loin, ont contribué à l'accomplissement de ce travail.
Je tiens à remercier particulièrement:
Le Professeur Zoro Bi Irié Arsène, pour la confiance qu'il m'a accordée pour la
réalisation de ce travail, ainsi que pour sa disponibilité. Profonde gratitude.
Aux membres du jury, pour leurs critiques, suggestions et la portée scientifique à
l'élaboration de ce document.
Aux Docteurs Koffi Kouamé Kévin, Kouassi Kouadio Ignace, Kouakou Kouakou
Laurent, pour l'aide précieuse lors des manipulations au laboratoire et pour la rédaction de ce
document.
Aux Doctorants Yao Koffi Bertin, Goré Bi Boh Nestor, Béket Bonny Sévérin,
Gnamien Yah Gwladys, pour leur aide pour la réalisation de ce travail et pour tous ces
moments de bonne humeur passés.
À Mme Djanbra Opportune, pour son accueil et pour l'aide inestimable apportée lors
de ma prospection effectuée à Agbaou. A Kobé Chévri pour m'avoir guidé au cours de mes
recherches.
À Mr Aka Denis et à toute sa famille à Assié-Kournassi, je ne sais par quels mots vous
exprimer ma profonde gratitude. Que Dieu tout-puissant vous le rende au centuple.
À Mr Amon Pierre et sa famille ainsi qu'à Mr Yapi Julien à Yakassé-Mé, merci
infiniment pour votre disponibilité et votre soutien.
Au chef du village d' Ananda et à toute sa famille, au chef du village d' Assabli
Komenank:ro, à Mme Ani Suzanne et à Mr Kouomenan Frédéric à Kouakoussekro, merci
pour toute 1 'aide apportée.
111
1

À Mme Kouadio Cécile à M'Bahiakro, merci tantie, que Dieu guide tes pas et soit ton
bouclier et ta force. Au commandant Assiri Tanoh Maximin, pour toute l'aide apportée.
À mes chers amis prospecteurs, à Ouattara Djoudjo, Gbotto Anique, pour la bonne
ambiance vécue. À mon père et ma mère, pour leur soutien inconditionnel et leur bienveillance. Toute
ma reconnaissance et tout mon amour. À mes amis, Amangoua Ferdinand, Konan Jacky, N'Gaza Félicité, Doubi Bi Serge,
Guiraud Brigitte, Kouassi Franck, pour toute votre aide et votre disponibilité.
À tous ceux qui m'ont apporté leur soutien et dont j'ai oublié de citer le nom, que Dieu
vous bénisse.
IV

RESUME
L'espèce Cucumis melo est une importante plante cultivée dans le monde. Celle-ci est
subdivisée en deux sous-espèces : la sous-espèce melo et la sous-espèce agrestis. Plusieurs
études moléculaires de la diversité génétique ont été réalisées sur cette espèce. Mais la
classification de certaines variétés reste controversée, surtout pour les types cultivés en
Afrique. Dans la présente étude, les marqueurs ISSR ont été utiJisés pour évaluer la diversité
génétique entre deux variétés de l'espèce Cucumis melo subsp. agrestis cultivée en Côte
d'Ivoire. Les relations phylogénétiques de ces deux variétés avec d'autres variétés de melons
ont été également évaluées.
Vingt et une (21) accessions ont été sélectionnées dont 16 accessions des deux variétés
"légume" et "oléagineuse" et 5 accessions des autres variétés du melon (momordica,
cantalupensis, flexuosus, dudaim, inodorusy. Les quatre amorces utilisées ont produit 82 loci
ISSR. Une forte similarité a été établie entre les variétés: par contre entre les accessions une
grande diversité génétique a été observée.
Les relations phylogénétiques établies et I' AFD (Analyse Factorielle Discriminante) ont
permis de regrouper les différentes accessions. Les relations phylogénétiques ont permis de
mettre en évidence deux (2) grands groupes. Quant à I' AFD trois (3) groupes se sont
distingués. Les résultats des analyses moléculaires n'ont pas permis de différencier les
variétés "légume" et "oléagineuse" ni également d'élucider la phylogénie de ces deux variétés
avec les autres variétés de melons utilisés dans cette étude.
Mots-clés : Cucurbitaceae, Cucumis melo subsp. agrestis, Caractérisation moléculaire. ISSR
Diversité génétique, Phylogénie.
V

LISTE DES TABLEAUX ET DES FIGURES
TABLEAUX
Tableau 1: Liste des accessions 14
Tableau 2: Liste des amorces sélectionnées 17
Tableau 3: Nombre d'amorces, pourcentage des Loci polymorphes généré par amorce et PlC
par amorce 19
Tableau 4: Poids moléculaire (pb) et nombre de loci amplifiés par amorce chez les 21
accessions de melons 21
Tableau 5: Analyse de la variance moléculaire (AMOY A) testant la différenciation génétique
de 21 accessions de Cucumis melo selon les variétés et les zones de collecte Erreur!
Signet non défini.
FIGURES
Figure 1: Zone d'amplification des marqueurs ISSR 5
Figure 2: Fruits et graines de deux variétés de Cucu mis melo subsp. agrestis 8
Figure 3: Localisation des zones de collectes des accessions échantillonnées en Côte d'Ivoire
...................................................................................................................................... 13
Figure 4: Graines des sept variétés de melons utilisées dans cette étude 15
Figure 5: Polymorphisme (présence / absence) révélé par amplification de l'amorce
(AC)8YC chez 16 individus de melons 20
Figure 6: Mise en évidence des groupes d'individus identifiés à partir de I' AFD portant sur
21 accessions de Cucumis melo 25
Figure 7: Dendrogramme obtenu par la méthode de Ward pour la différenciation génétique
basé sur la distance de Jaccard des marqueurs ISSR entre 21 accessions de Cucumis
melo 27
Figure 8: Relations phylogénétiques entre les 103 individus de melons révélés par la méthode
UPGMA basée sur les coefficients de dissimilarités 28
VI

LISTE DES ABREVIATIONS
AFD: Analyse Factorielle Discriminante
AFLP: AmpLified Fragment Lenght Polymorphism
AMOVA: Analyse de la Variance Moléculaire
FAO: Food and Agriculture Organisation of the United Nations
ISSR: Inter Simple Sequence Repeats
PCR: Polymerase Chain Reaction
PIC: Polymorphism Information Content
RAPD: Randomly Amplified Polymorphie DNA
RFLP: Restriction Fragment Length Polymorphism
SSR: Simple Sequence Repeats
UPGMA: Unweight Pair-Group Mean Analysis
VII

TABLE DES MATIERES
DEDICACE 11
REMERCIEMENTS ID
RESUME V
LISTE DES TABLEAUX ET DES FIGURES VI
LISTE DES ABREVIATIONS VIl
INTRODUCTION 1
GENERALITES 3
1.1. !MPORTANCE DES RESSOURCES PHYTOGENETIQUES 3 1.2. MARQUEURS DE DIVERSITE GENETIQUE 3 1.2.1. Marqueurs morphologiques 3 1. 2. 2. Marqueurs protéiques 4 1.2.3. Marqueurs moléculaires 4
1.3. LE MELON (CUCUMJSMEW) 6 1.3.1. Origine et distribution géographique 6 J.3.2. Taxonomie 6 1.3.3. Problématique de la phylogénie du melon 9 1.3.4. Diversité génétique du melon 9
2. MATERIEL ET METHODES 13
2.1. MATERIEL VEGETAL 13 2.2. METHODES 16 2. 2.1. Préparation des échantillons 16 2.2.2. Extraction de l'ADN 16 2. 2. 3. Quantification l 6 2. 2. 4. PCR et électrophorèse l 7 2.2.5. Analyse statistique des données 18
3. RESULTATS ET DISCUSSION 19
3.1. RESULTATS 19 3.1.1. Polymorphisme des loci 19 3.1.2. Structure de la diversité génétique des variétés 22 3.1.3. Relations phylogénétiques 26
3 .2. DISCUSSJON 29
CONCLUSION ET PERSPECTIVES ..........•.................................................................... 31
REFERENCES BIBLIOGRAPIDQUES 32

INTRODUCTION
Selon la FAO (FAO, 2009), près de 873 millions de personnes sont malnutries dans le
monde. D'ici l'an 2050, la population mondiale pourrait atteindre les 10 milliards de
personnes. Cette croissante augmentation de la population aura pour corollaire un grand
nombre de personnes malnutries. En Afrique, par exemple au Sud du Sahara, la production
annuelle de céréales qui représentait 1,9 % de la production mondiale en 1970 est passée à
0,66% en 1990. Cette baisse de production est due, entre autres, à la diminution de la fertilité
du sol et aux pratiques culturales (G:ruhn et al., 2000). Dans les années à venir, l'humanité
sera confrontée à un problème de disponibilité des ressources alimentaires, face à une
population mondiale en constante évolution. L'amenuisement des terres arables disponibles
ainsi que les faibles ressources en eau supplée par la baisse des productions agricoles font de
la sécurité alimentaire un défi majeur en ce 21 ième siècle (Cakmak, 2002).
L'importance de l'agriculture dans la gestion d'une sécurité alimentaire durable,
nécessite des programmes visant l'amélioration des productions agricoles et la conservation
des ressources phytogénétiques. Ces ressources, à travers la diversité génétique sont
essentielles pour l'avenir de l'humanité. La compréhension de la distribution et de l'ampleur
de la diversité génétique des espèces est primordiale pour leur conservation et leur utilisation
efficace et efficiente. L'étude de la diversité génétique permettra une bonne compréhension de
la taxonomie, de l'origine et de l'évolution des plantes (Rao & Hodgkin, 2002). Parmi ces
plantes, celles négligées ou sous-utilisées et désignées sous le vocable de plantes mineures ou
orphelines occupent une place importante. Les cucurbitaceae oléagineuses sont prisées pour
leur huile obtenue à partir des graines et utilisées pour préparer les sauces. Leurs graines sont
riches en lipides et en protéines (Loukou et al., 2007). La valorisation des cucurbitaceae peut
contribuer à améliorer la qualité de l'alimentation. Par ailleurs, les cucurbites ont de
nombreuses potentialités agronomiques et économiques. Elles sont bien adaptées à différents
agroécosystèmes et à plusieurs systèmes de cultures (Chweya & Eyzaguirre, 1999).
L'augmentation de la production des cucurbites pourrait être une solution au problème de la
sécurité alimentaire et également augmenter le revenu des paysans.
En Côte d'Ivoire, des missions de prospection et de collecte ont permis d'identifier dans
plusieurs zones de production, cinq espèces (Zoro Bi et al., 2003) parmi lesquelles Cucumis
melo subsp. agrestis (L. Naudin) ou melon africain. Deux variétés de melon africain ont été
identifiées. Ces plantes se différencient par la couleur des baies matures, des graines et

surtout par l'usage qu'on en fait. En effet, l'une des variétés, ceUe dont la baie mature a la
couleur jaune, est consommée à l'état frais, comme légume dans les sauces à cuire. Par contre,
la deuxième variété, dont les baies matures restent vertes avec des rayures jaunes, contient des
graines oléagineuses, de taille relativement grande. Ces graines séchées et transformées en
pâte servent à préparer les sauces dites "sauce pistache". Les baies de ces deux variétés
produites en Côte d'Ivoire sont de petites tailles. Le poids d'une baie varie entre 27,22 g et
51,04 g, avec une valeur moyenne de 41,39 ± 15,24 g pour la variété oléagineuse et de 84, 76
± 70,5 g pour la variété consommée en légume (Djè et al., 2006a; Angui, 2008 ). Il existe,
cependant, une grande diversité morphologique au sein de l'espèce. L'amélioration du
rendement des types ivoiriens requiert donc des croisements inter-variétaux. Cela suppose,
non seulement, une bonne connaissance de la diversité génétique, mais, également, de la
phylogénie. Or, la phylogénie des types ivoiriens de l'espèce C. melo fait actuellement l'objet
de beaucoup de controverse (Achigan-Dako & Baudoin, 2007). Une clarification de la
phylogénie de ces deux variétés s'avère nécessaire.
Nous nous sommes fixés comme objectif, d'évaluer la différenciation génétique au sein
des variétés ivoiriennes de l'espèce Cucumis melo subsp. agrestis.
Pour ce faire, nous allons procéder à: (1) l'évaluation de la diversité génétique des
variétés de Cucumis melo subsp. agrestis produites en Côte d'Ivoire, par l'utilisation des
marqueurs ISSR; puis à (2) l'étude de la phylogénie des deux variétés par référence à des
variétés de melon dont la phylogénie a déjà fait l'objet d'études approfondies.
La première partie de cette étude est consacrée aux généralités sur Cucumis melo. La
seconde partie présente le matériel et les méthodes utilisés. Ensuite, les résultats obtenus sont
présentés et discutés dans une troisième partie qui sera suivie de la conclusion et des
perspectives.
2

GENERALITES
1.1. Importance des ressources pbytogénétiques
Les ressources génétiques locales demeurent la base du développement agricole et
socio-culturel de l'homme. Celles qui servent à l'alimentation et à l'agriculture constituent la
base biologique de la sécurité alimentaire mondiale. La nature a fournit à l'homme de milliers
d'espèces animales et végétales qui lui procurent gracieusement tout ce dont il a besoin pour
se nourrir, se vêtir, se soigner et se loger. De ce fait, les ressources génétiques en général et
les ressources phytogénétiques en particulier sont fondamentales pour l'alimentation. le bien
être et la santé des populations. C'est pourquoi, leur conservation ou préservation et leur
utilisation 'durable est indispensable. Grâce à l'agriculture traditionnelle, plusieurs plantes sont
produites en zones rurales. Ces plantes de grande importance et souvent méconnues servent à
l'alimentation d'une proportion croissante de la population mondiale (Malice & Baudoin,
2009). Certaines de ces plantes, considérées comme des plantes mineures ou sous-utilisées
sont d'une grande importance pour les agriculteurs et pour les consommateurs. En effet,
celles-ci jouent un rôle important dans la sécurité alimentaire, la nutrition et les revenus des
paysans. C'est le cas par exemple de trois espèces mineures à tubercules cultivées dans les
agrosystèmes traditionnels andins: Oxalis tuberosa, Ullucus tuberosus et Tropaeolum
tuberosum (Malice & Baudoin, 2009); d'une légumineuse du genre Lathyrius, cultivé en
Turquie comme plante fourragère et utilisé dans le Sud del' Asie dans l'alimentation humaine
(William & Haq, 2002). Les plantes mineures ou sous-utilisées présentent une grande
diversité génétique. Compte tenu du potentiel génétique de ces plantes, la mise au point de
stratégies de conservation des ressources génétiques pour une utilisation rationnelle et efficace
par les généticiens, agronomes, naturothérapeutes s'avère nécessaire. La mise au point de ces
stratégies passe nécessairement par plusieurs étapes, entre autres, par l'évaluation de la
diversité génétique.
1.2. Marqueurs de diversité génétique
Les outils utilisés dans les études de diversité génétique se classent généralement en
trois groupes: les marqueurs morphologiques, les marqueurs protéiques et les marqueurs
moléculaires (Roux, 1987).
1.2.1. Marqueurs morphologiques
Les marqueurs morphologiques ont été utilisés dans les premiers travaux de
classification et d'identification des espèces. Les études morphologiques sont toujours basées
3

sur des caractères qualitatifs et quantitatifs prédéfinis par l'expérimentateur. Les marqueurs
morphologiques nécessitent un équipement simple et constituent la mesure la plus directe du
phénotype. L'étude de la diversité de plusieurs plantes dont les cucurbites par les marqueurs
morphologiques a été réalisée. C'est le cas de Citrullus lanatus (Maggs-Kolling et al., 2000),
Lagenaria siceraria (Koffi et al., 2009) et de Cucumeropsis mannii (Koffi et al., 2008). Les
différentes études menées par ces auteurs montrent que les cultivars de cucurbites se
différencient sur la base des critères morphologiques établis par Jes agriculteurs. En outre, ces
études ont permis de proposer des stratégies de conservation de ces différentes espèces.
1.2.2. Marqueurs protéiques
Les marqueurs protéiques basés sur le polymorphisme des protéines de réserve ou des
enzymes sont de nature codominantes. Les acides aminés des chaînes polypeptidiques
peuvent s'ioniser en solution. Les protéines acquièrent alors une charge électrique. Celles-ci
se déplacent en fonction de leur charge et de leur masse dans un substrat poreux (gel
d'amidon ou d'acrylamide). Divers types d'enzymes codées par des loci distincts peuvent
avoir la même activité catalytique; on parle d'isozymes. Pour un locus particulier, si un gène
mute à un codon, modifiant la charge de la protéine, un nouvel allèle (allozyme) est obtenu
(Pasteur et al., 1987).
L'électrophorèse des protéines présente cependant certains inconvénients. En effet
l'électrophorèse ne révèle qu'un nombre réduit de locus. Les protéines ne reflètent que la
variation de la région codante du génome qui représente seulement 5 à 20% du génome. Les
variations dans la majeure partie du génome restent donc inaccessibles. En outre,
l'électrophorèse des protéines montre un niveau de polymorphisme relativement faible. En
effet, il est observé que la variation est plus faible pour un gène codant que pour )'ADN non
codant. Le polymorphisme observé à l'aide des protéines s'avère donc très limité. Cependant,
les marqueurs protéiques restent encore très utilisés chez les plantes cultivées en général et les
cucurbites en particulier (Djè et al., 1998; Koffi et al., 2008; Koffi et al., 2009).
1.2.3. Marqueurs moléculaires Les marqueurs moléculaires, directement issus du polymorphisme existant au niveau
de l' ADN, sont fréquemment utilisés pour l'analyse des ressources génétiques et dans les
programmes d'amélioration des plantes (Santoni et al., 2000). Leur mode d'expression sur gel
d'électrophorèse, lié à la procédure de leur mise en évidence, permet de les séparer en deux
famitJes. La première est constituée par les marqueurs codominants dont les plus courants
4

sont les marqueurs RFLP (Restriction Fragment Length Po/ymorphism) et les microsatellites.
La seconde famille est constituée par les marqueurs dominants. Ce sont, entre autres, les
marqueurs RAPD (Randomly Amplified Polymorphie DNA), les AFLP (Amplified Fragment
Lenght Poiymorphismy et les ISSR (Inter Simple Sequence Repeats). La méthode ISSR est utilisée au cours de cette étude.
Comme indiqué par la figure 1, la méthode ISSR est une technique qui utilise la PCR
pour amplifier des séquences d'ADN entre deux locus microsatellites (Zietkiewicz et al.,
1994). Les amorces utilisées peuvent être des di-nucléotides, tri-nucéotides, tétra-nucléotides
ou penta-nucléotides qui sont non marquées ou marquées à l'extrémité 3' ou 5' (Gupta et al.
1994). Les amorces permettent de produire plusieurs dizaines de produits qui sont visualisés
soit sur des gels d'agarose, soit sur des gels d'acrylamide. Les marqueurs ISSR sont très
polymorphes. Ils permettent de distinguer des variétés génétiquement très proches (Santoni et
al., 2000). La méthode ISSR peut être appliquée sur un taxon pour lequel des informations sur
les séquences spécifiques ne sont pas disponibles. La mise en œuvre de la technique ISSR est
simple et rapide. Cependant, les marqueurs ISSR sont des marqueurs dominants qui
nécessitent de I' ADN de très bonne quai ité.
Les marqueurs ISSR sont d'utilisation courante pour l'évaluation de la diversité génétique
du maïs (Kantety et al., 1995), pour l'identification de cultivar de colza et de pomme de terre
(Charters et al., 1996; Bornet et al., 2002). En outre, des marqueurs ISSR ont été employés
pour caractériser des collections de ressources génétiques conservées dans des banques de
gènes (Blair et al., 1999) et aussi pour identifier des cultivars étroitement liés (Fang & Roose,
1997).
amorces ISSR
microsatellites Figure 1: Zone d'amplification des marqueurs ISSR (Djè et al., 2006b)
5

1.3. Le melon (Cucumis melo)
1.3.J. Origine et distribution géographique
L'origine du melon est controversée. U serait d'Afrique ou du sud de l'Asie (Pitrat et
al., 1999). En effet, des échantillons ont été retrouvés dans les régions sahélo-soudaniennes
d'Afrique. Toutefois, c'est en Asie que l'on trouve une grande diversité du melon (Pitrat et
al., 1999)
Il aurait été domestiqué depuis 3000 ans avant Jésus-Christ (AJ.C). En Inde, sa
culture remonterait à 2000 ans A.J.C. Le melon s'est, ensuite, répandu à travers le monde.
1.3.2. Taxonomie
Le melon, Cucumis melo (2n = 2x = 12), est une plante de la famille des
Cucurbitacées. Il est l'un des fruits légumes les plus cultivés dans des régions tropicales et
tempérées. Il se caractérise par une très forte variabilité au niveau des caractères
morpbologiques et physiologiques tels que la couleur, la taille et le goût du fruit (Yashiro et
al., 2005). L'espèce C. melo est subdivisée en deux sous-espèces : la sous-espèce agrestis et la
sous-espèce melo (Pitrat, 2008).
Sur la base de certains critères comme les traits du fruit, C. melo subsp. melo a été
initialement subdivisée en dix groupes ou variétés botaniques par Naudin (Naudin, 1859).
Cette classification a été révisée par Munger et Robinson (1991) qui ont défini sept groupes
ou variétés botaniques au sein de la sous-espèce. Ceux-ci proposent des désignations
trinomiques (c'est-à-dire C. melo agrestis, C. melo flexuosus, etc.). Les deux sous-espèces
incluent, respectivement, cinq et onze variétés. La sous-espèce agrestis inclut, entre autre,
conomon Thunberg et momordica Roxburgh, et la sous-espèce melo inclut cantalupensis
Naud., inodorus Jacquîn,flexuosus L., dudaim L., et chito Morren (Pitrat, 2008).
Des morpbotypes économiquement important de melons sont généralement divisés
en classe selon leurs attributs culinaires (Staub et al., 2000). Par exemple Je groupejlexuosus
(snake melon), le groupe conomon (Oriental, Pickling melon et Chinese white cucumber), le
groupe cantalupensis (CantaJoupe ou muskmelon, Earl's, House, Galia, Charentais et Ogen),
le groupe inodorus (winter melon, Honeydew et Casaba), le groupe chito (mango melon) et le
groupe dudaim (Queen's pocket melon) (Staub et al., 2004; Nakata et al., 2005). Deux
morphotypes botaniques de l'espèce Cucumis melo subsp. agrestis ont été décrits en Côte
d'Ivoire (Djè et al., 2006a).
6

Le premier, dont les graines sont oléagineuses, a des fruits qui restent vert pâle à
maturité avec une chaire non aromatisée et amère. Les graines de cette variété sont un peu
plus grosses que celle de la seconde variété et sont de couleur blanche.
Le second, la variété dont les fruits sont consommés en légume, a des fruits qui
deviennent orange à maturité avec une odeur aromatisée. Les graines de cette variété sont de
petite taille et de couJeur jaunâtre (Figure 2).
En Côte d'Ivoire, les graines de Cucumis melo subsp. agrestis de la variété oléagineuse
sont utilisées pour préparer les sauces. L'autre variété dont les fruits à maturité sont orange,
sert de légume à l'état immature en tant que substitut des aubergines, au cours de périodes
prolongées de disette, dans certaines régions du sud de la Côte d'Ivoire (Djè et al., 2006a).
7

Figure 2: Fruits et graines de deux variétés de Cucumis melo subsp. agrestis. a : fruits de la
variété oléagineuse en culture; b: graines de la variété oléagineuse ; c: fruits de la variété
consommée en légume à maturité; d: graines de la variété consommée en légume.
8

1.3.3. Problématique de la phylogénie du melon
La phylogénie se définit comme l'étude de la formation et de l'évolution des
organismes vivants en vue d'établir leurs parentés (Santoni et al., 2000; L6pez-Sesé et al.
2002). Une phylogénie est souvent représentée par un arbre phylogénique. Pour reconstituer
les liens de parentés entre êtres vivants, la phylogénie se base sur deux approches: la
phénétique et la cladistique. L'étude de la phylogénie de plusieurs plantes ont été menée
(Berthou, 1983; Terauchi et al., 1992; Nakazawa et al., 1997). Ces études ont permis soit de
ranger les espèces étudiées dans le même groupe que certaines espèces sauvages, indiquant
ainsi leur lien de parenté comme c'est le cas chez le caféier (Berthou, 1983). Dans certains
cas, elle a permis de confirmer les études antérieurement menées sur la classification de
certaines espèces. C'est l'exemple de Chrysosplenium de la famille des Saxifragaceae
(Nakazawa et al., 1997). Enfin, elle a permis de déterminer l'origine de certaines plantes dont
l'igname (Terauchi et al., 1992).
Plusieurs études ont été menées afin d'examiner la phylogénie des variétés de melons
(Staub et al., 2004; Yashiro et al., 2005). Ces études ont essentiellement concernées les
melons de types occidentaux et asiatiques. La phylogénie des melons africains et
particulièrement ceux de la Côte d'Ivoire ont fait l'objet de peu d'études. Celles menées sur la
phylogénie des variétés de l'espèce C. melo cultivée en Côte d'Ivoire font l'objet de
controverse (Achigan-Dako & Baudoin, 2007). En effet, selon ces auteurs, l'espèce Cucumi
melo subsp. agrestis est bien présente en Côte d'Ivoire selon la base de données du
Département d' Agriculture des Etats-Unis (USDA). Celle-ci se rencontre sur les terrains
vagues, autour des agglomérations, dans les jachères cultivées, les savanes herbeuses ou
arbustives. En outre, selon Achigan-Dako et Baudoin (2007), l'espèce décrite par Djè et al.
(2006a) se rapproche plus de la sous-espèce melo que de la sous-espèce agrestis. U serait plus
indiqué pour eux de dire qu'il existe une variété cultivée de l'espèce C. melo en Côte d'Ivoire.
La présente étude basée sur des marqueurs moléculaires devrait donner plus de précision sur
la phylogénie des deux variétés du melon africain cultivées en Côte d'Ivoire.
1.3.4. Diversité génétique du melon La diversité génétique du melon a été évaluée à l'aide de plusieurs types de marqueurs
moléculaires (les isozymes, les RFLP, les RAPD, les AFLP et les SSR).
Akashi et al. (2002) ont évalué la diversité génétique au sein des melons de l'Est et du
Sud del' Asie par J'analyse des isozymes. Ils ont montré que les melons de l'Inde avaient une
grande diversité génétique par rapport à ceux de l'Est del' Asie. Leurs résultats ont en outre
9

montré une différenciation entre les melons analysés. Cette séparation basée sur la taille des
graines montre une différenciation entre le groupe Conomon var. makuwa et var. conomon
(4,5-8,5 mm) et les melons cultivés en Inde (4,0-13,0 mm).
Silberstein et al. (1999) ont utilisé des marqueurs RFLP pour étudier la variation
moléculaire au sein de l'espèce Cucumis melo L. Un sous-ensemble de huit variétés a ainsi été
analysé avec des sondes de Pstl. Parmi les 56 sondes examinées avec six enzymes de
restriction, environ 80% de polymorphisme a été détecté sur les huit accessions. Il s'est avéré
que le génome du melon contient d'abondants sites de restriction de l'enzyme PstI, et
qu'EcoRI était l'enzyme de restriction la plus productive car elle détecte un polymorphisme
élevé au sein du melon.
Stephansky et al. ( 1999) ont évalué la diversité intraspécifique du melon Cucumi s
melo. La technique RAPD a été utilisé à cet effet. Les analyses ont révélé une plus grande
diversité entre les cultivars nord-américains et européens de cantalupensis et d'inodorus qui
ont constitué un groupe, et les variétés "exotiques": conomon, chito, dudaim, agrestis et
momordica, un deuxième groupe.
Mliki et al. (2001) ont évalué la diversité génétique du melon Cucumis melo au sein
des germoplasmes africains à l'aide des marqueurs RAPD. Les analyses ont permis de
distinguer deux groupes à partir des accessions de références. La différenciation génétique
observée entre les pools géniques africains est associée à la proximité géographique des pays
africains. De plus les résultats indiquent que la diversité génétique des accessions de référence
de l'Europe et des Etats-Unis (cantalupensis et inodorus) peut être accrue par l'introgression
des accessions africaines.
Lopez-Sésé et al. (2003) ont réalisé des travaux sur la diversité génétique des melons
espagnols. Ceux-ci ont utilisé des marqueurs moléculaires de référence et des accessions de
diverses origines pour cette étude. Les résultats des marqueurs RAPD révèlent que les
accessions de melons espagnols (essentiellement inodorus) sont génétiquement différents des
accessions de référence et des autres variétés d'inodorus de diverses origines. Plusieurs
accessions africaines possèdent une affinité génétique et forment un groupe associé aux
variétés conomon et chito examinés dans cette étude. Un fort taux de polymorphisme a été
détecté entre les melons originaires du centre de l'Espagne.
Une autre étude a été menée par Tanaka et al. (2007) avec ces mêmes marqueurs sur le
melon du Sud et de l'Est de l'Asie. Une grande diversité génétique a été observée au sein des
accessions indiennes et une faible diversité au sein du groupe Conomon var. makuwa et var.
conomon de l'Est del' Asie. Les résultats montrent clairement une différence génétique entre
10

les melons du Sud de l'Asie en fonction de la taille des graines et que les melons de petite
taille de l'Est de l'Asie sont étroitement liés au groupe Conomon var. makuwa et var.
conomon. En outre, Yi et al. (2009) ont évalué la diversité moléculaire des races locales de
melon (Cucumis melo) de Myanmar à partir des RAPD. lis ont ainsi classé le matériel analysé
en 6 groupes majeurs. Les résuJtats indiquent aussi qu'il existe une grande diversité génétique
des melons indiens à Myanmar.
Plusieurs études ont été menées à partir des AFLP pour l'évaluation de la diversité au
sein du melon.
Yashiro et al. (2005) ont aussi utilisé les marqueurs AFLP pour évaluer la diversité
génétique des melons de l'Est et du Sud de l'Asie. Les analyses ayant porté sur les 99
accessions ont permis de révéler trois grands groupes : le groupe des plantes à graines de
petites tailles; Je groupe des cultivars F1 et le groupe des plantes à graines de grandes tailles.
Les résultats ont révélés que les melons originaires d'Inde ont une très grande variabilité
génétique.
Les marqueurs SSR ont aussi été utilisés pour évaluer la diversité génétique au sein de
1 'espèce Cucumis melo. Plusieurs études ont été initiées à cet effet.
Katzir et al. (1996) ont initié une recherche afin d'évaluer le degré de polymorphisme
des marqueurs SSR du melon et d'autres espèces de la famille des Cucurbitacées. Aussi. ont
ils évalués la possibilité d'utiliser ces amorces SSR dans d'autres genres ou des espèces de
Cucurbitacées. Sept marqueurs SSR ont été employés et cinq des sept marqueurs ont détecté
du polymorphisme parmi les 8 génotypes de melons utilisés. Les amorces SSR spécifiques
des espèces C. melo et C. sativus peuvent être utilisées pour l'amplification de l' ADN extrait
des génotypes des autres genres de la famille des Cucurbitacées tels que Citrullus sp,
Cucurbita sp.
Monforte et al. (2003) ont évalués la diversité génétique d'une collection de 27
accessions de melon (Cucumis melo) par les SSR. Cette collection est constituée d'une large
gamme de melons sauvages et cultivés. Les analyses ont révélés une séparation des accessions
en deux principaux groupes qui correspondent aux deux sous-espèces: agrestis et melo.
Il ressort de cette revue bibliographique que le melon est l'une des cucurbites qui
regroupe en son sein une grande diversité génétique. Les différentes études menées par
l'utilisation des marqueurs moléculaires portent souvent sur les melons de types occidentaux
et orientaux. Très peu d'études ont été portées sur les types africains (El Tahir & Taha Yousif,
11

2004). Cependant, Mliki et al. (2001) ont utilisé les marqueurs RAPD pour l'évaluation de la
diversité génétique des melons africains. Ceux-ci ont montré que les accessions africaines ont
une grande diversité génétique et pourraient servir à accroître la diversité des accessions de
l'Europe et des Etats-Unis.
12

2. MATERIEL ET METHODES
2.1. Matériel végétal
Seize accessions des deux variétés de l'espèce Cucumis me/o subsp. agrestis, cultivées
en Côte d'Ivoire, ont été utilisées dans cette étude. Ces accessions ont été coUectées au Nord,
à l'Est et au Sud du pays (Figure 3). Les échantillons ont été coUectés au cours d'une
prospection de juin à septembre 2009. En outre, 5 autres variétés de melons obtenues de
l'Université de Çukurova (Turquie) ont été incluses dans cette étude. Ce sont les variétés
momordica, cantalupensis, flexuosus, dudaim et inodorus. Au total 21 accessions représentant
sept variétés ont été utilisées dans cette étude (Tableau 1). Chacune de ces variétés représente
une accession. Les graines de chaque variété sont présentées par la figure 4.
Korhogo •
Yamoussoukro •
Yamoussoukro
• Ouélé • Daoukro
Bongouanou • Akoupé •
Figure 3: Localisation des zones de collectes des accessions échantillonnées en Côte d'Ivoire
13

Tableau 1: Liste des accessions utilisées dans notre étude
Accessions Espèces Types Origine N
NI435 C.melo subsp. agrestis Légume Akoupé 5
NI452 C.melo subsp. agrestis Légume Akoupé 5
Nl445 C.melo subsp. agrestis Légume Yakassé-Mé 5
N1447 C.melo subsp. agrestis Légume Yakassé-Mé 5
Nl453 C.melo subsp. agrestis Légume Bongouanou 5
NI454 C.melo subsp. agrestis Légume Bongouanou 5
NI455 C.melo subsp. agrestis Oléagineux Korhogo 5
Nl456 C.melo subsp. agrestis Oléagineux Korhogo 5
NI460 Cmelo subsp. agrestis Oléagineux M'Bahiakro 5
Nl461 C.melo subsp. agrestis Oléagineux M'Bahiakro 5
Nl469 C.melo subsp. agrestis Oléagineux Bongouanou 5
NI475 C.melo subsp. agrestis Oléagineux Bongouanou 5
Nl463 C.melo subsp. agrestis Oléagineux Daoukro 5
Nl464 C.melo subsp. agrestis Oléagineux Daoukro 5
NI466 C.melo subsp. agrestis Oléagineux Ouéllé 5
NI467 C.melo subsp. agrestis Oléagineux Ouéllé 5
NI481 Cucumis melo Momordica Turquie 3
Nl480 Cucumis melo cantalupensis Turquie 5
NI484 Cucumis melo Flexuosus Turquie 5
NI482 Cucumis melo Dudaim Turquie 5
N1479 Cucumis melo Inodorus Turquie 5
N: Nombre d'individus analysés
14

Figure 4: Graines des sept variétés de melons utilisées dans cette étude
a: var. momordica; b: var. inodorus ; c: var.jlexuosus d: var. cantalupensis, e: var.dudaim
f: Cucumis melo subsp. agrestis (légume); g: Cucumis melo subsp. agrestis (oléagineuse)
15

2.2. Méthodes
2.2.1. Préparation des échantillons
Cinq graines ont été sélectionnées pour chaque accession, et semées en milieu naturel.
103 échantillons de feuilles ont été prélevés sur des plantules ayant atteint l'étape de 2 à 3
feuilles. Ces prélèvements ont eu lieu très tôt le matin (entre 6h et 7h30) ou en début de soirée
(après 18h). Ensuite, ces échantillons ont été mis dans des tubes Eppendorf puis gardés dans
la glace et conservés dans le cryoconservateur (-80°C) jusqu'au moment de l'extraction des
feuilles.
2.2.2. Extraction de I' ADN
L' ADN génomique a été extrait à partir des fragments de feuilles en suivant le
protocole de Dellaporta et al. (1983) avec de légères modifications. Les fragments de feuilles
ont été broyés avec des micropilons directement dans les tubes Eppendorf contenant de
l'azote liquide. Ensuite, du SDS (Sodium Désoxyl Sulfate) à 10 % à raison de 150 µI puis 800
µJ de tampon d'extraction et 4 µl de 2-~-mercaptoéthanol (sous une hotte) ont été ajouté au
broyat. Le tampon est composé de Tris-Hel 1 M, NaCI 5 M, l % de PVP et de 0,5 M de
EDT A. Le broyat a été conservé au bain marie à 65 °C pendant au moins 30 min en agitant
par inversions chaque 10 min. L'acétate de potassium 5 M à raison de 250 µla été ajouté puis
chaque tube a été agité au moins six fois par inversion. Les tubes sont ensuite gardés dans le
congélateur (-20°C) pendant 30 min suivie d'une centrifugation à 12000 trs/min (tpm)
pendant 20 min à température ambiante. Le surnageant (800 µl) a été récupéré dans un tube
Eppendorf et complété avec 700 µI d'isopropanol puis agité par inversion. Ensuite les tubes
sont placés au congélateur (-20 °C) pendant 1 h pour que l' ADN précipite. En outre, ceux-ci
sont centrifugés pendant 10 min à 12000 trs/min (tpm). Après, l'ADN a été essoré par
retournement du tube Eppendorf sur du papier absorbant pour l'élimination du surnageant.
Enfin l'ADN a été lavé avec 500 µI d'isopropanol puis centrifugé à 12000 trs/min (tpm)
pendant 4 min à 4 °Cet séché à l'étuve à 37 °C pendant 30 min. L' ADN est conservé à -20°C
dans 100 µl de tampon Tris-EDTA (TE) composé du Tris-Hel 10 Mm pH 8.0 et de l'EDTA 1
mM pH 8,0 jusqu'au moment de l'amplification.
2.2.3. Quantification L' ADN extrait a été quantifié en réalisant une électrophorèse sur gel d'agarose à 0,8 %
soumis à 90 V pendant 1 h. Le tampon d'électrophorèse Tris-Borate EDTA (TBE) 1 Mm pH
8,0 a été utilisé. Le Standart Smart LadderTM qui donne des bandes dont l'intensité peut-être
corrélée à une concentration d'ADN a été utilisé pour la quantification.
16

2.2.4. PCR et électrophorèse
Les amplifications (PCR) ont été effectuées dans un volume réactionnel de 9, 7 µl.
Cette quantité est constituée de 0,2 µl de Taq polymérase (Eurogentec), 1 µI de tampon PCR
(Eurogentec), 0,4 µl de dNTPs à 2 mM (Eurogentec), 0, 16 µ1 d'amorces ISSR, 1,5 µl d'extrait
d'ADN et 6,44 µI d'eau distillée stérile. Quatre amorces ont été testées sur cinq individus par
accession (Tableau 2). Deux amorces ont été testées simultanément sur le même gel. Chaque
cycle PCR a comporté une phase de dénaturation de l' ADN double brin (5 min à 95 °C) 36
cycles de [30 s à 95 °C (dénaturation del' ADN), 45 s à une température Ta qui a varié selon
l'amorce (hybridation des amorces), 2 min à 72 °C (élongation) et 5 min à 95°C (élongation
finale)].
Chaque produit d'amplification a été soumis à une électrophorèse à 90 V pendant 1 b
45 min appliquée à un gel d'agarose dans du tampon TBE. Les fragments d'ADN ont été
révélés à l'aide de 4,9 µl/350 mL de bromure d'éthidium de concentration 0,7 Mm ajouté au
gel juste avant sa solidification. Les fragments amplifiés ont été visualisés à l'aide du système
de documentation Vilbert Lourmart comportant un transilluminateur à UV, une cage équipée
d'une caméra et un écran de visualisation doté d'un lecteur de disques de 3,5 pousses.
Tableau 2: Liste des amorces sélectionnées dans notre étude
Amorce Nom de l'amorce
Séquence (5'---+3') Température d'hybridation (°C)
1
2
3
4
(AC) 8 G ACA-CAC-ACA-CAC-ACA-CG 52
(TG) 8 G TGT-GTG-TGT-GTG-TGT-GG 52
(GA) 8YG GAG-AGA-GAG-AGA-GAG-A YG 56
(AC) 8YC ACA-CAC-ACA-CAC-ACA-CYC 56
17

2.2.5. Analyse statistique des données
Les locus des différents marqueurs ont été marqué par la méthode binaire: 1 quand la
bande est présente et O quand la bande est absente. La matrice de données générée pour les
différentes variétés a été utilisée pour calculer les indices de différenciation génique,
notamment le f~, (Wright, 1951 ).
L'expression estimant le coefficient de différenciation F« est :
a Fs1= 1-
a+b+c
où a, exprime les variations entre populations; b, les variations entre individus à l'intérieur
des populations etc, les variations entre les allèles au sein des individus.
Le ]~1 mesurant le taux de différenciation génique entre les accessions a été testé entre
toutes les variétés et entre ]es zones de collectes par I' Analyse de la Variance Moléculaire ou
AMOVA (Excoffier el al., 1992) en utilisant le logiciel GenAIEx, version 6 (Peakall &
Smouse, 2001).
Le PIC (Polymorphism Information Content ou encore indice de diversité de Nei) a été
utilisé pour évaluer la diversité au niveau des variétés locales. Celui-ci se calcule selon cette
formule suivante :
PIC= I [1- (p/ + aï2)]
où Pi et ai représentent respectivement la présence et l'absence des fréquences dei bandes.
Pour chaque variété, les distances génétiques entre différentes paires d'accessions ont
été calculées afin de construire un dendrogramme à partir de la matrice de distances obtenue.
Les arbres phylogénétiques ou dendrogrammes ont été construits en utilisant respectivement
le logiciel XLST AT pour la phylogénie entre les accessions et Le logiciel Darwin version 5.8
pour les relations phylogéniques entre les 103 individus analysés. La robustesse du
dendrogramme a été testée par 1000 réechantillonages numériques (bootstraps).
Une analyse factorielle discriminante (AFD) a été réalisée avec le logiciel XLSTAT.
Cette méthode permet de classer les échantillons dans le cadre des groupes constitués de
façon à ce que le risque de classement erronés soit le plus petit possible. Les variables
canoniques choisies de façon à rendre maximum la différence entre les groupes, permettent de
préciser la répartition des groupes dans l'espace de départ.
18

3. RESULTATS ET DISCUSSION
3.1. Résultats
3.1.1. Polymorphisme des loci
Quatre amorces ISSR [(AC) 8G, (TG) 8G, (GA) 8YG, (AC) 8YC] ont été appliquées
aux 21 accessions de melon. Un total de 82 loci a été observé. L'indice de diversité de Nei
évalué à travers le PIC (Polymorphism Information Content) varie entre 0,15 [(AC) 8YC] et
0,23 [ (AC) 8G] avec une moyenne de 0, 18 (Tableau 3). La valeur moyenne du PIC observée
indique une faible diversité générée par les amorces pour les deux variétés.
Le poids moléculaire des fragments amplifiés varie de 120 à 2000 paires de bases
(Tableau 4). L'amorce (GA) 8YG s'est révélée comme étant la plus polymorphe avec un
total de 28 loci observés. Quant à l'amorce (AC) 8G. elle a montré un faible nombre de loci
(15 loci). A partir de la matrice générée sur la base du profil des individus analysés, les
indices de diversité génétique des accessions, des variétés et des zones de collecte ont été
évalués. Un profil d'amplification représentatif de la diversité obtenu avec l'amorce (AC)
8YC est présenté à la figure 5.
Tableau 3: Nombre d'amorces, pourcentage des loci polymorphes obtenu par amorce et PIC
par amorce
Amorces Total Loci (¾)Loci PIC ( moyenne ± polymorphes polymorphes écart-type)
(AC) 8 G 15 15 100 0,23 ± 0,17
(TG) 8 G 18 18 100 0.16 ± 0.18
(GA) 8YG 28 28 100 0,16 ± 0.17
(AC) 8YC 21 21 100 0, 15 ± 0, 18
Total 82 82
Moyenne 20,5 20,5 100 0,18 ± 0, 17
19

PM 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 PM
1500 pb
1000 pb
800 pb
600 pb
400 ob 200 pb
1 1 ·- ...
~ ~- .... -· • - - •.... ----- - •• .,_ - ~ .•. -
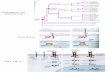
Figure 5: Polymorphisme (présence / absence) révélé par amplification de l'amorce
(AC)8YC chez 16 individus de melons. Les canaux PM indiquent le marqueur de poids
moléculaire (Smart Ladder)
20

Tableau 4: Poids moléculaire (pb) et nombre de loci amplifiés par amorce chez les 21 accessions de melons
Amorces (AC) 8G (TG) 8G (GA) 8YG (AC) YC
1914 2000 2000 960
1425 1500 1500 840
1050 1425 1450 800
1000 1275 1425 739
934 1200 1275 720
800 1000 1000 700
739 934 934 640
677 900 800 630
600 800 739 600
540 739 600 590
480 700 590 580
400 600 580 540
320 580 500 500
Poids 540 460 450 moléculaire
(ph) 480 450 440
450 440 400
400 420 340
320 400 320
380 300
360 200
320
300
240
230
200
180
160
120
Nombre de loci 15 18 28 21
21.

3. 1.2. Structure de la diversité génétique des variétés
Pour évaluer la diversité génétique entre les 7 variétés de melons étudiées, une
Analyse Factorielle Discriminante (AFD) (Figure 6) a été réalisée. Les deux principaux axes
expriment 63,84% de la variabilité totale avec 47,39 % et 16,46 % de la variabilité pour l'axe
l et l'axe 2 respectivement. Les accessions se sont regroupées selon les variétés. Les
accessions appartenant aux variétés "oléagineuse" es flexuosus se regroupent à droite de l'axe 1, les variétés dudaim, momordica et celle consommée en légume, se rangent à gauche de
l'axe 1. Quant à la variété cantalupensis, elle se range au-dessus de l'axe 2. Les résultats de
I' AFD ont permis de distinguer trois groupes : le premier groupe est constitué uniquement de
la variété cantalupensis; le second groupe comporte quatre variétés, inodorus, dudaim,
momordica et celle consommée en légume et le troisième groupe est constitué des variétés
flexuosus et "oléagineuse".
Tableau 5: Analyse de la variance moléculaire (AMOY A) testant la différenciation génétique
de 21 accessions de Cucumis melo selon les variétés et les zones de collecte
Niveau de Source de DL SCE CM F %F r; p
diversité différentiation
Entre variétés 6 312,836 52,139 2,809 12 0,124 0,010
Entre accession 14 620,913 44,351 5,732 26 0,295 0.010 Variété par variété
Entre individu 82 1286,600 15,690 15,690 71 0,287 0.010 par accession
Entre zone 7 445,597 63,657 3,571 16 0,160 0,010
Entre accession 13 488,152 37,550 4,492 20 0,294 0,010 Zone par variété 82 1286,600 15,690 15,690 71 0,287 0,010
Entre individu par accession
L'analyse de la différenciation entre toutes les variétés ainsi que les zones de collectes
a été réalisée à l'aide d'une AMOY A (Tableau 5).
L'analyse de la différenciation entre différents niveaux de structuration de toutes les
variétés montre que la différenciation génétique entre les accessions par variété et entre les
individus par accession (Fs,) est respectivement de 0,295 et 0,287 (Tableau 5). Cette valeur
élevée met en évidence une très grande différenciation génétique entre les accessions par
22

variété ainsi qu'entre individus par accession. Une faible valeur de r~r a été observée entre les variétés CF.ri= 0, 124), correspondant à seulement 12 % de variation entre celles-ci. Ce résultat
montre la forte similarité entre les variétés étudiées. En outre, en considérant les zones de
collectes, une forte différenciation génétique est observée entre les variétés. Cependant, entre
les accessions par variété et entre les individus par accession, la différenciation génétique est
très grande. La variation entre individus par accession est de l'ordre de 71 % aussi bien
lorsqu'on considère les variétés que les zones de collecte.
Tableau 5: Analyse de la variance moléculaire (AMOV A) testant la différenciation génétique
de 21 accessions de Cucumis melo selon les variétés et les zones de collecte
Niveau de Source de DL SCE CM F %F r; p
diversité différentiation
Entre variétés 6 312,836 52,139 2,809 12 0,124 0,010
Entre accession 14 620,913 44,351 5,732 26 0,295 0,010 Variété par variété
Entre individu 82 1286,600 15,690 15,690 71 0,287 0,010 par accession
Entre zone 7 445,597 63,657 3,571 16 0,160 0,010
Entre accession 13 488,152 37,550 4,492 20 0,294 0.010 Zone par variété 82 1286,600 15,690 15,690 71 0,287 0,010
Entre individu par accession
23

Au niveau de la structuration entre les zones de colJectes des différentes accessions,
les résultats indiquent qu'à l'intérieur de chaque zone, une différence significative a été
observée entre les accessions par variétés (f~1 = 0,294 soit 20 % ; P = 0,010) et entre les individus par accession (Fs1 = 0,287 avec 71 % ; P = 0,010). Tableau 5: Analyse de la variance moléculaire (AMOY A) testant la différenciation génétique
de 21 accessions de Cucumis melo selon les variétés et les zones de collecte
Niveau de Source de DL SCE CM F ¾F r; p
diversité différentiation
Entre variétés 6 312,836 52,139 2,809 12 0,124 0,010
Entre accession 14 620,913 44,351 5,732 26 0,295 0,010 Variété par variété
Entre individu 82 1286,600 15,690 15,690 71 0,287 0,010 par accession
Entre zone 7 445,597 63,657 3,571 16 0, 160 0,010
Entre accession 13 488,152 37,550 4,492 20 0,294 0,010 Zone par variété
82 1286,600 15,690 15,690 71 0,287 0,010 Entre individu par accession
24

L
10
8 - ~ 6 1 ~ • 1 0 ~ ••• 4 • 2 ~~ • -.. I •3 - ') I N - QI •4 ;.'; ~
• 5
-4 ~k J ,·~ -6 • I
-14-12-10-S -6 -4 -2 0 2 4 6 S 10 L
Axe 1 (47,39%)
Figure 6: Mise en évidence des groupes d'individus identifiés à partir de I' AFD portant sur
21 accessions de Cucumis melo. Les symboles en couleur représentent les différentes variétés.
I: (2: "oléagineuse", 5:flexuosus), Il :(l:"légume", 3: momordica 6: dudaim 7: inodorus}, Ill:
4: cantalupensis.
25

3.1.3. Relations phylogénétiques
Pour déterminer les relations phylogénétiques entre les accessions utilisées, un
dendrogramme basé sur les distances génétiques a été construit. Le dendrogramme réalisé à
partir de la méthode de Ward (Ward, 1963) a permis de révéler deux (2) principaux groupes
d'accessions (Figure 7). Le premier groupe (groupe A) est constitué des accessions des
variétés "oléagineuse", "légume" et une variété Turque (momordica). Le second groupe
(groupe B) est composé des quatre (4) autres accessions originaires de Turquie. d'une
accession de la variété consommée en légume et des accessions de la variété oléagineuse. Le
groupe A est subdivisé en deux sous-groupes : le sous-groupe Ai et le sous-groupe A2. La
configuration du dendrogramme montre que les regroupements des accessions sont faits
indépendamment des zones de collecte.
Les données moléculaires collectées ont permis d'établir les relations phylogénétiques
entre 103 individus de l'espèce Cucumis melo. Le dendrogramme a été établit en utilisant la
méthode UPGMA. Les individus se sont regroupés en deux (2) grands groupes. Le groupe I
inclut, en majorité, les individus des variétés; "légume" et ''oléagineuse" et de quelques
individus des accessions originaires de Turquie. Quand au groupe IL il est constitué,
majoritairement, des individus des melons d'origine turque bien qu'on y trouve certains
individus des variétés " légume" et "oléagineuse". Le groupe I est subdivisé en deux sous
groupes : le sous-groupe Ia et le sous-groupe lb. La configuration du dendrograrnme (Figure
8) montre que les regroupements des individus n'ont pas été faits selon les variétés. De plus,
les faibles valeurs de bootstrap montrent que les nœuds unissant les génotypes ne sont pas
robustes. Tous les deux sous-groupes dégagés à partir du dendrogramme sont constitués des
individus de toutes les variétés analysées dans notre étude. Par ailleurs, les regroupements ne
sont pas suivants les origines des individus.
26

NI454-LE
NI453-LE
NI447-LS '-------1• NI445-LS
NI435-LS NI460-0C Nl455-0N Nl456-0N NI481-MT Nl475-0E NI452-LS NI479-IT NI482-DT NI466-0C NI464-0C Nl463-0C Nl480-CT Nl467-0C NI484-FT NI469-0E
~-----tNI461-0C
A
B
-0.08 6 -0.04
(' oeffklent de rlls~imilarité
_.,_o_
Figure 7: Dendrogramme obtenu par la méthode de Ward basé sur la distance de Jaccard pour
la différenciation génétique des marqueurs ISSR entre 21 accessions de Cucumis melo. Les
numéros d'accessions sont respectivement suivi du type de variété (0: oléagineuse, L:
légume, M: momordica, I: inodorus, F:flexuosus, C: cantalupensis, D: dudaim et de la région
d'origine (C: Centre, E: Est, S: Sud, N: Nord, T: Turquie)
27

. 118175171
r-180 1184
187 1
l1i a
1 I
18-5 181
119
-
193 1 189 177
1
141 ~J ?P#=f b
188 1U
191 116
186 173
1 I II
o~---~0.1
Figure 8: Relations phylogénétiques entre les 103 individus de melons révélés par la méthode
UPGMA basée sur les coefficients de dissimilarités.
• var. momordica;
• var. dudaim
• var. inodorus; O var. flexuosus; • var. cantalupensis;
• Cucumis melo subsp. agrestis (légume);
o Cucumis melo subsp. agrestis (oléagineuse)
28

3.2. Discussion
La technologie ISSR est un outil moléculaire d'usage courant pour évaluer la diversité
génétique des espèces végétales (Zietkiewicz et al., 1994; Fang & Roose, 1997). Cette
technique basée sur la PCR, est efficace et moins coûteuse. Les marqueurs ISSR ont été
utilisés pour révéler un haut degré de polymorphisme au sein de plusieurs plantes telles que la
mûre (Kar et al., 2008) et les cultivars du genre Citrus (Fang & Roose, 1997). Dans cette
étude. des marqueurs ISSR ont été utilisés pour évaluer la différenciation au sein de deux
variétés de l'espèce C. melo subsp. agrestis ainsi que leurs relations phylogénétiques avec
d'autres variétés de melons.
Les analyses effectuées portant sur le PIC ont montré que les amorces utilisées ne
révèlent pas un haut niveau de polymorphisme entre les deux variétés locales relativement
aux valeurs rapportées par d'autres auteurs (Ritschel et al., 2004). En effet, les résultats
obtenus par ces auteurs ont permis de révéler un haut niveau de polymorphisme au sein de
l'espèce Cucumis melo. Les valeurs de PIC obtenues de cette espèce varient entre 0,28 et 0,65
contrairement à celles des deux variétés locales qui varient de 0,15 à 0,23. Ce résultat
contraire à la très forte diversité morphologique observée au sein de cette espèce (Angui
2008); pourrait suggérer que les régions du génome explorées par les amorces utilisées dans
cette étude ne sont pas celles qui gouvernent la morphologie et la phénologie des plantes et
des fruits.
Une différenciation génétique des variétés utilisées a été révélée par une AMOV A.
Les résultats montrent une faible diversité entre les variétés analysées, F« = 0,124. Ce résultat
suggère une forte similarité entre les variétés. Cette observation a été également notée chez la
cucurbite Citrullus lanatus var. lanatus, qui bien que présentant une forte diversité
morphologique, a une très faible diversité génétique (Levi et al., 2001 ; Zarnir et al., 1984).
Cependant, une forte différenciation a été observée entre les accessions F« = 0.295. Ce
résultat est similaire à celui observé au sein des accessions de melons d'Inde et d'Afrique
Centrale qui possèdent une certaine variabilité intra-accession (Monforte et al., 2003).
L'influence de la zone d'origine a été testée par une AMOV A. Les résultats montrent
que l'origine des accessions a une influence sur la structuration de la variabilité génétique.
Cette observation est similaire à celle observée au sein des melons de l'Est et du Sud de
l'Asie. En effet, il existe une différenciation génétique et géographique selon la taille des
graines chez les melons asiatiques, avec des graines de grande taille en Asie centrale et du
Sud-ouest et des petites graines en Asie de l'Est (Akashi et al., 2002; Yashiro et al., 2005).
29

Les relations phylogénétiques établies révèlent que les accessions étudiées ne se
regroupent pas selon les variétés ni les origines géographiques. Ces résultats sont similaires à
ceux de Lôpez-Sesé et al. (2003) obtenus à partir de l'étude sur l'analyse moléculaire des
melons espagnols. Des différences n'ont pas été révélées à partir des régions entre les
accessions locales d'une part et entre les accessions locales et turques d'autre part. Les
analyses ont révélés une affinité entre les accessions locales et celles de Turquie. Dans la
littérature, plusieurs auteurs ont observé que les accessions africaines, européennes et
asiatiques de melons présentent une forte affinité phylétique (Mliki et al., 2001; Monforte et
al., 2003; Nakata et al., 2005).
Aussi, les analyses des relations phylogénétiques ont-ils permis de distinguer deux
grands groupes. Les deux groupes établis sont composés des accessions de toutes les variétés
étudiées. La séparation entre les variétés n'est pas nette. Les faibles valeurs de bootstrap
montrent que les nœuds unissant les génotypes ne sont pas robustes. Ce résultat pourrait
suggérer que la séparation entre les différentes variétés est récente. Elle pourrait être attribuée
au fait que la différence observée est la résultante de la sélection paysanne au fil des ans et du
processus de domestication.
Les résultats obtenus à partir de l' AFD permettent de différencier les deux variétés
locales: la variété "légume" et la variété "oléagineuse". Dans la littérature, les différentes
variétés de melons se rangent en deux (2) sous-espèces.la sous-espèce melo et la sous-espece
agrestis (Silberstein et al., 1999; Stepansky et al., 1999; Monforte et al., 2003). Dans la sous
espèce agrestis on trouve les variétés conomon et momordica et dans la sous-espèce melo les
variétés cantalupensis, inodorus.flexuosus, dudaim et chito (Pitrat, 2008). Tenant compte du
positionnement des individus des variétés locales par rapport à ces variétés, nous avons pu
élucider leur classification. En effet, il est ressorti de notre analyse que la variété
"oléagineuse" se regroupe avec la variété flexuosus qui est classé dans la sous-espèce melo,
par contre, la variété "légume" se range avec les variétés dudaim et momordica. Sur la base de
ces résultats, nous sommes tentés de suggérer que la variété "oléagineuse" appartient à la
sous-espèce melo. Par conséquent, nos résultats accréditeraient l'hypothèse d' Achigan-Dako
et Baudoin (2007) c'est-à-dire que ta variété de melon cultivée en Côte d'Ivoire devra être
classée dans la sous-espèce melo. De ce fait, nous préconisons d'autres analyses moléculaires
afin de confirmer nos résultats.
30

CONCLUSION ET PERSPECTIVES
La connaissance de la diversité et les rapports génétiques entre les races locales est
importante dans les stratégies d'amélioration des plantes. Les marqueurs moléculaires utilisés
à cet effet révèlent des différences au niveau de l'ADN et sont des outils directs. fiables et
effectifs pour la conservation et la gestion du germoplasme. L'étude de la différenciation par
l'utilisation des marqueurs moléculaires entre les variétés "légume" et "oléagineuse" de
l'espèce C. melo subsp. agrestis a été menée. En outre, les relations phylogénétiques de ces
deux variétés avec d'autres types de melons ont été analysées. La technique ISSR a permis de
réaliser cette étude. Les analyses effectuées ne permettent pas de différencier les variétés "légume" et
"oléagineuse". Une très grande différenciation génétique a été cependant mise en évidence
entre les accessions par variété ainsi qu'entre individus par accession. En outre, une faible
différenciation génétique a été observée entre les variétés étudiées. Aussi, faut-il signaler une
grande différenciation parmi les accessions au niveau des zones de collectes.
Cette étude a pu suggérer une nouvelle classification des variétés de melons cultivées en
Côte d'Ivoire. Toutefois, vu le faible nombre d'individus analysés et d'amorces utilisés, il
conviendrait d'envisager de renforcer cette étude pour élucider définitivement cette
classification.
Par conséquent nous proposons:
- D'augmenter le nombre d'accessions et d'individus avec une plus grande
représentativité des zones de collecte
- D'augmenter le nombre d'amorce pour être sûr de parcourir la majeure partie du
génome de ces variétés
- Enfin, utiliser des marqueurs Co-dominants tels que les SSR qui, en plus d'être très
polymorphes, sont plus informatifs.
31

REFERENCES BIBLIOGRAPIDQUES
Achigan-Dako GE & Baudoin JP (2007). Cucumis melo L. subsp. agrestis (Naudin)
Pangolo (Cucurbitaceaey : nécessité de clarification sur le statut de la sous-espèce.
Biotechnologie Agronomie Societé et Environnement 11 (4): 283-286.
Akashi Y, Fukuda N, Wako T & Kato K (2002). Genetie variation and phylogenetic m
East and South Asian melon, Cucumis melo L. based on the analysis of five isozymes.
Euphytica 125: 385-396.
Angui CMV (2008). Caractérisation morphologique de deux variétés d'une cucurbite
comestible Cucumis melo ssp. agrestis (L.) Naudin. Mémoire de Maîtrise. Abidjan
(Côte d'Ivoire): Abobo-Adjarné; 30 pages.
Berthou F (1983). CbJoroplast and mitochondrial DNA variation as indicator of phylogenetic
relationships in the genus Coffea L. Theoretical and Applied Gene tics 65: 77-84.
Blair MW, Panaud O & Mc Couch SR (1999). Inter-Simple Sequence Repeat (ISSR)
amplification for analysis of microsatellite motif frequency and fingerprinting in rice
( Oryza sati va L.). Theoretica/ and Applied Gene tics 98: 780- 792.
Bornet B, Goraguer F, Joly G & Branchard M (2002). Genetie diversity in European and
Argentinian cultivated potatoes (Solanum tuberosum subsp. tuberosumy detected by inter-simple sequence repeats (ISSRs). Genome 45 (3): 481-484.
Cakmak I (2002). Plant nutrition research: Priorities to meet human needs for food m
sustainable ways. Plant and Soif 247: 3-24.
Charters YM, Robertson A, Wilkinson MJ & Ramsay G (1996). PCR analysis of oilseed
rape cultivars (Brassica napus L. ssp. ol!fera) using 5'-anchored simple sequence
repeat (SSR) primers. Theoretical and Applied Genetics 92: 442-447.
Chweya JA & Eyzaguirre PB (1999). The biodiversity of traditional leafy vegetables. Rome
(Italia): International Plant Genetie Resources Intitule (IPGRI); 182 pages.
Dellaporta SL, Wood J & Hicks JB (1983). A plant DNA minipreparation: version II. Plant
Molecular Biology 1: 19-21.
Djè Y, A ter M, Lefèbvre C & Vekemans V (1998). Patterns of morphological and allozyme
variation in sorghum landraces of Northwestern Morocco. Genetie Resources and ropEvolution 45: 541-548.
32

Djè Y, Kouonon CL, Zoro Bi IA, Gnamien YG & Baudoin JP (2006a). Etude des
caractéristiques botaniques, agronomiques et de la biologie florale du melon africain
(Cucumis melo L. var. agrestis Naudin, Cucurbitaceaeï. Biotechnology Agronomy
Society and Environnement l O (2): 109-119.
Djè Y, Tabi GC, Zoro Bi lA, Malice M, Baudoin JP & Bertin P (2006b). Optimization of
ISSR marker for A.frican edible-seeded Cucurbitaceae species1 genetic diversity
analysis. African Journal of Biotechnology 5 (2): 83-87.
Excoffier L, Smouse PE & Quattro JM (1992). Analysis of molecular variance inferred
from metric distances among DNA haplotypes: Application to human mitochondrial
DNA restriction data. Genettes 131: 479-491.
Fang QD & Roose LM (1997). Identification of closely related citrus cultivars with inter
simple sequence repeat markers. Theoretical and Applied Genetics 95: 408-417.
FAO (2009). Number of undemourished persons. Food Security Statistics. Available via
D!ALOG. www.fao.org/economic/ess/food-security-statistics/en/:
Gruhn P, Goletti F & Yudelman M (2000). Integrated nutrient, soif fertility, and
sustainable agriculture: current issues and future challenges. food, Agriculture and
the Environment Discussion Paper 32. Washington, DC: TnternationaJ Food Policy
Research lnstitute 32 pages.
Gupta M, Chyi Y-S, Romero-serveson J & Owen J (1994). Amplification ofDNA markers
frorn evolutionarily diverse genomes using single primers of simple sequence repeats.
Theoretical and Applied Genetics 89: 998-1005.
Kantety RV, Zeng XP, Bennetzen JL & Zehr BE (1995). Assessment of genetic diversity
in dent and popcorn (Zea mays L.) inbred lines using inter-simple sequence repeat
(ISSR) amplification. Molecular Breeding 1: 365-373.
Kar PK, Srivastava PP, Awasthi AK & Urs SR (2008). Genetie variability and association
of ISSR markers with some biochemicaJ traits in mulberry (Morus spp.) genetic
resources available in Jndia. Tree Genettes and Genomes 4: 75-83.
Katzir N, Danin-Poleg Y, Tzori G, Karchi Z, Lavi U & Cregan PB (1996). Length
polymorpbism and homologies of microsatellites in several Cucurbitaceae species.
Theoretical and Applied Genetics 93: 1282-1290.
Koffi KK, Anzara GK, Malice M, Djè Y, Bertin P, Baudoin JP & Zoro Bi 1A (2009).
Morphological and allozyme variation in a collection of Lagenaria siceraria (Molina)
Standl. from Côte d'Ivoire. Biotechnology Agronomy Society and Environnement 13
(2): 257-270.
33

Koffi KK, Gbotto AA, Malice M, Djè Y, Bertin P, Baudoin JP & Zoro Bi 1A (2008).
Morphological and allozyme variation in a collection of Cucumeropsis mannii Naudin
(Cucurbitaceae) from Côte d'Ivoire. Biochemical Systematics and Ecology 36: 777-
789.
Levi A. Thomas CE, Wehner TC & Zhang X (2001b). Low genetic diversity indicates the
need to broaden the genetic base of cultivated watermelon. Horticultural Science 36
(6): 1096-1101.
Lôpez-Sesé IA, Staub JE & Gômez-Guillamôn LM (2003). Genetie analysis of Spanish
melon ( Cucumis melo L.) germplasm using a standardized molecular-marker array
and geographically diverse reference accessions. Theoretical and Applied Genetics
108: 41-52.
Lôpez-Sesê JA, Staub JE, Katzir N & Gômez-Ouillamôn LM (2002). Estimation of
between and within accession variation in selected Spanish melon germplasm using
RAPD and SSR markers to assess strategies for large collection evaluation. Euphytica
127: 41-51.
Loukou AL, Gnakri D, Djè Y, Kippré A V, Malice M, Baudoin JP & Zoro Bi 1A (2007).
Macronutrient composition of three cucurbit species cultivated for seed consumption
in Côte d'Ivoire. African Journal of Biotechnology 6 (5): 529-533.
Maggs-Këtling GL, Madsen S & Christiansen JL (2000). A phenetic analysis of
morphologicaJ variation in Citrullus lanatus in Namibia. Genetie Resources and Crop
Evolution 47: 385-393.
Malice M & Baudoin JP (2009). Genetie diversity and germplasm conservation of three
minor Andean tuber crop species. Biotechnology Agronomy Society and
Environnement 13 (3): 441-448.
Mariod M & Matthaus B (2008). Fatty acids, tocopherols, sterols, phenolic profiles and
oxidative stability of Cucumis melo var. agrestis oil. Journal of Food Lipids 15: 56 -
67.
Mliki A, Staub JE, Zhangyong S & Ghorbel A (2001). Genetie diversity in melon
(Cucumis melo L.): An evaluation of African germplasm. Genetie Resources and Crop
Evolution 48: 587-597.
Monforte AJ, Garcias-Mas J & Arûs P (2003). Genetie variability in melon based on
microsatellite variation. Plant Breeding 122: 153-157.
34

Morimoto Y, Maundu P, Fujimaki H & Morishima H (2005). Diversity oflandraces of the
white-flowered gourd (Lagenaria siceraria) and its wild relatives in Kenya: fruit and
seed morphology. Genetie Resources and Crop Evolution 52: 737-747.
Munger HM & Robinson RW (1991 ). Nomenclature of Cucumis melo L. Cucurbit Genetics
ooperation Report 14: 43-44.
Nakata E, Staub JE, Lôpez-Sesé 1A & katzir N (2005). Genetie diversity of Japanese
melon cultivars (Cucumis melo L.) as assessed by randorn arnplified polymorphie
DNA and simple sequence repeat markers. Genetie Resources and Crop Evolution 52:
405-419.
Nakazawa M, Wakabayashi M, Ono M & Murata J (1997). Molecular phylogenetic
analysis of Chrysosplenium (Saxifragaceae) in Japan. Journal of Plant Research 110:
265-274.
Naudin CV (1859). Essais d'une monographie des espèces et des variétés du genre Cucumis.
Annales des Sciences Naturelles, Botanique 4 (11): 5-81.
Pasteur N, Pasteur G, Bonhomme F, Catalan J & Britton-Davidian J (1987) Manuel
technique de génétique par élèctrophorèse des protéines. Techniques et
documentation, Lavoisier edn, Paris (France), p 75.
Peakall R & Smouse PE (2001). GENALEX. Genetie analysis in Excel. Population genetic
software for teaching and research; version 6.1. Canberra (Australia): Australian
National University. www.anu.edu.au/BoZo/GenALEx:
Pitrat M (2008) Melon. In: Prohens J & Nuez F (Eds) Vegetables J ( Asteraceae,
Brassicaceae, Chenopodicaceae and Cucurbitaceae). New York ( USA): Springer, pp
283-314.
Pitrat M, Chauvet M & Foury C (1999). Diversity, history, production of cultivated
cucurbits. Acta Horticulturae 492: 21-28.
Rao RV & Hodgkin T (2002). Genetie diversity and conservation and utilization of plant
genetic resources. Plant Cell, Tissue and Organ Culture 68: 1-19.
Ritscbel PS. de Lima Lins TS, Tristan RL, Cortopassi Buso GS, Buso JA, Ferreira ME
(2004). Development of microsatellite markers from an enriched genomic library for genetic
analysis of melon (Cucumis melo L.). BioMed Central Plant Biol 4:9
Roux L (1987). Utilisation des isoenzymes comme marqueurs génétiques. Le sélectionneur
Français 39: 31-39.
35

Santoni S, Faivre-Rampant P, Prado E & Prat D (2000). Marqueurs moléculaires pour
l'analyse des ressources génétiques et l'amélioration des plantes. Cahiers Agricultures
9 (4): 311-327.
Silberstein L, Kovalski 1, Huang R, Anagnostou K, Jahn KMM & Perl-Treves R (1999).
Molecular variation in melon (Cucumis melo L.) as revealed by RFLP and RAPD.
'cientia Horticulturae 79: 101-111.
Staub JE, Danin-Poleg Y, Fazio G, Horejsi T, Reis N & Katzir N (2000). Comparative
analysis of cultivated melon groups (Cucumis melo L.) using random amplified
polymorphie DNA and simple sequence repeat markers. Euphytica 115: 225-241.
Staub JE, Lôpez-Sesê 1A & Fanourakis N (2004). Diversity among melon landraces
(Cucumis melo L.) from Greece and their genetic relationships with other melon
germplasm of diverse origins. Euphytica 136: 151-166.
Stepansky A, Kovalski I & Perl-Treves R (1999). Intraspeci:fic classifcation of melons
(Cucumis melo L.) in view of their phenotypic and molecular variation. Plant
lystematics and Evolution 217: 313-332.
Tanaka K, Nishitani A, Akashi Y, Sakata Y, Nishida H, Yoshino R & Kato K (2007).
Molecular characterization of South and East Asian melon, Cucumis melo L., and the
origin of group Conornon var. makuwa and var. conomon revealed by RAPD analysis.
Euphytica 153: 233-247.
Terauchi R, Chikaleke VA, Thottappiuy G & Hahn SK (1992). Origin and phylogeny of
Guinea yams as revealed by RFLP analysis of chJoroplast DNA and nuclear ribosomal
DNA .. Theoretical and Applied Genetics 83: 743 - 751.
Ward HJ (1963). Hierarchical grouping to optimize an objective function. Journal of the
American Statistical Association 58 (301 ): 236-244.
William JT & Haq N (2002). Global research on underutilized crops. An assessment of
current activities and proposais for enhanced cooperation. Southampton, UK: ICUC;
45 pages. Wright S (1951). The genetical structure of populations. Annois of Eugenetics 15: 6531-
6535.
Yashiro K, lwata H, Akashi Y, Tomita K, Kuzuya M, Tsumura Y & Kato K (2005).
Genetie relationship among East and South Asian melon (Cucumis melo) revealed by
AFLP analysis. Breeding Science 55: 197-206.
Yi SS, Akashi Y, Tanaka K, Cho TT, Khaing TM, Yosbino H, Nishida R, Yamamoto T,
Win K & Kato K (2009). Molecular analysis of genetic diversity in melon landraces
36

(Cucumis melo L.) from Myanmar and their relationship with melon germplasm from
East and South Asia. Genetie Resources and Crop Evolution 56: 1149-1161.
Zamir D, Navot N & Rudich J (1984). Enzyme polymorphism in Citrullus lanatus and
colocynthis in Israel and Sinaï. Plant Systematics and Evolution 146: 137-163.
Zietkiewicz E, Rafalski A & Labuda D (1994). Genome fingerprinted by Simple Sequence
Repeat (SSR) Anchored Polymerase Chain Reaction Amplification. Genomics 20:
176-183.
Zoro Bi IA, Koffi KK & Djè Y (2003). Caractérisation botanique et agronomique de trois
espèces de cucurbites consommées en sauce en Afrique de l'Ouest: Citrullus
sp.,cucumeropsis mannii Naudin et Lagenaria siceraria (Molina) Standl.
Biotechnologie, Agronomie Société et Environnement 1 (3-4): 189-199.
37
Related Documents