N O O H N O H O <Chapter 7> 3. Write the Lewis structures for the following molecules and polyatomic ions. In each case, the first atom is the central atom. (a) IO 2 - (b) SiF 4 원자가 전자수 : I = 7 원자가 전자수 : Si = 4 O = 6 F = 7 (c) BrI3 (d) CN - 원자가 전자수 : Br = 7 원자가 전자수 : C = 4 I = 7 N = 5 11. Dinitrogen pentoxide, N 2 O 5 , when bubbled into water can form nitric acid. Its skeleton structure has no N-N or O-O bonds. Write its Lewis structure. 29. Below are two different Lewis structures for nitrous acid (HNO 2 ). Which is the better Lewis structure based only on formal charge? structure I structure II

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript
N OOHN OH
O
<Chapter 7>
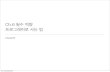
3. Write the Lewis structures for the following molecules and polyatomic ions. In
each case, the first atom is the central atom.
(a) IO2- (b) SiF4
원자가 전자수 : I = 7 원자가 전자수 : Si = 4
O = 6 F = 7
(c) BrI3 (d) CN-
원자가 전자수 : Br = 7 원자가 전자수 : C = 4
I = 7 N = 5
11. Dinitrogen pentoxide, N2O5, when bubbled into water can form nitric acid. Its
skeleton structure has no N-N or O-O bonds. Write its Lewis structure.
29. Below are two different Lewis structures for nitrous acid (HNO2). Which is the
better Lewis structure based only on formal charge?
structure I structure II
* 형식전하(formal charge) 구하는 법
Cf = X - (Y +Z/2)
X = 결합되지 않은 원자의 원자가 전자수 = 주기율표에서 족번호의 마지막 자리수
Y = Lewis 구조에서 원자에 의해 소유된 비공유 전자수
Z = Lewis 구조에서 원자가 공유한 결합 전자수
=> structure I
① N : X = 5, Y = 2, Z = 6. Cf = 5 - (2+6/2) = 0
② O (왼쪽) : X = 6, Y = 4, Z = 4. Cf = 6 - (4+4/2) = 0
③ O (오른쪽) : X = 6, Y = 4, Z = 4. Cf = 6 - (4+4/2) = 0
④ H : X = 1, Y = 0, Z = 2. Cf = 1 - (0+2/2) = 0
=> structure II
① N : X = 5, Y = 0, Z = 8. Cf = 5 - (0+8/2) = 1
② O (아래) : X = 6, Y = 6, Z = 2. Cf = 6 - (6+2/2) = -1
③ O (위) : X = 6, Y = 4, Z = 4. Cf = 6 - (4+4/2) = 0
④ H : X = 1, Y = 0, Z = 2. Cf = 1 - (0+2/2) = 0
=> 형식전하 측면에서 structure I 이 더 적합하다.
31. Predict the geometry of the following species.
(a) SCO (b) IBr2-
AX2 의 형태 AX2E3 의 형태
(c) NO3- (d) RnF4
AX3 의 형태 AX4E2 의 형태
C C
Cl
HH
Cl
1
C C
H
ClH
Cl
2
C C
Cl
ClH
H
3
C C
Cl
HH
Cl
1
C C
H
ClH
Cl
2
C C
Cl
ClH
H
3
35. (a) octahedral
(b) tetrahedral
(c) see-saw
(d) tetrahedral
47. There are the compounds with the formula C2H2Cl2
Which of these molecules are polar?
=> 1 과 3 의 구조가 polar 하다.
49. Give the hybridization of the central atom in each species in Question 31.
(a) SCO
=> C 를 중심으로 2개의 결합 : sp 혼성
(b) IBr2-
=> I 를 중심으로 2개의 결합과 3개의 비공유 전자쌍 : sp3d 혼성
(c) NO3-
=> N 를 중심으로 3개의 결합 : sp2 혼성
(d) RnF4
=> Rn 을 중심으로 4개의 결합과 2개의 비공유 전자쌍 : sp3d2 혼성
69. Consider vitamin C. Its skeleton structure is
CO C
H
H
H
H
O
C
H C
O
C
O
C O
O
H
H
HA B
C
①
②③
CO C
H
H
H
H
O
C
H C
O
C
O
C O
O
H
H
H
(a) How many sigma and pi bonds are there in vitamin C ?
=> 단일결합에는 1개의 sigma bond 존재 하고 이중결합에는 1개의 sigma bond 와
1개의 pi bond 존재하므로
위의 Vitamin C 는 20개의 sigma bonds 와 2개의 pi bonds 가 존재한다.
(b) How many unshared electron pairs are there?
(위의 Lewis 구조로부터) 비공유 전자쌍은 12쌍이 있다.
(c) What are the approximate values of the angles marked (in blue) ①,② and ③?
① 109.5°
② 109.5°
③ 120°
(d) What is the hybridization of each atom marked (in red) A,B and C?
A : O 를 중심으로 2개의 결합과 2개의 비공유 전자쌍 : sp3 혼성
B : O 를 중심으로 1개의 결합과 2개의 비공유 전자쌍 : sp2 혼성
C : C 를 중심으로 3개의 결합 : sp2 혼성
75. Give the formula of an ion or molecules in which an atom of
(a) N forms three bonds using sp3 hybrid orbitals.
=> N 을 중심으로 4개의 전자쌍이 존재 : NH3, NH4+
(b) N forms two pi bonds and one sigma bond.
=> N의 삼중결합 : N2, CN-
(c) O forms one sigma and one pi bond.
=> O 의 이중결합 : NO
(d) C forms four bonds in three of which it uses sp2 hybrid orbitals.
=> C 를 중심으로 3개의 전자쌍이 존재 : H2CO3
(e) Xe forms two bonds using sp3d2 hybrid orbitals.
=> Xe 를 중심으로 5개의 전자쌍이 존재 : XeF2-2
81. It is possible to write a simple Lewis structure for the SO4- ion, involving only
single bonds, which follows the octect rule. However, Linus Pauling and others
have suggested an alternative structure, involving double bonds, in which the
sulfur atom is surrounded by six electron pairs.
(a) Draw the two Lewis structures.
(b) What geometries are predicted for the two structures?
=> 둘 모두 AX4 의 형태 : Tetrahedral
(c) What is the hybridization of sulfur in each case?
=> 둘 모두 S 를 중심으로 4개의 결합 : sp3
(d) What are the formal charges of the atoms in the two structures?
=> * 첫 번째 구조
① S : X = 6, Y = 0, Z = 8. Cf = 6 - (0+8/2) = +2
② O (네 개 모두 동일) : X = 6, Y = 6, Z = 2. Cf = 6 - (6+2/2) = -1
* 두 번째 구조
① S : X = 6, Y = 0, Z = 12. Cf = 6 - (0+12/2) = 0
② O (왼쪽) : X = 6, Y = 6, Z = 2. Cf = 6 - (6+2/2) = -1
③ O (위) : X = 6, Y = 4, Z = 4. Cf = 6 - (4+4/2) = 0
④ O (오른쪽) : X = 6, Y = 6, Z = 2. Cf = 6 - (6+2/2) = -1
⑤ O (아래) : X = 6, Y = 4, Z = 4. Cf = 6 - (4+4/2) = 0
Chapter 8. Thermochemistry (열역학)
열의흐름은 상태함수가 아니므로 어떤 경로를 따라 진행되는가에 의해 결정
Endothermic (q>0)
Exothermic (q<0)
열 흐름의 크기는 j 혹은 kj
q C t m c t= ×∆ = × ×∆
C = heat capacity (열용량=계의 온도를 10C상승시키는데 필요한 열량, J/K )
c = specific heat (비열=순수물질 1g을 10C상승시키는데 필요한 열량, J/g. 0C)
re cal re calq q q C t= − = − ×∆
일정한 압력하에서는 반응계의 열을 생성물과 반응물 사이의 엔탈피차이로 나타낼 수 있다.
tanre product reac tq H H H= ∆ = − 엔탈피는 열함량이라 불리우는 일종의 화학에너지
발열반응 tan0 product reac tq H H H= ∆ < < 흡열반응 tan0 product reac tq H H H= ∆ > >
<열화학법칙>
1. H∆ 의 크기는 반응물이나 생성물의 양에 비례한다.
2. 한 반응의 H∆ 는 역반응의 H∆ 와 부호는 반대이고 그 크기는 같다.
3. 반응에서의 H∆ 값은 반응이 한 단계로 진행되거나, 여러 단계를 거쳐 일어나거나 상관
없이 같다. : Hess’s law
7. (a) what is q for the calorimeter?
열랑계 내에서 발생한 열이 얼마냐는 질문이다. 열량계의 열용량과 온도차를 곱한다.
4
4
4
(2.115 10 / ) (27.71 23.49 ) = (2.115 10 / ) 4.22 = 89253J 8.93 10
q C t J C C CJ C C
J
= ×∆ = × ° × ° − °
× ° × °
≈ ×유효숫자, 4.22 에 맞춰 3자
(b) what is q when 4.50g of fructose is burned?
4.50g의 과당이 연소될 때 발생하는 열을 구하는 문제. 과당을 반응으로 보면 열이
발생되었기에 q<0 이므로 48.93 10 J− × 이다.
(c) what is q for the combustion of one mole fructose?
1mol의 과당은 180.2g 이므로, 44.50 : ( 8.93 10 ) 180.2 :g J g x− × = 로 풀어내면,
33.58 10 KJ− × 이다. 유효숫자는 4.50에 맞춰 3자리이다.
15. (a) write the thermochemical equation for the reaction between one mole of nitrogen oxide and
Oxygen.
NO + 1/2 O2 -> NO2 △H=-57.0 kJ
(b) Is the reaction exothermic or endothermic?
57.0Kj of heat is evolved: 열이 발생하였다: 발열반응: q<0: exothermic
(c) Draw an energy diagram showing the path of this reaction.
(d) What is H∆ when 5.00g of nitrogen oxide react?
NO 5g은 5.0030.01
mol 이므로 5.00 ( 57.0 ) 9.496.. 9.5030.01
KJ KJ× − = − ≈ −
(e) How many grams of nitrogen oxide must react with an excess of oxygen to liberate 10KJ of heat?
(30.01 : 57.0 :10.0 )g KJ X KJ= X= 5.26g
19. (a) write a balanced thermochemical equation for the reaction.
32 3
3Sr(s)+C(s)+ O ( ) SrCO ( ) 1.220 102
g s H kJ→ ∆ = − ×
(b) 반응된 산소의 몰수를 구하면, 엔탈피를 구할 수 있다. 압력과 온도, 그리고 부피가
나와있으므로 이상기체 방정식인 PV=NRT를 사용한다. 또한 에너지가 발하였으므로
엔탈피는 마이너스 값을 갖는다.
PV 10.00L 1atmN= 0.409RT (25 273 ) (0.0821L atm/mol )
molK K
×= =
+ × ⋅ ⋅
1.5 : 1220 0.409 :mol kj mol x− =
X= -332kj
29. 1mol의 아세틸렌( 2 2C H )가 분해할때의 반응열을 계산하라.
2 2C H 가 분해하게 되면 C,H 만 남게된다. 이러한 반응식을 얻어내기 위해서는 부산물인
이산화탄소와 물을 제거하는 반응식을 구하자.
Reactant
Product
2 2 2 2 2
2 2
2 2 2
5C H + O 2CO +H O H=-1299.5KJ2
2CO 2C+2O H=+787KJ1H O H + O H=+285.8KJ2
→ ∆
→ ∆
→ ∆
이것을 전부 더하면, 2 2 2C H ( ) 2C(s)+H ( ) H=-226.7 kJg g→ ∆ , -226.7KJ 이 얻어지
게 된다.
37. 표준엔탈피변화, OH∆ 는 생성물들이 갖는 표준생성엔탈피의 합에서 반응물들이 갖는
표준생성엔탈피의 합을 빼준것과 같다. 표 8-3에서 생성엔탈피를 찾고, 계수를 고려하여
차를 구한다.
(a) 58.9 kj
(b) 108.5kj
(c) -179.9kj
43. (a) 암모니아와 반응하여 질소, 염소, 플루오린화수소 기체를 발생한다 하였으므로
03 3 2 22ClF ( ) 2NH ( ) N ( ) +Cl ( )+6HF( ) 1196g g g g g H kJ+ → ∆ = −
(b) 3
03
6( 271.1) 2(ClF ) 2( 46.1) 1196
( ) 169
Of
f
H
H ClF g kJ
− − ∆ − − = −
∆ = −
의. ClF3는
53. (a) 프로페인 연소시 이산화탄소와 물이 생성되므로,
3 8 2 2 2C H ( ) 5O ( ) 3CO ( ) 4H O(l)g g g+ → +
(b) gH E n RT∆ = ∆ + ∆ , gn∆ 는 (생성물 기체의 몰수-반응물기체의 몰수) 이다.
먼저 엔탈피의 변화를 구하면, 3( 393.5) 4( 285.8) ( 103.8) 2219.9kj− + − − − = −
( 2219.9 ) 3(0.00831)(25 273) 2212.5kj kj kj− + + = −
57. 60분을 걸었을 때 250Kcal가 소모되므로, 120Kcal를 소모시키기 위해서는,
60min : 250 min :120Kcal x Kcal= , 28.8min 을 걸어야 한다.
69. (a) T
(b) T.
(c) T. 결합엔탈피의 정의 : 1mol의 결합이 기체상태에서 끊어지는데 필요한 H∆
(d) F
(e) F
76. (a) ( 1675.5) ( 824.2) 851.5kj− − − = −
(b) q C t m c t= ×∆ = × ×∆ 를 이용. 비열이 문제에 주어졌기에 각 질량을 구하자.
2 3Al O :101.96 2Fe:111.7gg 이므로,
851.5KJ = [(101.96g * 0.77 j/gc) + (111.7g * 0.45j/gc)] t∆ 가 되어 t∆ =6612C이다.
상온에서 반응이 시작하였으므로 25C를 더하면 6637C가 된다.
(c) 철의 녹는점은 1535c이므로 당연히 녹는다.
Chapter 9 Liquids and Solids
9. Mt. Mckinley in Alaska has an altitude of 20,320ft. Water(∆Hvap =
40.7kJ/mol) boils at 77℃ atop Mt. Mckinley. What is the normal
atmospheric pressure at the summit?
답) ln(P2/P1) = -∆Hvap/R[1/T2 - 1/T1] 이므로
ln(760mmHg/x) = (-40.7*103J/mol)/(8.31J/mol∙K)[1/373K - 1/350K]
x = 320.6 = 321mmHg
17. Given the following data about xenon,
normal boiling point = -108℃
normal melting point = -112℃
triple point = -121℃ at 281mmHg
critical point = 16.6℃ at 58atm
(a)Construct an appropriate phase diagram for xenon.
답)
(b)Estimate the vapor pressure of xenon at -115℃
답)약 500mmHg
-121도부터 -108도 까지 13도 증가할 때 압력은 479mmHg 증가했으므로
비례식으로 풀면
13:479=6:x x=221
221+281=502.xxx
약 500mmHg
(c)Is the density of solid Xe larger than that for liquid Xe?
답) yes
책 p.232 melting point 부분 참고
압력의 증가는 더욱 높은 밀도상의 형성을 유리하게 한다. 이 그림에서는 고
체-액체 평형선이 오른쪽으로 기울어져 있어 압력이 증가할 때 고체는 녹는
점 이상의 온도에서도 안정하게 되므로 고체가 더욱 높은 밀도 상을 갖는다.
27.Explain in terms of forces between structural units why
(a)HI has a higher boiling point than HBr
답)dispersion force
HBr보다 HI의 분자크기가 더 큼
(b)GeH4 has a higher boiling point than SiH4
답)dispersion force
(c)H2O2 has a higher melting point than C3H8
답)Hydrogen bonding
(d)NaCl has a higher boiling point than CH3OH
답)Ionic Vs Molecular
33. What are ther strongest attractive forces that must be overcome to
(a)boil silicon hydride SiH4
답)dispersion forces
(b)vaporize calcium chloride
답)ionic bonds
(c)dissolve Cl2 in carbon tetrachloride, CCl4
답)dispersion forces
(d)melt iodine
답)dispersion forces
37.Of the four general types of solid, which one(s)
(a)are generally low-boiling?
답)molecular
(b)are ductile and malleable?
답)metallic
(c)are generally soluble in nonpolar solvent?
답)molecular
table 9.5 참조
49. In the LiCl structure shown in Figure 9.18, the chloride ions form a
face-centered cubic unit cell 0.513nm on an edge. The ionic radius of
Cl- is 0.181nm?
(a)Along a cell edge, how much space is between the Cl- ions?
답)0.513nm-0.181*2nm= 0.151nm
(b)Would an Na+ ion (r= 0.095nm) fit into this space? A K+ ion (r=
0.133nm)?
답)Na+ 2r=0.190nm므로 0.151nm보다 크므로 no fit
K+ 2r=0.266nm 역시 no fit
53. Consider the sodium chloride unit cell shown in Figure 9.18.
Looking only at the front face (five large Cl- ions, four small Na+ ions),
(a)how many cubes share each of the Na+ ions in this face?
답)4개
(b)how many cubes share each of the Cl- ions in this face?
답)모서리의 Cl- 는 8개의 cube와 공유 face 가운데의 Cl-는 2개의 cube와
공유한다.
66. A flask with a volume of 10.0L contains 0.400g of hydrogen gas
and 3.20g of oxygen gas. The mixture is ignited and the reaction
2H2(g) + O2(g) → 2H2O
goes to completion. The mixture is cooled to 27℃. Assuming 100%
yield,
(a)what physical state(s) of water is (are) present in the flask?
답)PV= (mass/MM)RT
답)liquid and vapor
총 3.60g의 water형성
mass = PV*MM/RT 이므로
#물의 27℃에서 증기압은 26.74 mmHg (부록1 참조)
(26.74/760atm)(10.0L)(18.02g/mol)/(0.0821L∙atm/mol∙K)(300K)= 0.257g이
liquid and vapor
(b)What is the final pressure in the flask?
답)26.74 = 26.7mmHg
(c)What is the pressure in the flask if 3.2g of each gas is used?
답)3.46atm
반응의 질량비는 1:8:9 이므로 각 가스가 3.2g씩 사용되면 산소 가스는 모
두 사용되고 수소가스는 2.8g이 남는다. 그리고 3.6g의 물이 생성된다.
이때의 증기압이 26.74mmHg이므로 26.74/760 = 0.035atm
여기에 남은 수소가스의 압력을 더해주면 된다.
P(H2) = (2.80g/2.016g/mol)(0.0821L∙atm/mol∙K)(300K)/10.0L = 3.42atm
0.035+3.42 = 3.46atm
69. As shown in Figure 9.18, Li+ ions fit into a closely packed array of
Cl- ions, but Na+ ions do not. What is the value of the rcation/ranion ratio
at which a cation just fits into a structure of this type?
답)0.414
LiCl 구조는 각각의 Cl 이온이 서로 맞대고 있으므로
1: √2 = rcation + ranion : 2ranion
ranion = √2rcation / (2-√2)
rcation/ranion = √2-1 = 0.414
chap10. Solution
15. 1L의 용액의 무게는 1689g이다.
인산의 무게=0.850☓1689g=1436g
물의 무게=1689g-1436g=253g
×
21.
(a)
(b)흡열반응 이므로 온도가 늘어나면 용해도도 증가한다.
23.
(a) × ×
×
(b) × × ×
(c)
× × ×
× ⋅⋅
33.
⋅⋅×
×
× × ×
×
×
43.
100g 벤젠당 0.435mol의 나프탈렌 존재.
나프탈렌의 무게=×
순도=
×
57.(a)BaSO4
(b) Ba2+(aq)+SO42-(aq)→BaSO4(S)
×
×× ×
SO42-가 더 적으므로 0.04303mol의 BaSO4를 얻는다
BaSO4의 무게=×
(c) ×
69.
(a)바닷물에 녹아있는 이온들이 어는점을 더 낮게 하므로 어는점이 낮다.
(b)설탕은 차가워지면 결정이 된다.
(C)삼투압 때문에 혈관주사의 영양액이 혈액보다 묽으면 혈액 세포 안의 액보다 삼투압이
낮아서 혈액 세포가 파괴될 때까지 혈액 세포 안으로 물이 흘러 들어가고 너무 진하면 물은
세포 안에서 흘러나와 세포가 죽게 된다.
(d)O2가 더 많기 때문에
(e)뚜껑을 열면 압력이 낮아져서 녹아있던 CO2가 기체로 나오기 때문에.
77.(a) Molarity NaOH=
×
(b)NaOH가 한정되어 있다면:1.248mol NaOH->1.872mol H2
Al이 한정되어 있다면:1.508mol Al->2.295mol H2
1.872mol의 H2는 반드시 얻을 수 있다.
(c) ⋅⋅
Chemistry - Masterton & Hurley
CHAPTER 11
7. (a)
(b) instantaneous rate 0.003 /mol L s≈ ⋅
(c) 0.10 /average rate 0.0033 /
30mol L mol L s
s= = ⋅
(d) instantaneous rate < average rate
15.
(a) [ ]
2 2 22
2
2NO N +2O
rate NOk
→
=
(b) ( )21.17 / min 0.250 /
18.7 / minmol L k mol L
k L mol⋅ = ×
= ⋅
(c) [ ] ( )2 22rate NO 18.7 / min 0.800 / 12.0 / mink L mol mol L mol L= = ⋅ × = ⋅
0
0.1
0.2
0.3
0.4
0 10 20 30 40 50 60
[A]
Y 값
17.
(a)
[ ] [ ]( ) ( )
22
28
3 2 2
rate NO Br
1.6 10 / min 0.020 / 0.030 /
1.3 10 / min
k
mol L k mol L mol L
k L mol
−
−
=
× ⋅ = ×
= × ⋅
(b)
[ ] [ ]( ) [ ]
[ ]
22
27 3 2 22
2
rate NO Br
3.5 10 / min 1.3 10 / min 0.043 / Br
Br 0.15 /
k
mol L L mol mol L
mol L
− −
=
× ⋅ = × ⋅ × ×
=
(c)
[ ] [ ] [ ] [ ]
[ ] [ ]
[ ]
2 22
26 3 2 2
NOrate NO Br NO
4NO
2.0 10 / min 1.3 10 / min NO4
NO 0.18 /
k
mol L L mol
mol L
− −
= =
× ⋅ = × ⋅ × ×
=
21.
(a)
2- -2 8S O I
2.22 0.0300.2,3 11.85 0.0250
3.06 0.0275.3, 4 12.22 0.0200
m n
m
n
rate k
Expt m
Expt n
⎡ ⎤ ⎡ ⎤= × ×⎣ ⎦ ⎣ ⎦
⎛ ⎞⇒ = ∴ =⎜ ⎟⎝ ⎠
⎛ ⎞⇒ = ∴ =⎜ ⎟⎝ ⎠
(b) 2- -2 8S O Irate k ⎡ ⎤ ⎡ ⎤= × ×⎣ ⎦ ⎣ ⎦
(c) ( ) ( )
( ) ( )
2- -2 8
4
4
.1
S O I
1.15 10 / min 0.0200 / 0.0155 /
1.15 10 / min 0.371 / min0.0200 / 0.0155 /
Expt
rate k
mol L k mol L mol L
mol Lk L molmol L mol L
−
−
⇒
⎡ ⎤ ⎡ ⎤= × ×⎣ ⎦ ⎣ ⎦× ⋅ = × ×
× ⋅= = ⋅
×
(d)
2- -2 8
3
rate S O I
0.371 / min 0.105 / 0.0875 /3.41 10 / min
k
L mol mol L mol Lmol L−
⎡ ⎤ ⎡ ⎤= × ×⎣ ⎦ ⎣ ⎦= ⋅ × ×
= × ⋅
27.
(a)
[ ]
[ ]
-2 2
-2 2
I H O
0.0052 0.035.1, 2 10.0022 0.015
0.0087 0.050.2, 4 10.0052 0.030
I H O
m n
m
n
rate k
Expt m
Expt n
rate k
⎡ ⎤= × ×⎣ ⎦
⎛ ⎞⇒ = ∴ =⎜ ⎟⎝ ⎠
⎛ ⎞⇒ = ∴ =⎜ ⎟⎝ ⎠
⎡ ⎤∴ = × ×⎣ ⎦
(b)
[ ]( ) ( )
-2 2I H O
.1 0.0022 / min 0.015 / 0.030 /4.9 / min
rate k
Expt mol L k mol L mol Lk L mol
⎡ ⎤= × ×⎣ ⎦⇒ ⋅ = ×
= ⋅
(c) [ ]
[ ]
-
2 2
-2 2
25.0 0.100I 0.050050.025.0 1.00 / 10%
34.02H O 1.470.0500
I H O 4.9 / min 0.0500 / 1.47 / 0.36 / min
mL M MmLmL g mL mol
ML
rate k L mol mol L mol L mol L
×⎡ ⎤ = =⎣ ⎦
× ×⎛ ⎞⎜ ⎟⎝ ⎠= =
⎡ ⎤= × × = ⋅ × × = ⋅⎣ ⎦
35. first-order reactions
(a) ( )
0
1
[ ]ln[ ]150.0ln 1.24 0.75043.21.65
A ktA
mg k hrmg
k hr−
=
= =
=
(b) 1/ 2 1
ln 2 0.693 0.4201.65
t hrk hr−= = =
(c) 11ln 1.65
0.051.8
hr t
t hr
−= ×
=
45. second-order reactions
(a) [ ]
( )( )
1/ 20
1
1 2.65 / min1.51min 0.250 /
tk A
k L molmol L
=
= = ⋅
(b)
[ ] [ ]01 1
1 1 2.650.0915 0.187
10.93 5.35 2.11min2.65
ktA A
t
t
− =
− =
−= =
(c) [ ] ( )2 22 4C H 2.65 / min 0.335 / 0.297 / minrate k L mol mol L mol L= ⋅ × = ⋅
55.
(a)
2
1 1 2
5 2
1 1ln
22.8 1 1ln 5.840.066 8.31 565 273 728 273
2.50 10 2.50 10
a
a
a
Ekk R T T
E
E J kJ
⎛ ⎞= −⎜ ⎟
⎝ ⎠⎛ ⎞= = −⎜ ⎟+ +⎝ ⎠
= × = ×
(b)
3
0.066 250000 1 1ln 3.798.31 758 838
0.066 44.3
1.5 10 / min
k
kk L mol−
⎛ ⎞= − =⎜ ⎟⎝ ⎠
=
= × ⋅
(c) 4
22.8 250000 1 1ln 0.67611.6 8.31 1001
3.01 10 0.676 30.05 30.73
979
T
TT K
⎛ ⎞= − =⎜ ⎟⎝ ⎠
×= + =
=
82.
(a)
2 20 0
,
2
0 62.44 / 26.48 /
2 26.48 62.44 9.48165 9.48 174
f f
o
a reverse
H I HI
H kJ mol H kJ mol
H kJ kJ kJE kJ kJ kJ
+
∆ = ∆ =
∆ = × − = −= + ≈
(b) ( ) ( )
,,
// 9 / 0.00831 973 1.1
/ 0.33
0.33 138 / 46 /
a reversea a reverse
a
E RTE E RTreverse
E RT
reverse
k Ae e e ek Ae
k L mol s L mol s
−− − × −
−= = = = =
= × ⋅ = ⋅
(c) [ ] ( )2 2HI 46 / 0.200 / 1.8 /rate k L mol s mol L mol L s= = ⋅ × = ⋅
83.
0
1 [ ] [ ]
[ ][ ][ ]ln[ ]
d A k Aa dtd A akdtAA aktA
− =
−=
=
Related Documents