SISTEMIK LUPUS ERITEMATOSUS I. DEFINISI Lupus Eritematosus Sistemik Adalah penyakit autoimun yang mengenai multiple organ, ditandai dengan beragam macam autoantibodi terutama antibodi antinukleus (ANA), dimana perlukaan disebabkan oleh deposit kompleks imun dan pengikatan antibodi dengan berbagai sel dan jaringan. Lupus berasal dari bahasa latin yang berarti anjing hutan atau serigala, sedangkan erythematosus dalam bahasa Yunani berarti kemerah-merahan. Istilah lupus erythematosus pernah digunakan pada zaman Yunani kuno untuk menyatakan suatu penyakit kulit kemerahan di sekitar pipi yang disebabkan oleh gigitan anjing hutan. II. EPIDEMIOLOGI Insiden tahunan SLE di Amerika serikat sebesar 5,1 per 100.000 penduduk, sementara prevalensi SLE di Amerika dilaporkan 52 kasus per 100.000 penduduk, dengan rasio jender wanita dan laki-laki antara 9-14:1. Belum terdapat data epidemiologi SLE yang mencakup semua wilayah Indonesia. Data tahun 2002 di RSUP Cipto Mangunkusumo (RSCM) Jakarta, didapatkan 1.4% kasus SLE dari total kunjungan pasien di poliklinik Reumatologi Penyakit Dalam sementara di RS Hasan Sadikin Bandung terdapat 291 Pasien SLE atau 10.5% dari total pasien yang berobat ke poliklinik reumatologi selama tahun 2010. 1

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

SISTEMIK LUPUS ERITEMATOSUS
I. DEFINISI
Lupus Eritematosus Sistemik Adalah penyakit autoimun yang mengenai multiple organ,
ditandai dengan beragam macam autoantibodi terutama antibodi antinukleus (ANA), dimana
perlukaan disebabkan oleh deposit kompleks imun dan pengikatan antibodi dengan berbagai
sel dan jaringan.
Lupus berasal dari bahasa latin yang berarti anjing hutan atau serigala, sedangkan
erythematosus dalam bahasa Yunani berarti kemerah-merahan. Istilah lupus erythematosus
pernah digunakan pada zaman Yunani kuno untuk menyatakan suatu penyakit kulit
kemerahan di sekitar pipi yang disebabkan oleh gigitan anjing hutan.
II. EPIDEMIOLOGI
Insiden tahunan SLE di Amerika serikat sebesar 5,1 per 100.000 penduduk, sementara
prevalensi SLE di Amerika dilaporkan 52 kasus per 100.000 penduduk, dengan rasio jender
wanita dan laki-laki antara 9-14:1. Belum terdapat data epidemiologi SLE yang mencakup
semua wilayah Indonesia. Data tahun 2002 di RSUP Cipto Mangunkusumo (RSCM) Jakarta,
didapatkan 1.4% kasus SLE dari total kunjungan pasien di poliklinik Reumatologi Penyakit
Dalam sementara di RS Hasan Sadikin Bandung terdapat 291 Pasien SLE atau 10.5% dari
total pasien yang berobat ke poliklinik reumatologi selama tahun 2010.
III. ETIOLOGI
Etiologi dari penyakit ini belum seluruhnya diketahui namun diduga :
1. Faktor genetik
Saudara kandung pasien SLE memiliki risiko menderita SLE 30% lebih tinggi
daripada orang yang tidak memiliki saudara penderita SLE. Tingkat penemuan gen
dalam SLE meningkat pada beberapa tahun terakhir. Asosiasi penelitian genom (large
genome-wide association studies (GWAS)) telah mengkonfirmasi adnya asosiasi gen
terhadap respon imun dan inflamasi.
1

2. Efek Epigenetik
Risiko menderita SLE dapat dipengaruhi oleh efek epigenetik seperti metilasi DNA
dan modifikasi post-translasi histone, yang mana dapat terjadi karena faktor keturunan
atau termodifikasi oleh lingkungan. Epigenetik mengacu pada perubahan pada
ekspresi gen yang diturunkan yang disebabkan oleh mekanisme selain perubahan
dasar sequence DNA.
3. Faktor lingkungan
Pencetus SLE dalam lingkungan adalah sinar ultraviolet, obat demethilasi, infeksi
endogen virus. Sinar matahari adalah pencetus yang nyata dari eksaserbasi SLE.
Epstein-barr virus (EBV) telah diidentifikasi sebagai faktor penyebab perkembangan
lupus. EBV dapat bernaung dan berinteraksi dengan B cells dan dan mencetuskan
produksi interferon α (IFNα) oleh sel dendritik plasma (pDCs), peningkatan IFNα di
lupus mungkin bagian dari penyebabnya adalah infeksi kronis dari virus. Obat yang
dimetabolisme dengan asetilasi seperti procainamide and hydralazine dapat
menyebabkan lupus pada pasien yang memiliki asetilator yang lambat.obat ini dapat
merubah ekspresi gen pada CD4+ T cells dengan menginhibisi metilasi dari DNA
yang menginduksi ekspresi berlebihan dari antigen LFA-1, yang menyebabkan
autoreaktivitas. Hydralazine yang digunakan secara luas untuk terapi pada hipertensi.
Sindrom ini terjadi pada 6-7% penderita hipertensi, setelah terapi selama 3 tahun
dengan hydrallazine,dengan dosis 100 mg/hari (5,4%) dan 200 mg/hari (10,4%).
Tetapi tidak terjadi pada pemberian dengan dosis 50 mg/hari.
4. Faktor Hormon
Peningkatan estrogen atau prolaktin dapat menyebabkan penotipe autoimun dengan
peningkatan tinggi afitinas dari autorektif B cells. Biasanya terjadi pada pengguna
estrogen sebagai kontrsepsi oral atau terapi post menopause, dapat juga terjadi pada
wanita hamil pada trimester pertama
5. Jenis kelamin : lebih tinggi pada wanita (11,6%) dibanding pria (2,8%).
IV. PATOGENESIS
Patogenesis SLE sangat kompleks melibatkan kelainan imun multipel termasuk fungsi
abnormal sel B yang terus menerus membentuk antibodi dan membentuk sel T yang
autoreaktif. Di samping itu terjadi pula pembersihan abnormal kompleks imun berakibat
penumpukan dalam jaringan, aktivasi komplemen dan apoptosis sel cacat yang menyebabkan
penumpukan autoantigen yang potensial. Hasil akhir proses di atas adalah induksi radang dan
2

gagal organ termasuk ginjal, jantung, kulit dan sistem saraf. Bukti adanya predidposisis
genetik antara lain adalah peningkatan corcodance penyakit pada kembar monozigot
dibandingkan dengan kembar dizigot, frekuensi penyakit sebesar 10% pada pasien yang
memiliki lebih dari satu anggota keluarga dengan penyakit serupa, dan korelasi gena tertentu.
(terutama MHC kelas II dan III) dengan penyakit dan autoantibodi. C4AQO, alel kelas III
yang defektif dan tidak dapat mengkode protein C4A fungsional, merupakan penanda genetik
yang paling dikaitkan dengan SLE pada banyak kelompok etnik.
Pada suatu populasi, haplotipe extended tertentu, seperti B8, DR3, DQw2, C3AQO,
menimbulkan kecenderungan timbulnya SLE. Asosiasi gen terdapat paling kuat terdapat pada
HLA kelas II (terutama Dqbeta) dan autobaodi yang menentukan subset klinik lupus.
Misalnya titer IgG anti-DNA yang tinggi berkaitan dengan nefritis lupus dan dengan
DQB10201. *0602, dan *0302 yabg diturunkan dengan DR2 dan DR3. Antibodi terhadap
Ro/La (SS-A/SS-B) berkaitan dengan dermatitis pada lupus kutis subakut dengan dan dengan
gen DQA atau DQB tertentu yang diturunkan bersama DR3 (kadang-kadang DR2).
Antikoagulan lupus, yang secara klinis berkaitan dengan pembekuan , berhubungan dengan
DQB*0301, *0302, *0303, dan *0602 yang diturunkan dengan DR4 dan DR7. Gena
kerentanan DQA atau DQB pada setiap kelompok sama-sama memiliki sekuens asam amino
yang mungkin menentukan kemampuan membentuk autoantibodi tertentu. Kajian terhadap
keluarga mengisyaratkan bahwa gena yang tidak berkaitan dengan HLA juga ikut berperan
pada kerentenan dan bahwa, dibandingkan laki-laki, perempuan lebih besar kemungkinannya
mengekspresikan gejala autoimun genotipenya. Makin banyak seseorang memiliki gena
kerentanan, makin tinggi risiko relatif SLE; mungkin diperlukan tiga atau empat gena yang
berlainan.
Faktor lingkungan yang menyebabkan timbulnya SLE timbulnya tidak diketahui, kecuali
sinar UV-B (dan kadang-kadang UV-A). Hampir 70% pasien bersifat fotosensitif. Faktor lain
yang diduga berperan antara lain adalah memakan minyak wijen (alfafa sprout) dan zat
kimia, seperti hidrazin dan pewarna rambut. S\sekarang sedang dilakukan penelitian untuk
mencari virus atau retrovirus sebagai penginduksi tetapi hasilnya belum dapat disimpulakan.
Walaupun beberapa beberapa obat dapat menginduksi penyakit mirip lupus, lupus spontan
dan lupus akibat obat memiliki perbedaan klinis maupun antibodi. Jenis kelamin perempuan
jelas merupakan faktor kerentanan, karena prevalensi pada perempuan berusia subur adalah
tujuh sampai sembilan kali lebih tinggi dari pada laki-laki, sedangkan rasio perempuan
dibandingkan laki-laki adalah 3:1 pada masa pra- dan pasca menopause. Pada pasien lupus,
3

metabolisme hormon estrogenik dan androgenik abnormal.hormon seks jugamempengaruhi
toleransi imun.
Respon imun abnormal nyang ditemukan termasuk juga pembentukan teru menerus subset
autoantibodi dan komplek imun yang patogenik. Belum diketahui adanya gena
imunoglunulin yang secara ekslusif mengkode autobodi yang merugikan , walaupun gena
regio V tertentu (terutama VH) tampaknya sering terpakai, dan mungkin terdapat seleksi
klonal sel B yang mengeksresikan antibodi beraviditas tinggi terhadap autoantigen. Pada
sebagian model lupus pada murine, peran sel T penolong sangat menentukan timbulnya
penyakit. Telah dilakukan penelitian supresi sel T sebagai intervensi terapeutic untuk pasien.
Kelainan yang memungkinkan hiperaktivasi sel T dan B autoreaktif mendominasi respons
imun pada SLE masih belum diketahui. Sel ini lolos dari meskanisme toleransi normal;
mereka tidak mengalami deplesi atau anergi. Bukti terbaru pada tikus mengisyaratkan bahwa
gangguan apoptosis, yang dikode secara genetis, mungkin menghambat eliminasi sel
autoreaktif. Terdapat bukti bahwa prekusor sel induk sumsum tulang untuk sel B dan
mungkin sel T, secara intrinsik tidak normal. Selain itu, mungkin lingkungan mikro tempat
sel induk ini berkembang yang tidak normal. Kemungkinan gena, hormon seks, dan antigen
eksogen mempengaruhi toleransi dan pengaktifan sel. Selain itu, sel ini mungkin mengalami
4

perubahan akibat adanya antibodi antilimfosit. Struktur antigen yang merangsang
autoantibodi masih dalam penelitian. Beberapa diantaranya jelas berasal dari diri-sendiri
( histon, RNP< antige permukaan eritrosit); sebagian lainnya mungkin berasal dari
lingkungan luar dan mirip dengan komponen diri (mis. Komponen virus stomatis vesikuler
mirip dengan peptida pada antigen Ro). Beberapa autoantibodi menginduksi penyakit melalui
reaksi langsung dengan antigennya, misalnya antibodi yang ditujukan kepada antigen
permukaan eritrosit dan trombosit. Sebagian lagi mungkin melekat ke membaran sel
(misalnya membrana basal glomelurus, MBG) melalui muatan kation atau karena mereka
bereaksi silang dengan komponen jaringan. Juga dapat terjadi perubahan fungsi sel setelah
antibodi berikatan dengan antigen dengan membrana tanpa tergantung pada pengaktifan
komplemen. SLE terjadi jika terdapat kelainan pengaturan respon imun. Pembersihan
komplek-imun tidak adekuat. Reseptor CR1 pada eritrosit jumlahnya sedikit. (biasnya
reseptor tersebut berkurang akibat tingginya kadar komplek imun, kadang-kadang karena
kontrol genetik) sehingga banyak KI tidak ditranspotasikan ke sistem fagosit mononukleus
(SFM). SFM tidak mampu mengolah KI secara normal jaringan idiotipe-anti-idiotipe tidak
dapat menekan sel T dan B yang hiperaktif. Pada SLE, sebagian besar fungsi limfosit T
menjadi fungsi penolong: sel T CD4+CD8, CD4-CD8+, CD4-CD8-, alfa/beta, dan
gama/delta telah dibuktikan membantu sel B memproduksi autoantibodi. Dengan demikian,
fungsi penekan yang biasanya dimiliki oleh sel CD4-CD8+ dan sel NK menghilang.
Akhirnya, mekanisme toleransi normal yang melenyapkan atau menginaktifkan limfosit T
dan B yang sangat autoreaktif juga terganggu.
Secara ringkas sebagai individu secera genetis memiliki kecenderungan mengalami SLE.
Dibawah pengaruh berbagai gena. Sering dicetuskan oleh pengaruh lingkungan dan sangat
dipengaruhi oleh jenis kelamin, individu tersebut dapat mengalami berbagai sindroma klinis
yang memenuhi kriteria SLE. Penyebab sindroma ini sangat kompleks dan mungkin berbeda
untuk tiap-tiap pasien.
V. MANIVESTASI KLINIS
SLE adalah penyakit autoimun multisistem yang dapat bersifat eksaserbasi dan remisi.
Penyakit ini menyerang berbagai macam organ seperti kulit, ginjal, muskuloskeletal, saraf,
kardiovaskular, serta rongga mulut. Sebanyak 50-70% pasien SLE mengalami gangguan pada
ginjalnya. Keterlibatan ginjal merupakan penyebab utama tingginya morbiditas dan
5

mortalitas pada populasi ini. Secara klinis, penyakit ginjal pada SLE berawal dari proteinuria
asimtomatik yang kemudian berkembang dengan cepat menjadi glomerulonefritis progresif
disertai dengan gagal ginjal. Sekitar 95% pasien SLE dapat menunjukkan manifestasi pada
muskuloskeletal. Arthralgia, deformitas sendi, kelainan sendi temporomandibular dan
nekrosis avaskular telah dilaporkan terjadi pada pasien SLE. Pada kulit, manifestasi SLE
disebut juga lupus dermatitis. Lupus dermatitis dapat dibagi menjadi discoid lupus
erythematosus (DLE) dan subacute cutaneous lupus erythematosus (SCLE). Kebanyakan
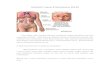
gambaran klinis SLE pada kulit berupa lesi diskoid yang umum bersifat fotosensitif, eritema
sedikit meninggi, bersisik, pada wajah bagian pipi dan sekitar hidung yang disebut buterfly
rash karena membentukseperti sayap kupu-kupu (Gambar 1), telinga, dagu, daerah leher,
punggung atas, dan bagian ekstensor dari lengan. Sebanyak 5% individu dengan DLE
memiliki SLE namun, diantara individu dengan SLE, sebanyak 20% memiliki DLE.
Tingkat keparahan butterfly rush, kadang disertai dengan serangan penyakit sistemik. SCLE
dapat menimbulkan bercak merah bersisik mirip dengan psoriasis atau lesi sirkuler datar
kemerahan. Pasien dengan manifestasi ini sangat fotosensitif; kebanyakan memiliki antibodi
terhadap Ro (SS-A). Manifestasi SLE pada kulit lainnya dapat ditemukan berupa urtikaria
rekuren, dermatitis lichen planus-like, bulla, dan panikulitis. Timbulnya manifestasi sistem
saraf pusat (SSP) dapat terjadi pada sekitar 20% pasien SLE dan biasanya disebabkan oleh
vaskulitis serebral atau kerusakan saraf langsung. Manifestasi SSP terdiri dari psikosis,
stroke, kejang, myelitis dan dapat memperburuk keseluruhan prognosis dari penyakit SLE.
SLE dapat melibatkan kardiovaskular, berupa vaskulitis dan perikarditis. Selain itu,
kerusakan endokardium, miokarditis, dan cacat konduksi biasanya juga terjadi. Selama
kelangsungan hidup pasien SLE, arterosklerosis akan meningkat dengan dipercepat oleh
6

penyakit arteri koroner, dan hal ini telah menjadi masalah klinis yang penting. Berdasarkan
sebuah studi, dinyatakan bahwa infark miokardium, gagal jantung, dan stroke adalah 8,5,
13,2 dan 10,1 kali lebih sering terjadi pada perempuan dengan SLE dibandingkan dengan
populasi umum. Kecenderungan peningkatan trombosis pada SLE dipengaruhi oleh adanya
kelainan pada fibrinolisis, protein antikoagulan (protein S), dan adanya antibodi
antifosfolipid. SSP dan trombosis vena dengan emboli paru adalah penyebab utama
morbiditas pada pasien SLE. Sebagai pencegahan pasien SLE membutuhkan antikoagulan
tingkat tinggi.
Derajat Berat Ringannya Penyakit SLE
7

Seringkali terjadi kebingungan dalam proses pengelolaan SLE, terutama menyangkut obat
yang akan diberikan, berapa dosis, lama pemberian dan pemantauan efek samping obat yang
diberikan pada pasien. Salah satu upaya yang dilakukan untuk memperkecil berbagai
kemungkinan kesalahan adalah dengan ditetapkannya gambaran tingkat keparahan SLE.
Penyakit SLE dapat dikategorikan ringan atau berat sampai mengancam nyawa.
Kriteria untuk dikatakan SLE ringan adalah:
1. Secara klinis tenang
2. Tidak terdapat tanda atau gejala yang mengancam nyawa
3. Fungsi organ normal atau stabil, yaitu: ginjal, paru, jantung, gastrointestinal, susunan
saraf pusat, sendi, hematologi dan kulit.
Contoh SLE dengan manifestasi arthritis dan kulit.
Penyakit SLE dengan tingkat keparahan sedang manakala ditemukan:
1. Nefritis ringan sampai sedang ( Lupus nefritis kelas I dan II)
2. Trombositopenia (trombosit 20-50x10/mm3)
3. Serositis mayor
Penyakit SLE berat atau mengancam nyawa apabila ditemukan keadaan sebagaimana
tercantum di bawah ini, yaitu:
1. Jantung: endokarditis Libman-Sacks, vaskulitis arteri koronaria, miokarditis,
tamponade jantung, hipertensi maligna.
2. Paru-paru: hipertensi pulmonal, perdarahan paru, pneumonitis, emboli paru, infark
paru, ibrosis interstisial, shrinking lung.
3. Gastrointestinal: pankreatitis, vaskulitis mesenterika.
4. Ginjal: nefritis proliferatif dan atau membranous.
5. Kulit: vaskulitis berat, ruam difus disertai ulkus atau melepuh (blister).
6. Neurologi: kejang, acute confusional state, koma, stroke, mielopati transversa,
mononeuritis, polineuritis, neuritis optik, psikosis, sindroma demielinasi.
7. Hematologi: anemia hemolitik, neutropenia (leukosit <1.000/mm), trombositopenia <
20.000/m, purpura trombotik trombositopenia, trombosis vena atau arteri.
8

VI. DIAGNOSIS
Diagnosis penyakit SLE sangat sulit untuk ditegakkan. Selain dapat menimbulkan kerusakan
beberapa organ dalam, gejala dari penyakit ini juga terlihat sangat bervariasi dan tidak sama
pada setiap penderita.
9

Bila dijumpai 4 atau lebih kriteria diatas, diagnosis SLE memiliki sensitiitas 85% dan�
spesiisitas 95%. Sedangkan bila hanya 3 kriteria dan salah satunya ANA positif, maka sangat�
mungkin SLE dan diagnosis bergantung pada pengamatan klinis. Bila hasil tes ANA negatif,
maka kemungkinan bukan SLE. Apabila hanya tes ANA positif dan manifestasi klinis lain
tidak ada, maka belum tentu SLE, dan observasi jangka panjang diperlukan.
10

Gejala yang dapat timbul berupa demam berkepanjangan, foto sensitifitas, perubahan berat
badan, kelenjar limfe yang membengkak, dan terjadi perubahan terhadap beberapa organ vital
lainnya. SLE pada tahap awal, seringkali memberikan gambaran seperti penyakit lain
misalnya artritis reumatoid, gelomerulonefritis, anemia, dermatitis, dan sebagainya. Oleh
karena itu, ketepatan diagnosis dan deteksi dini penyakit SLE penting untuk diperhatikan,
mengingat gejala penyakit ini sama dengan penyakit lain. Pada tahun 1982, American
Collage Of Rheumatology membuat suatu kriteria yang dapat menjamin akurasi diagnosis
lupus yaitu sampai ketepatan 98% dan pada tahun 1997 telah di revisi.
Pemeriksaan Penunjang Minimal Lain yang Diperlukan untuk Diagnosis dan
Monitoring:
1. Hemoglobin, lekosit, hitung jenis sel, laju endap darah (LED)*
2. Urin rutin dan mikroskopik, protein kwantitatif 24 jam, dan bila diperlukan kreatinin
urin.
3. Kimia darah (ureum, kreatinin, fungsi hati, proil lipid)*�4. PT, aPTT pada sindroma antifosfolipid
5. Serologi ANA, anti-dsDNA, komplemen (C3,C4))
6. Foto polos thorax
§ pemeriksaan hanya untuk awal diagnosis, tidak diperlukan untuk monitoring
* Setiap 3-6 bulan bila stabil
† Setiap 3-6 bulan pada pasien dengan penyakit ginjal aktif.
ANA, antibodi antinuklear; PT/PTT, protrombin time/partial tromboplastin time.
Pemeriksaan tambahan lainnya tergantung dari manifestasi SLE. Waktu pemeriksaan untuk
monitoring dilakukan tergantung kondisi klinis pasien.
Pemeriksaan Serologi pada SLE
Tes imunologik awal yang diperlukan untuk menegakkan diagnosis SLE adalah tes ANA
generik.(ANA IF dengan Hep 2 Cell). Tes ANA dikerjakan/diperiksa hanya pada pasien
dengan tanda dan gejala mengarah pada SLE. Pada penderita SLE ditemukan tes ANA yang
11

positif sebesar 95-100%, akan tetapi hasil tes ANA dapat positif pada beberapa penyakit lain
yang mempunyai gambaran klinis menyerupai SLE misalnya infeksi kronis (tuberkulosis),
penyakit autoimun (misalnya Mixed connective tissue disease) (MCTD), artritis rematoid,
tiroiditis autoimun), keganasan atau pada orang normal.
Jika hasil tes ANA negatif, pengulangan segera tes ANA tidak diperlukan, tetapi perjalanan
penyakit reumatik sistemik termasuk SLE seringkali dinamis dan berubah, mungkin
diperlukan pengulangan tes ANA pada waktu yang akan datang terutama jika didapatkan
gambaran klinis yang mencurigakan. Bila tes ANA dengan menggunakan sel Hep-2 sebagai
substrat; negatif, dengan gambaran klinis tidak sesuai SLE umumnya diagnosis SLE dapat
disingkirkan.
Beberapa tes lain yang perlu dikerjakan setelah tes ANA positif adalah tes antibodi terhadap
antigen nuklear spesi ik, termasuk anti-dsDNA, Sm, nRNP, Ro(SSA), La (SSB), Scl-70 dan
anti-Jo. Pemeriksaan ini dikenal sebagai profil ANA/ENA. Antibodi anti-dsDNA merupakan
tes spesi ik untuk SLE, jarang didapatkan pada penyakit lain dan spesi itasnya hampir 100%.
Titer anti-dsDNA yang tinggi hampir pasti menunjukkan diagnosis SLE dibandingkan
dengan titer yang rendah. Jika titernya sangat rendah mungkin dapat terjadi pada pasien yang
bukan SLE.
Kesimpulannya, pada kondisi klinik adanya anti-dsDNA positif menunjang diagnosis SLE
sementara bila anti ds-DNA negatif tidak menyingkirkan adanya SLE. Meskipun anti-Sm
didapatkan pada 15% -30% pasien SLE, tes ini jarang dijumpai pada penyakit lain atau orang
normal. Tes anti-Sm relatif spesi ik untuk SLE, dan dapat digunakan untuk diagnosis SLE.
Titer anti-Sm yang tinggi lebih spesi ik untuk SLE. Seperti anti-dsDNA, anti-Sm yang
negatif tidak menyingkirkan diagnosis.
Penilaian Aktivitas Penyakit SLE
Perjalanan penyakit SLE yang ditandai dengan eksaserbasi dan remisi, memerlukan
pemantauan yang ketat akan aktivitas penyakitnya. Evaluasi aktivitas penyakit ini berguna
sebagai panduan dalam pemberian terapi. Indeks untuk menilai aktivitas penyakit seperti
SLEDAI, MEX-SLEDAI, SLAM, BILAG Score, dsb. Dianjurkan untuk menggunakan
MEX-SLEDAI atau SLEDAI. MEX-SLEDAI lebih mudah diterapkan pada pusat kesehatan
primer yang jauh dari tersedianya fasilitas laboratorium canggih.
12

13

VII. TATALAKSANA
Pengobatan imunosupresif merupakan pengobatan utama bagi SLE berat dan telah terbukti
efektif mengurangi beberapa gejala sisa SLE termasuk penyakit ginjal stadium akhir namun
tidak terbukti memperbaiki morbiditas dan mortalitas. Di samping itu pengobatan tersebut
dapat meningkatkan risiko infeksi serius, toksik terhadap jaringan dan organ di luar sistem
imun.
Obat harus efektif dan aman dengan memperhatikan tahapan patofisiologi perkembangan
autoimun, respons imun abnormal yang terus menerus dan kerusakan jaringan akibat
imunitas yang dibutuhkan untuk mengenal dan menentukan sasaran sangat spesifik.
14

Pengetahuan mekanisme SLE dapat digunakan untuk memilih obat lebih baik yang ditujukan
pada target. Target terhadap sel B dan sel T akan memperbaiki hasil induksi remisi.
Manifestasi tertentu SLE seperti penyakit kulit yang refrakter dan nefritis berhasil diatasi
dengan baik dengan antagonis TNF-a dan anti IL-6.
Pilar Pengobatan Lupus Eritematosus Sistemik
1. Edukasi dan konseling
2. Program rehabilitasi
3. Pengobatan medikamentosa
a. OAINS
b. Anti malaria
c. Steroid
d. munosupresan / Sitotoksik
e. Terapi lain
1. Edukasi / Konseling
Pada dasarnya pasien SLE memerlukan informasi yang benar dan dukungan dari sekitarnya
dengan maksud agar dapat hidup mandiri. Perlu dijelaskan akan perjalanan penyakit dan
kompleksitasnya. Pasien memerlukan pengetahuan akan masalah aktivitas isik, mengurangi�
atau mencegah kekambuhan antara lain melindungi kulit dari paparan sinar matahari (ultra
violet) dengan memakai tabir surya, payung atau topi; melakukan latihan secara teratur.
Pasien harus memperhatikan bila mengalami infeksi. Perlu pengaturan diet agar tidak
kelebihan berat badan, osteoporosis atau terjadi dislipidemia. Diperlukan informasi akan
pengawasan berbagai fungsi organ, baik berkaitan dengan aktivitas penyakit ataupun akibat
pemakaian obat-obatan. Butir-butir edukasi pada pasien.
15

2. Program Rehabilitasi
Terdapat berbagai modalitas yang dapat diberikan pada pasien dengan SLE tergantung
maksud dan tujuan dari program ini. Salah satu hal penting adalah pemahaman akan
turunnya masa otot hingga 30% apabila pasien dengan SLE dibiarkan dalam kondisi
immobilitas selama lebih dari 2 minggu. Disamping itu penurunan kekuatan otot akan terjadi
sekitar 1-5% per hari dalam kondisi imobilitas. Berbagai latihan diperlukan untuk
mempertahankan kestabilan sendi. Modalitas fisik seperti pemberian panas atau dingin�
diperlukan untuk mengurangi rasa nyeri, menghilangkan kekakuan atau spasme otot.
Demikian pula modalitas lainnya seperti transcutaneous electrical nerve stimulation (TENS)
memberikan manfaat yang cukup besar pada pasien dengan nyeri atau kekakuan otot. Secara
garis besar, maka tujuan, indikasi dan tekhnis pelaksanaan program rehabilitasi yang
melibatkan beberapa maksud di bawah ini, yaitu:
a. Istirahat
b. Terapi isik�
c. Terapi dengan modalitas
d. Ortotik
e. Lain-lain.
16

3. Medikamentosa
Imunosupresi dengan target sel B
Sebagian besar sel B terlibat dalam patogenesis SLE sebagai sumber autoantibodi, sebagai
antigen-presenting cells (APC), sebagai pemrakarsa serta pengatur radang melalui sekresi
sitokin. Sel B merupakan target pengobatan imunosupresi termasuk anti-CD20 monoclonal
antibody (rituximab) dan anti-B lymphocyte stimulator (BLyS).
Anti-CD20 Antibody
Antibodi untuk mengurangi jumlah sel B pada SLE yaitu antibodi monoklonal terhadap
CD20 (rituximab). Ekspresi CD20 terjadi pada awal perkembangan limfosit B. Pemberian
rituximab akan mengurangi limfosit B positif CD20 dengan cepat, setelah itu terjadi remisi
dengan sel B asli yang tidak terpapar antigen. Efek samping rituximab yang paling sering:
reaksi transfusi (30–35%), neutropenia (8%), dan produksi human antichimeric antibodies
(9%). Kasus fatal yang jarang terjadi termasuk progressive multifocal leukoencephalopathy
17

yang disebabkan polyomavirus JC. Monoclonal anti-CD20 antibodies yang baru termasuk
ocrelizumab, merupakan recombinant humanized monoclonal anti-CD20 antibody telah
dicoba pada SLE ekstrarenal dan nefritis lupus.
18

Anti-CD22 Antibodies - Epratuzumab
Fungsi epratuzumab adalah untuk mengatur fungsi sel B tanpa mengurangi jumlahnya.
Dalam penelitian obat tersebut digunakan untuk SLE sedang sampai berat dengan hasil baik
dan aman serta mengurangi kebutuhan dosis kortikosteroid.
B-Lymphocyte Tolerogens – Abetimus (LJP-394)
Obat ini merupakan tolerogen terhadap sel B yang menyebabkan apoptosis sel B. Abetimus
telah diteliti pada manusia baik penderita lupus non renal maupun lupus nefritis. Tolerogen
lain, yaitu TV-4710 (Edratide), merupakan peptida yang disusun oleh 19 asam amino.
BLyS Blockers
B-cell survival molecule B-lymphocyte stimulator (BLyS) yang juga disebut B-cell activation
factor of the TNF family (BAFF) berperan kunci dalam aktivasi dan diferensiasi sel B
sehingga dapat digunakan sebagai target yang baik untuk intervensi SLE. Penghambatan
BLyS akan mengurangi sel B dan bermakna meningkatkan aktivasi imun.
Contoh obat ini belimumab merupakan human monoclonal antibody yang berikatan dengan
BLyS sehingga menghambat aktivitas biologinya. FDA (Food And Drug Administration)
Amerika Serikat telah menyetujui obat tersebut untuk pengobatan SLE. Penghambat BlyS
lain atacicept ( TACI-Ig) merupakan soluble transmembrane activator dan calcium-modulator
19

dan cyclophilin ligand interactor ( TACI) receptor, yang mengikat BAFF. Obat ini ditoleransi
baik oleh penderita SLE.
Imunosupresi dengan target sel T
Aktivasi sel T membutuhkan interaksi rangsangan CD28:B7. CD28 terekspresi pada sel T
sedangkan ligand B7-1 dan B7-2 (CD80 dan CD86) ditemukan pada APC (Antigen
Precenting Cell). Abatacept dapat menghambat interaksi tersebut. Suatu antibodi monoklonal
efalizumab dapat langsung menghambat CD11a yang berperan penting untuk aktivasi,
reaktivasi, ekstravasasi dan mengalirkan sel T ke kulit. Dengan demikian pemberian obat ini
dapat mengurangi manifestasi kulit penderita SLE.
Imunosupresi yang menghambat sitokin
Sitokin yang berperan pada proses radang, yang selanjutnya akan menyebabkan kerusakan
jaringan dan organ, termasuk tumor necrosis factor alpha ( TNF-a), interferon alpha/gamma
(IFN-a/γ) dan interleukin (IL) 1, 6, 10, 15, dan 18. Sitokin-sitokin tersebut potensial sebagai
target pengobatan untuk mengurangi radang kronis pada SLE.
Anti-TNF-a
TNF-a pada SLE dapat meningkatkan apoptosis dan berpengaruh bermakna pada aktifi tas sel
B, sel T dan sel detritus. Selain itu anti TNF-a menghambat pembentukan autoantibodi
termasuk antinuclear, anti-dsDNA dan anti cardiolipin. Ada beberapa preparat anti TNF-a
yang tersedia termasuk infl iximab, adalimumab, golimumab, certolizumab pegol dan
etanercept.
Anti-IFN-a/γ
IFN-a berperan bermakna pada patogenesis SLE dan berkorelasi dengan aktivitas penyakit
dan komplikasi ginjal. Obat anti INF-a termasuk sifalimumab (MEDI-545) dan rontalizumab
serta obat anti INF-γ (AMG 811) merupakan obat yang aman serta ditoleransi penderita SLE.
Anti-IL-1
Pada SLE, kadar serum TNF dan anti-dsDNA antibody meningkatkan kadar serum IL-1,
peningkatan kadar IL-1 dihubungkan dengan aktifi tas penyakit dan kadar rendah antagonis
reseptor IL-1 dihubungkan dengan nefritis lupus. Anakinra menetralkan aktivitas biologi IL-
1; obat ini aman pada penderita SLE dan efektif memperbaiki artritis.
20

Anti-IL-6
IL-6 menginduksi diferensiasi sel B menjadi sel plasma, sekresi antibodi dan hiperaktif, di
samping itu juga mendorong proliferasisel T, diferensiasi cytotoxic T-cell dan radang lokal.
Ekspresi IL-6 pada nefritis lupus tinggi sehingga digunakan anti IL-6 (tocilizumab).
Neutropeni merupakan efek samping yang sering terjadi pada pemberian tocilizumab.
Anti-IL-10
IL-10 diproduksi oleh sel Th2 dan menghambat sitokin untuk sel T. Kadar IL-10 pada SLE
meningkat dan dihubungkan dengan aktifitas penyakit. Pemberian anti IL-10 akan
menurunkan titer anti-dsDNA antibody dan menghambat terjadinya proteinuria dan
glomerulonefritis.
Anti-IL-15
IL-15 terutama diproduksi oleh makrofag dan ditemukan meningkat pada 40% penderita
SLE, namun peningkatan tersebut tidak berhubungan dengan aktivitas penyakit. Obat anti IL-
15 sedang dicoba untuk penyakit autoimun lain.
Anti-IL-18
IL-18 merupakan sitokin proinfl amasi yang erat hubungannya dengan IL-1. Berbagai
penelitian menemukan peningkatan kadar serum IL-18 pada penderita SLE yang
dihubungkan dengan kadar TNF. Sampai saat ini penghambat IL-18 belum digunakan pada
SLE manusia.
Imunosupresan menghambat komplemen
Sistem komplemen terdiri dari 3 jalur dan lebih dari 30 protein terlibat secara langsung atau
tidak langsung memperantarai efek komplemen. Sistem komplemen mempunyai efek
proteksi terhadap SLE sedangkan pada keadaan defisiensi komponen jalur klasik
dihubungkan dengan peningkatan risiko SLE. Deposisi kompleks imun menyebabkan sistem
komplemen aktif dan meningkatkan respons radang. Ada dua penghambat komplemen yaitu
TP10 dan eculizumab yang walaupun belum ada penelitian klinik, mungkin dapat digunakan
sebagai pengobatan SLE.
VIII. PROGNOSIS
21

Morbititas dan mortalitas pasien SLE masih cukup tinggi. Berturut-turut kesintasan (survival)
SLE untuk 1-5, 5-10, 10-15, 15-20, dan 20 tahun adalah 93-97%, 53-64%, 64-80%, 70-85%
Kesintasan 5 tahun pasien SLE di RSCM adalah 88% dari pengamatan terhadap 108 orang
pasien SLE yang berobat dari tahun 1990-2002, Angka kematian pasien dengan SLE hampir
5 kali lebih tinggi dibandingkan populasi umum. Pada tahun-tahun pertama mortalitas SLE
berkaitan dengan aktivitas penyakit dan infeksi (termasuk infeksi M. tuberculosis, virus,
jamur dan protozoa, sedangkan dalam jangka panjang berkaitan dengan penyakit vaskular
aterosklerosis.
Daftar pustaka:
22

1. Kasper DL, Hausel Sl. Harrison’s principle of internal medicine. 19th Ed. New york:
Mc GrawHill; 2015. P. 2878-90.
2. Papadakis MA, McPhee SJ. Current medical diagnosis and treatment. 55th Ed.
Chicago: Mc GrawHill; 2016. P. 842-77.
3. Walker BR, Colledge BR. Davidson’s principle and practice of medicine. 22nd Ed.
British: Elsevier; 2014. P. 1130-50.
4. Wallace DJ, Hhan BH. Dubois Lupus Erythematosus and Related Syndromes Expert
Consult. 8th Ed. British: Elsevier; 2014. P. 590-631.
5. Kumar V, Abas AK. Robbins Cotran Pathologic Basis of Disease. 9th Ed.
Philadelphia: Elsevier; 2015. P. 226-57.
6. Krishnan S, Chowdhury B, Juang Y-T, Tsokos GC. Overview of the Pathogenesis of
Systemic Lupus Erythematosus. Philadelphia: Mosby, Inc.; 2007. p. 55-63.
7. Kyttaris VC, Tsokos GC. New Treatments in Systemic Lupus Erythematosus.
Philadelphia: Mosby, Inc.; 2007. p.516-23.
8. Postal M, Costallat LT, Appenzeller S. Biological therapy in systemic lupus
erythematosus. Int J Rheumatol. 2012;2012:578-641.
9. Perhimpunan reumatologi Indonesia. Diagnosis dan pengelolaan lupus eritematosus
sistemik. Jakarta: PSDPI; 2011. P. 1-54.
10. Lahita G, ed. Systemic lupus erythematosus, 5th edn. Amsterdam: Elsevier, 2011. P.
476-505.
23
Related Documents