Modulo 16: La fosforilazione ossidativa 1

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

Modulo 16: La fosforilazione ossidativa
1

2
La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E� costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti prodotti durante le reazioni ossidative vengono ossidati nella catena di trasporto degli elettroni, lungo la quale gli elettroni vengono trasferiti all�ossigeno molecolare La catena respiratoria di trasporto degli elettroni è un sistema di complessi proteici localizzati nella membrana mitocondriale interna (membrana plasmatica delle cellule procariotiche) Tre di questi complessi sono ossidoreduttasi che pompano protoni, cioè generano un gradiente di protoni attraverso la membrana mitocondriale interna 2. Il gradiente di protoni è una fonte di energia libera che viene dissipata quando i protoni passano nuovamente attraverso la membrana mitocondriale interna tramite il complesso ATP sintasi In questo processo si forma ATP

3
E.Kennedy, A.Lehningher (1948): nelle cellule eucariotiche la fosforilazione avviene nei mitocondri. Questa scoperta rappresenta storicamente l�inizio degli studi sulla trasduzione energetica nei sistemi biologici
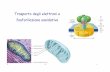
I mitocondri derivano probabilmente da batteri aerobici, contenenti già la fosforilazione ossidativa, entrati in rapporto simbiotico con cellule anaerobiche primitive di eucarioti Come i batteri gram-negativi, i mitocondri hanno due membrane

La fosforilazione ossidativa
4
} Gli e- sono tras fer i t i a l l ’O2 indirettamente mediante la catena respiratoria.
} L’energia libera resa disponibile dal flusso degli elettroni lungo la catena respiratoria è utilizzata per formare un gradiente protonico (l’energia libera conservata sotto forma di potenziale elettrochimico).
} Il flusso transmembrana di protoni in senso inverso viene sfruttato per generare ATP da ADP e Pi.
} NADH e FADH2 trasferiscono e- ad alto potenziale di trasferimento all’O2 liberando una quantità di energia sufficiente per generare ATP. Il processo prende il nome di fosforilazione ossidativa.
La catena respiratoria è formata da quattro complessi proteici trasmembrana I, II, III e IV, e 2 fattori solubili l’ubichinone (coenzima Q) ed la proteina citocromo C.

Il potenziale di trasferimento degli elettroni: potenziali di riduzione (E’0)
5
Ossidante Riducente n E´0(V) Succinate + CO2 α-Ketoglutarate 2 - 0.67 Acetate Acetaldehyde 2 - 0.60 Ferredoxin (oxidized) Ferredoxin (reduced) 1 - 0.43 2 H+ H2 2 - 0.42 NAD+ NADH + H+ 2 - 0.32 NADP+ NADPH + H+ 2 - 0.32 Lipoate (oxidized) Lipoate (reduced) 2 - 0.29 Glutathione (oxidized) Glutathione (reduced) 2 - 0.23 FAD FADH2 2 - 0.22 Acetaldehyde Ethanol 2 - 0.20 Pyruvate Lactate 2 - 0.19 Fumarate Succinate 2 0.03 Cytochrome b (+3) Cytochrome b (+2) 1 0.07 Dehydroascorbate Ascorbate 2 0.08 Ubiquinone (oxidized) Ubiquinone (reduced) 2 0.10 Cytochrome c (+3) Cytochrome c (+2) 1 0.22 Fe (+3) Fe (+2) 1 0.77 ½ O2+ 2 H+ H2O 2 0.82
Ox + 2e- + 2H+ → red H2
E´0 è il potenziale di riduzione standard (pH 7, 25°C) ed n è i l numero d i e le t t ron i trasferiti. E´0 si riferisce alla r e a z i o n e p a r z i a l e (semireazione) dell’ossidante che si riduce

Relazione tra ΔE°’ e ΔG°’
6
In una reazione di ossidoriduzione, gli elettroni si muovono spontaneamente verso atomi o molecole che hanno un potenziale di riduzione maggiore:
ΔE°’=Eacc°’- Edon°’
se ΔE°’>0 La reazione procede spontaneamente nella direzione scritta. La differenza di potenziale di riduzione ΔE permette di calcolare la variazione di energia libera (ΔG)
ΔGo’ = -nF ΔEo’
n = numero di elettroni, F= costante di Faraday (96,48 kJ mol-1 V-1 la quantità di carica di una mole di elettroni) Una reazione di ossidazione-riduzione con un valore positivo di ΔE avrà un valore di ΔG negativo e procederà spontaneamente.

Differenza di potenziale tra NADH e ossigeno molecolare
7
½ O2 + 2 H+ + 2 e- → H2O E´0 (V) = + 0.82 V NAD+ + H+ + 2 e- → NADH E´0 (V) = - 0.32 V
La reazione complessiva è:
½ O2 + NADH + H+ → H2O + NAD+ ΔE´0=Eacc´0- Edon´0 = (+0.82 V) - (-0.32 V ) = 1,14 V
ΔGo’ = -nF ΔEo’ = -2 x 96,48 kJ mol-1 V-1 x (1,14 V) = -220 kJ mol-1
Si ricorda che dall’idrolisi dell’ATP si ricava -30,5 kJ mol-1 per la sua sintesi sono necessari 30,5 kJ mol-1 L’ossidazione del NADH si ricava una quantità sufficiente per sintetizzare ATP, avviene indirettamente ed è accompagnata dalla formazione di un gradiente protonico.
Quanta energia viene rilasciata dalla ossidazione di NADH da parte dell’ossigeno?

8
Ubichinone (Coenzima Q) Benzochinone con catena laterale isoprenoide Può accettare un solo elettrone, trasformandosi in un radicale semichinonico, oppure può accettare due elettroni trasformandosi nella forma completamente ridotta (Ubichinolo) Come le flavoproteine, può mettere in relazione processi a due elettroni con altri ad un elettrone E� di piccole dimensioni ed idrofobico; può quindi diffondere liberamente nella membrana mitocondriale interna e può agire da ponte tra trasportatori di elettroni meno mobili Trasporta sia elettroni che protoni (importante ruolo nel processo di accoppiamento tra flusso elettronico e movimento protonico)

I componenti della catena respiratoria
9
l’ubichinone (coenzima Q)
Gruppi prostetici dei citocromi di tipo a, b, e c.
Il trasferimento elettronico dal NADH (e dal FADH2) all’O2 coinvolge diversi trasportatori solubili (ubichinone) oppure gruppi prostetici legati a proteine (citocromi e proteine Fe-S)
Centri ferro-zolfo delle proteine ferro-zolfo

I componenti della catena respiratoria
10
Complesso I : NADH-Q ossidoriduttasi, 43 subunità, FMN, 7 centri Fe-S Complesso II: Succinato deidrogenasi (ciclo krebs) 4 subunità, FAD, Fe-S Complesso III: Q- citocromo C ossidoriduttasi, 11 subunità, cit b, cit-c1, Fe-S Complesso IV: Citocromo C ossidasi, 13 subunità, (cit a, cit a3, CuA, CuB)
Proteine integrali di membrana :

11
Complesso I: da NADH a ubichinone NADH:ubichinone ossidoreduttasi o NADH deidrogenasi o NADH-UQ reduttasi Trasferimento di uno ione idruro
da NADH a FMN I due elettroni passano attraverso una serie di centri ferro-zolfo fino all�ubichinone che si riduce QH2 diffonde all�interno del doppio strato lipidico Il trasferimento di elettroni porta anche all�espulsione dalla matrice di protoni (4H+ per ogni coppia di e-) con un meccanismo non ancora noto
Il flusso protonico (pompa protonica) produce un potenziale elettrochimico tra i due lati della membrana che conserva parte dell�energia rilasciata dalle reazioni esoergoniche di trasferimento degli elettroni

12
Complesso II: da succinato a ubichinone Succinato deidrogenasi o succinato-UQ reduttasi
Gli elettroni si muovono dal succinato a FAD, quindi attraversano tre centri Fe-S fino all�ubichinone Il gruppo eme B presente nel complesso non si trova nel percorso diretto degli elettroni Può servire a proteggere dalla formazione di ROS catturando elettroni che �escono� dal sistema muovendosi dal succinato a O2
Struttura del complesso II di E.coli
matrice mitocondriale negli eucarioti

13
Altri substrati di deidrogenasi mitocondriali passano i loro elettroni alla catena respiratoria a livello dell’ubichinone senza passare dai complessi I o II
acil-CoA deidrogenasi (prima tappa della β-ossidazione degli acidi grassi): trasferimento degli elettroni a FAD, ETF (proteina che trasferisce elettroni), ETF:ubichinone ossidoreduttasi, ubichinone glicerolo 3-fosfato deidrogenasi mitocondriale flavoproteina localizzata sulla faccia esterna della membrana mitocondriale interna incanala gli elettroni nella catena respiratoria riducendo direttamente Q.

14
Complesso III: da ubichinone a citocromo c Complesso del citocromo bc1 o ubichinone:citocromo c ossidoreduttasi o ubichinone-citocromo c reduttasi contiene due siti di legame per Q: QP e QN
CICLO DELL�UBICHINONE (CICLO Q) : 1. una prima molecola di QH2 legata a QP cede separatamente un e- al citocromo c e l�altro ad una molecola di Q legato a QN: si forma una molecola di citocromo c ridotto e una molecola di radicale anionico semichinonico. Q neoformato abbandona il complesso. 2. una seconda molecola di QH2 cede un e- al citocromo c e l�altro al radicale: si forma citocromo c e QH2. il secondo trasferimento di e- comporta la captazione di due protoni dalla matrice. Q neoformato abbandona il complesso.
seconda pompa protonica (4 H+ per ogni coppia di e-)

La citocromo C ossidasi (complesso IV)
15
Il complesso IV catalizza la reazione di riduzione dell’O2
Contiene eme a eme a3 e 3 ioni rame che passano ciclicamente da Cu+ a Cu2+
Sono trasportati 4H+ ogni 4 elettroni ceduti ad una molecola di ossigeno
Una dopo l’altra 4 molecole di Citocromo C si legano all’enzima e trasferiscono un elettrone alla volta riducendo una molecola di O2 a H2O
4 cyt cinterm + 8 H+mat + O2 → 4 cyt cox + 2 H2O + 4 H+
interm

16
Il flusso di elettroni e protoni attraverso i quattro complessi della catena respiratoria
acyl-coA dehydrogenase
glycerol 3-phosphate dehydrogenase

Flusso degli elettroni attraverso la catena di trasporto degli elettroni dal NADH all’ossigeno
17 Flusso degli elettroni indicato dalla freccia Blu
I complessi trasportatori di elettroni sono disposti in sequenza ad l’affinità crescente per gli elettroni in modo che fluiscano spontaneamente dall’NADH verso l’ossigeno (ΔE>0, ΔG<0)
(Succinato DH)

L’energia rilasciata durante il trasferimento elettronico è conservata nella formazione di un
gradiente protonico
18
NADH + 11 H+matr + 1/2 O2 = NAD+ + 10 H+
interm + H2O
L’energia contenuta nella differenza di concentrazione protonica e di separazione di carica rappresenta una forma di conservazione dell’energia liberata dal trasferimento elettronico ed è chiamata forza motrice protonica
Spazio intermembrana Matrice
C2 C1

Energia di un gradiente protonico
Quanta energ ia s i r i cava da l la formazione di un gradiente protonico ? (vedi modulo 9 trasporto di membrana) ΔG = 2,303 RT log10 (c2/c1) + ZF ΔV
19
La differenza di pH tra l’esterno e l’interno della membrana mitocondriale è di 1,4 unità, (pH inferiore nello spazio intermembrana) Nelle condizioni del mitocondrio quindi: ΔV = 0,14 V, Z = 1, log10 (c2/c1) = 1,4 ΔG= (2,303 x 8,32 x 10-3 kJ mol-1 K-1 x 310 K x 1,4) + (+1 x 96,48 kJ mol-1 V-1 x 0,14 V) = 21,8 kJ mol-1 Ciascun protone (ione ossonio H3O+) portato dalla matrice verso lo spazio intermembrana richiede 21,8 kJ mol-1 e fornisce 21,8 kJ mol-1 quando rientra nella matrice

Trasporto di elettroni e sintesi di ATP attraverso il meccanismo chemiosmotico.
20
Trasporto degli elettroni Fosforilazione dell’ADP
Molecular biology of the cell, 4th ed. Figure 14-1.
Spazio intermembrana
Matrice mitocondriale
1 Tappa: il trasporto degli elettroni permette di pompare protoni attraverso
la membrana
2 Tappa: il gradiente protonico passa attraverso la ATP sintasi e si forma ATP

L’ATP Sintasi ( F1F0 ATPasi )
21
Il flusso protonico inverte la sua direzione: i protoni tornano alla matrice attraverso un canale protonico.
L’ATP sintasi: è formata da due domini funzionali: una unità di conduzione protonica con aspetto di uno stelo (subunità F0) e da una unità catalitica a forma di sferula (F1).

La struttura della ATP sintasi
22
F1= comp le s so per i fe r i co d i membrana formata da 5 polipeptidi diversi: α3β3 (il sito catalitico dell’ATP sintasi) e dalle proteine γδε. La subunità γ si inserisce nell’esamero α3β3 spezzandone la simmetria. Fo= complesso transmembrana forma il canale protonico (subunità a,b,c10)
L’enzima è dotato di: • una parte mobile (rotore): formata dall’anello c e dello
stelo centrale γε • una parte fissa (statore) comprendente il resto della
molecola (α3β3 e giunzione esterna a b δ)

La catalisi rotazionale è alla base del meccanismo di sintesi dell’ATP
23
ADP3- + HPO42- + H+ ATP4- + H2O
Le tre subunità β a seconda dell’interazione con subunità γ assumono conformazioni diverse per il legame con i nucleotidi adenilici: L, lassa che lega ADP e Pi , chiusa T tesa, che catalizza la formazione di ATP , chiusa O aperta, permette il rilascio del nucleotide
La subunità γ ruotando interconverte le tre forme
https://www.youtube.com/watch?v=PjdPTY1wHdQ
O
T L
O
L
T
O
L
T

Il flusso dei protoni intorno all’anello C determina la sintesi di ATP
24
Il passaggio di H+ tramite F0 determina una rotazione di F0 e della subunità γ rispetto i trimeri αβ di F1.
Subunità c: due α-el iche transmembrana con un residuo di Asp al centro
Subunità a: due semicanali che permettono agli H+ di penetrare nella membrana
Percorso dei protoni all’interno della
membrana Il movimento di H+ attraverso i semicanali della subunità a da una zona di alta concentrazione (intermembrana) ad una a bassa concentrazione di H+ (matrice) fornisce l’energia per la rotazione di C.

L’ossidazione del glucosio rende circa 30 molecole di ATP
25
La stechiometria del pompaggio di H+ e della sintesi di ATP è costituita da numeri non interi. Il trasporto di una coppia di elettroni attraverso NADH e FADH2 genera il pompaggio di circa 10 H+ (4+4+2), il passaggio di circa 4 protoni per ogni ATP formato
Stime indicano che:
NADH = 10H+ trasportati ~ 2.5 ATP
FADH2 = 6H+ trasportati ~ 1.5 ATP
Dalla completa ossidazione di una molecola di glucosio si ottengono 30-32 molecole di ATP.
La differenza (30 o 32) dipende dal sistema di trasferimento dell’NADH prodotto nel citoplasma nel mitocondrio.

Il controllo della fosforilazione ossidativa
26
La velocità di respirazione (consumo di ossigeno) nei mitocondri è controllata dalla disponibilità di ADP quale substrato per la fosforilazione (CONTROLLO DA ACCETTORE)
L’ ATP viene formato solo alla velocità con cui viene consumato. Gli elettroni non fluiscono attraverso la c a t e n a d i t r a s p o r t o d e g l i e l e t t r o n i s e contemporaneamente ADP non viene fosforilato ad ATP. I livelli di ADP influenzano anche la velocità del ciclo dell’acido citrico.
Il rapporto di azione di massa [ATP]/ [ADP][Pi] È molto elevato

27
processo Prodotto formato
Molecole di ATP prodotte
glicolisi 2 NADH(cit) 2 ATP
3 o 5* 2
Ox del piruvato (2 per molecola di glucosio)
2 NADH (mmt) 5
Ox dell’Acetil CoA
6 NADH 2 FADH2 2 ATP o GTP
15 3 2
Resa totale per molecola di glucosio
30 o 32

28
ΔGp= ΔG’° + RT ln [ADP][Pi] /[ATP] dove R= 8,315 J/mole K Sappiamo che ΔG’°= -30,5 kJ/mole Quanto sarà l’energia richiesta per sintetizzare ATP in un neurone?
ΔGp= -30,5 kJ/mole + (8,315 J/mole K x 310 K) ln (0,73 x 10-3) x (2,72 x 10-3)/(2,59 x 10-3) = -30,5 kJ/mole + (2,577 kJ/mole) (-7,166) = -30,5 kJ/mole – 18,467 kJ/mole = -48,96 kJ/mole perciò per la sintesi di ATP saranno necessari 48,96 kJ/mole

29
I livelli intracellulari di ATP: - I meccanismi regolatori mantengono le concentrazioni di ATP ben sopra ai valori di equilibrio per le reazioni di idrolisi - Quando la concentrazione di ATP scende, non solo diminuisce la quantità di combustibile, ma perde anche la sua potenza Al diminuire di [ATP] diminuisce anche ΔGp di idrolisi
Related Documents