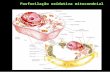
Fosforilação Oxidativa Bioquímica II Ano Lectivo 2010/2011 Trabalho Realizado por: Ana Isabel Martins Ana Luísa Delindro Ana Sofia Ferreira

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

Fosforilação OxidativaBioquímica II
Ano Lectivo 2010/2011
Trabalho Realizado por:Ana Isabel MartinsAna Luísa DelindroAna Sofia Ferreira
Cristina AlvesInês Queirós
Turma P1

Fosforilação Oxidativa – processo enzimático de fosforilação do ADP a ATP, a partir de um gradiente electroquímico de protões.
Ocorre acoplado ao transporte de electrões do NADH ou do FADH2 para o oxigénio molecular (aceitador final), na cadeia de respiração mitocondrial.

O potencial redox dos electrões vai sendo dissipado à medida que estes fluem através das proteínas da cadeia transportadora de electrões.
A dissipação deste gradiente através de um complexo proteico transmembranar permite a síntese de ATP (ATP sintase).
Libertação de energia - é acoplada ao transporte de protões para o espaço intermembranar contra o gradiente de concentração,
Gera-se um gradiente electroquímico de protões.

Estrutura da Mitocôndria
• Membrana externa• Membrana interna• Matriz mitocondrial• Cristas mitocondriais• Espaço intermembranar

Transportadores de electrões
NADFADUbiquinona ou Coenzima QCitocromos Proteínas de Fe-S

NAD
- Transportador de electrões hidrossolúveis;
- Constituído por 2 nucleótidos unidos por 2 grupos fosfato;
- Principal função: transporte de electrões entre as vias catabólicas e o primeiro complexo enzimático da cadeia respiratória, a NADH: ubiquinona oxiredutase (transporta 2 electrões)

FAD
• Cofactor das flavoproteínas.
• Flavina: capaz de transferir 1 ou 2 electrões Estes cofactores (FAD, FMN) são utilizados na transferência de electrões entre doadores de 2 electrões e transportadores de 1 electrão (ex: centros de FE-S e grupos heme)

Ubiquinona ou Coenzima Q
• Natureza lipídica;
Difunde-se livremente no interior da membrana
tornando num transportador móvel de electrões entre os complexos proteicos da cadeia respiratória ( do I e II para o III)
• Aceita 1 ou 2 electrões;

Citocromos
• O Fe é facilmente reduzido ou oxidado, permitindo a transferência de 1 electrão.

Proteínas Fe-S
•O ferro está ligado ao enxofre das cisteínas e a átomos de enxofre inorgânico.
•Estes centros podem doar e receber 1 electrão, oscilando assim entre 2 estados redox

Cadeia Respiratória mitocondrial

• Constituída por 4 complexos proteicos;
• Complexo I: Oxirredutase do NADH:ubiquinona• Complexo II: Desidrogenase do succinato• Complexo III: Oxirredutase da ubiquinona:citocromo c• Complexo IV: Oxidase do citocromo
Passo Final: Sintase do ATPO bombeamento de protões associado ao transporte de electrões é
dissipado, gerando-se ATP
Fosforilação oxidativa

Complexo I• Ocorre a transferência de um ião hidreto e de um protão do NADH ( 2 electrões) para uma ubiquinona- processo exergónico, liberta energia;
• São transferidos 4 protões da matriz mitocondrial para o espaço intermembranar (energia potencial) contra o gradiente de concentração
a energia libertada na reação exergónica é reservada em energia potencial;
Este complexo contribui asssim para a força protomotriz com 4 protões

Complexo II

Complexo II
• Processo de oxidação do succinato a fumarato - gera 2 electrões e 2 protões que reduzem a flavina (FAD)
• Os electrões da flavina reduzida (FADH2) são transferidos posteriormente de uma forma sequencial através dos centros ferro - enxofre até à ubiquinona.
•A ubiquinona reduz-se a ubiquinol.
O complexo II não funciona como bomba de protões e é independente do complexo I.

Complexo II
Hidrólise de triglicerídeos
3-fosfato de glicerol
MúsculoCérebro
3-fosfato de Glicerol
Redução

Complexo III• Cataliza a transferência
exergónica de 2 electrões do ubiquinol para o citocromo c
A energia libertada é utilizada e armazenada através da transferência endergónica de 4 H+ (por cada2 electrões da matriz para o espaço intermembranar).

Complexo IV
Cataliza a transferência exergónica de 2 electrões do citocromo c para o oxigénio molecular (liberta-se H2O)
Transferência endegónica de 2H+ por cada 2 electrões da matriz para o espaço intermembranar

• A citocromo c oxídase liga o oxigénio molecular entre os iões Fe2+ e Cu+ num centro heme (átomo de Fe no centro)
• Evita a libertação de intermediários parcialmente reduzidos (nefastos , originam fenómenos de oxidação das membranas e
proteínas - ex: anião superóxido)

Modelo Quimiosmótico da Síntese de ATP

Sintase do ATPFOF1-ATPase

Complexo FO
Estrutura e acção

Complexo F1
Estrutura e acção


Translocadores de ADP/ATP e Pi
+ 1 H+

REGULAÇÃO da Sintase do ATP IF1

Lançadeira Malato/Aspartato
•Fígado•Rim•Coração

Regulação
• Disponibilidade de ADP:Baixos níveis de ADP fosforilação oxidativa baixa
• Disponibilidade de Oxigénio:Ausência de O2 não ocorre a fosforilação do ADP a
ATP

• Inibição:
Os inibidores da cadeia respiratória actuam ligando-se a 1 ou mais transportadores de electrões e bloqueiam o fluxo electrónico impedindo processos de redução, oxidação ou transporte
(ex: rotenona, cianeto, malonato)

Desacopladores• Tipicamente compostos hidrofóbicos, na membrana interna
da mitocôndria
• Dissipam o gradiente de protões, transportando-os de volta para a matriz.
Dissipação de alguma energia sob a forma de calor
Alguns exemplos: • Termogenina- no tecido adiposo castanho• DCCD- têm propriedades ácido-base, inibem o movimento
dos protões na sintase do ATP (nomeadamente no complexo Fo)

Balanço energético
• Rendimento global da cadeia transportadora de electrões
Se o transporte é feito pela NADH: 4H+ + 4H+ + 2H+ = 10H+
Se o transporte é feito pelo FADH24H+ + 2H+ = 6H+
Related Documents