1 IV. METODE ELECTROCHIMICE DE ANALIZĂ Bibliografie suplimentară: Capitolul de metode electrochimice de analiză din cartea Muntean D.L., Imre S.: Analiza medicamentului – ghid practic, Editura University Press Targu-Mures, 2007 . IV.1. NOŢIUNI GENERALE Metodele electrochimice sunt metode de analiză care au la bază fenomene ce implică ioni şi electroni , fenomenele având loc la nivelul unor electrozi într-o celulă electrochimică. Definiţii: - Electrolitul este o substanţă care prin dizolvare într-un solvent potrivit disociază în ioni, producând o soluţie conducătoare de electricitate. - Un electrod este un conductor electric, prin intermediul căruia curentul electric intră sau iese dintr-un electrolit. Electrodul la nivelul căruia electronii ies din electrolit, producându-se oxidarea (electrolitul cedează electronii pe electrod), se numeşte anod, iar cel la nivelul căruia electronii intră în soluţie, producându-se reducerea (electrolitul acceptă electronii cedaţi de electrod) se numeşte catod. - Celula electrochimică reprezintă un a nsamblu de doi electrozi şi un electrolit (figura 1). a b Figura 1. Tipuri de celule electrochimice a) celulă galvanică – reacţia chimică din interiorul celulei produce curent electric în exterior; b) celulă electrolitică – curentul electric exterior produce o reacţie chimică în celulă (electroliză). http://www. public.asu.edu/~la serweb/woodbury/classes/ chm341/lecture_set1 0/lecture10.html :

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript
-
1
IV. METODE ELECTROCHIMICE DE ANALIZ
Bibliografie suplimentar: Capitolul de metode electrochimice de analiz din cartea Muntean D.L., Imre S.: Analiza medicamentului ghid practic, Editura University Press Targu-Mures, 2007.
IV.1. NOIUNI GENERALE
Metodele electrochimice sunt metode de analiz care au la baz fenomene ce implic ioni i electroni, fenomenele avnd loc la nivelul unor electrozi ntr-o celul electrochimic.
Definiii: - Electrolitul este o substan care prin dizolvare ntr-un solvent potrivit
disociaz n ioni, producnd o soluie conductoare de electricitate. - Un electrod este un conductor electric, prin intermediul cruia curentul
electric intr sau iese dintr-un electrolit. Electrodul la nivelul cruia electronii ies din electrolit, producndu-se oxidarea (electrolitul cedeaz electronii pe electrod), se numete anod, iar cel la nivelul cruia electronii intr n soluie, producndu-se reducerea (electrolitul accept electronii cedai de electrod) se numete catod.
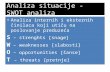
- Celula electrochimic reprezint un ansamblu de doi electrozi i un electrolit (figura 1).
a b
Figura 1. Tipuri de celule electrochimice a) celul galvanic reacia chimic din interiorul celulei produce curent electric n exterior; b) celul electrolitic curentul electric exterior produce o reacie chimic n celul (electroliz). http://www.public.asu.edu/~laserweb/woodbury/classes/chm341/lecture_set10/lecture10.html:
-
2
n timpul proceselor electrochimice, pot avea loc urmtoarele fenomene (Figura 2):
- Transformarea energiei electrice n energie chimic (producerea unei reacii chimice ca urmare a furnizrii de energie electric) sau de transport de ioni;
- Transformarea energiei chimice n energie electric (producerea curentului electric n urma unei reacii chimice, ex. funcionarea bateriilor electrice).
Energie electric Reacie redox
Figura 2. Interconversia de energie n cadrul metodelor electrochimice de analiz
Reaciile chimice implicate n procesele electrochimice se numesc reacii
redox. Reacia redox este reacia n care un reactant se oxideaz concomitent cu reducerea celuilalt reactant (Figura 2):
- oxidare - pierdere de electroni ceea ce duce la o cretere a strii de oxidare; exemplu: Fe0 2e- Fe2+
- reducere acceptare de electroni ceea ce duce la o scdere a strii de oxidare; exemplu: Fe2+ + 2e- Fe0
Clasificarea metodelor electrochimice: 1) Metode electrochimice la curent 0 sau fr curent net:
a) Poteniometria se msoar tensiunea dintre doi electrozi n funcie de concentraia speciilor ionice prezente n soluie;
b) Conductometria se msoar capacitatea de conducere a curentului electric de ctre ionii soluiei de analizat.
2) Metode electrochimice la curent finit: a) Coulometria se msoar cantitatea de curent consumat sau produs n
urma unei reacii chimice redox; de exemplu, electroliza; b) Voltamperometria se msoar cantitate de curent produs de o reacie
chimic redox la diferite tensiuni de curent aplicate (tensiunea = diferena de potenial); de exemplu, polarografia.
-
3
IV.2. POTENIOMETRIA
Poteniometria este o metod electrochimic de analiz prin care cantitatea de substan (electrolit) dintr-o soluie se msoar innd cont de diferena de potenial pe care o produce ntre doi electrozi, un electrod indicator i un electrod de referin:
- Electrodul indicator electrod al crui potenial electric se schimb n funcie de concentraia unei anumite specii ionice din soluia n care este introdus; exemplu: electrodul de sticl indicator de pH (ioni de H+), electrodul indicator de ioni de Ca2+, oxigen, clor Cl-;
- Electrodul de referin electrod cu un potenial electric constant i cunoscut; exemplu, electrodul de Ag/AgCl, electrodul de calomel Hg/Hg2Cl2, electrodul de hidrogen.
Cea mai des ntlnit tehnic poteniometric este pH-metria msurarea pH-ului, iar aparatul cu care se msoar pH-ul se numete pH-metru ale crui componente principale sunt prezentate n figura 3.
Figura 3. pHmetru (http://www.made-in-china.com/showroom/bkinstrument/product-
detaillqembzAOgQUM/China-Laboratory-PH-Meter.html)
Electrod combinat de pH
Senzor de temperatur
Punte de msur electronic
-
4
a) b)
Figura 4. Electrod de sticl: a) schema de ansamblu http://www.ktf-split.hr/glossary/en_o.php?def=glass%20electrode; b) detaliu http://www.flickr.com/photos/mitopencourseware/3215171485/
Componenta central a unui pH-metru o reprezint electrodul de sticl (Figura 4) format dintr-o membran de sticl, de regul sub forma unui bulb, i un electrod de referin intern (un fir de Ag pe care este depus AgCl) imersat ntr-o soluie intern cu concentraia constant de ioni H+. Electrodul combinat de pH conine n acelai bloc electrodul de sticl i electrodul de referin extern care este, de regul, electrodul de Ag/AgCl. La introducerea electrodului n soluia de cercetat, membrana de sticl se umecteaz, iar ionii H+ din soluia de cercetat ptrund n membran, deplasnd ionii de Na+ (membrana de sticl este format din SiO2, Na2O, CaO etc.). n urma acestui schimb de ioni, potenialul de la interfaa membran soluie se modific. Puntea electronic msoar diferena de potenial dintre electrodul de referin i electrodul de sticl i o traduce direct n uniti de pH (reamintim faptul c pH = -log [H+]). Diferena de potenial dintre electrozii pH-metrului i, implicit, pH-ul depind de temperatur i de aceea pHmetrele au ncorporate un senzor de temperatur, n acest fel puntea electronic de msur poate s corecteze valoarea pH-ului la cea corespunztoare unei temperaturi de referin de 25 C.
Efectuarea msurtorii de pH presupune parcurgerea mai multor etape: - conectarea aparatului la reeaua electric i pornirea acestuia; - verificarea instalrii electrodului de pH i a compensatorului de
temperatur (n cazul electrozilor noi, acetia trebuie meninui cel
-
5
puin 8 ore ntr-o soluie tampon cu pH 7); cele dou dispozitive trebuie imersate mpreun n soluia de analizat;
- calibrarea pH-metrului - se poate face ntr-un punct, dou sau trei puncte, n funcie de domeniul de pH pe care se lucreaz, cu ajutorul unor soluii tampon cu pH bine definit; indiferent de numrul de puncte de calibrare care vor fi realizate, se ncepe ntotdeauna cu soluia tampon cu pH 7;
- electrodul i compensatorul de temperatur trebuie cltii cu ap distilat dup scoaterea din soluia prob i apoi cu soluia ce urmeaz a fi msurat;
- msurarea pH-ului probei; - la ncheierea msurtorilor, electrodul i compensatorul de
temperatur trebuie cltii cu ap distilat i uscai cu ajutorul unei hrtii de filtru; electrodul se pstreaz ntr-o soluie soluie tampon cu pH 7 sau soluie saturat de KCl 2-3 M;
- oprirea i deconectarea aparatului. Pentru msurarea concentraiei altor specii dintr-o soluie prob se utilizeaz echipamente similare, avnd electrozi indicatori specifici.
-
6
IV.3. CONDUCTOMETRIA Conductometria reunete metodele electroanalitice care se bazeaz pe determinarea capacitii unor soluii de electrolii de a conduce curentul electric (conductibilitate electric). Conductibilitatea electric a corpurilor este legat de deplasarea sarcinilor electrice sub aciunea unei diferene de potenial. n cazul conductorilor metalici se deplaseaz electronii, iar n soluie de electrolii sau topituri, cauza conductibilitii electrice o reprezint deplasarea ionilor. Aparatul cu care se msoar capacitatea de conducere a curentului electric se numete conductometru ale crui componente principale sunt prezentate n figura 5.
a)
b) Figura 5. Conductometru: a) schema de principiu; b) model comercial
Punte de msur
Electrod
-
7
Celula conductometric este format din electrozi de platin ntre care se msoar conductana ionilor soluiei.
n conductometrie se lucreaz cu urmtoarele noiuni: Conductibilitatea electric sau conductana, q proprietatea unui corp de
a conduce curentul electric (se msoar n Siemens, S, sau ohm-1, -1) Rezistena electric, R inversul conductanei electrice (1 = rezistena
unui conductor care permite trecerea unui curent de 1 A sub diferena de potenial de 1 V):
S
lR =
R
1q =
unde - rezistivitate (depinde de natura conductorului), [.cm-1], l lungimea conductorului, [cm], S seciunea conductorului [cm2]. Mrimile l i S sunt caracteristicile geometrice ale conductorului electric.
Conductibilitatea specific (conductivitate), , reprezint conductibilitatea unui conductor de 1 cm lungime i 1 cm2 seciune, [ Scm-1]:
1 =
innd cont de definiiile anterioare:
l
Sq =
Dup cum se observ, q depinde de geometria conductorului, iar nu. Factori care influeneaz conductibilitatea specific: - natura probei (mobilitatea i valena ionilor, vscozitatea solventului); - concentraia ionilor; - temperatura; - presiunea; - frecvena curentului conductometrului. Conductometrele moderne msoar direct . Efectuarea msurtorii de
conductivitate presupune parcurgerea mai multor etape: - conectarea aparatului la reeaua electric i pornirea acestuia; - verificarea instalrii electrodului de conductivitate; - electrodul trebuie cltit cu ap distilat din abunden i apoi cu soluia
ce urmeaz a fi msurat; - msurarea probei; - la ncheierea msurtorilor, electrodul trebuie cltit cu ap distilat i
uscat cu ajutorul unei hrtii de filtru; electrodul se pstreaz ca atare sau n ap distilat;
- oprirea i deconectarea aparatului.
-
8
IV.4. ELECTROFOREZA CAPILAR
Principiu
Electroforeza este o metod de analiz care presupune separarea compuilor unei probe i se bazeaz pe migrarea speciilor purttoare de sarcini electrice globale din proba aflat n soluie sub efectul unui cmp electric printr-un suport corespunztor. Electroforeza capilar corespunde unei adaptri particulare a metodei generale de electroforez.
n tehnica clasic de electroforez, larg utilizat n domeniul bioanalitic, se utilizeaz benzi din material plastic acoperite cu o substan poroas impregnat cu un electrolit (Figura 6). Capetele sunt imersate n dou rezervoare independente, coninnd acelai electrolit i cuplate la electrozii unui generator de tensiune continu.
Proba este depus sub forma unui strat subire transversal pe band, eventual presat ntre dou plci izolante. Speciile hidratate prezente migreaz ntr-un timp variabil cuprins ntre cteva secunde pn la cteva ore spre una din extremitile benzii. Fiecare compus se difereniaz prin mobilitatea sa, dar absena unui front de solvent msurabil ne oblig s utilizm un standard intern. Detecia speciilor prezente dup migrare se efectueaz n general prin transferul acestora printr-un procedeu prin contact pe o membran unde sunt revelate cu ajutorul unor reactivi specifici obinndu-se electroforegrama.
Figura 6. Electroforeza de zon: principiul unei instalaii (sus) i electroforegrama (jos)
n electroforeza capilar (figura 7) suportul plan din tehnica clasic este
nlocuit de un tub capilar deschis la ambele capete, din sticl de siliciu cu
-
9
diametrul variind ntre 15 i 150 m. Acest capilar cu lungimea L = 20-80 cm este umplut cu un electrolit tampon.
Diferena de potenial aplicat la capetele capilarului poate atinge 600 V/cm, dar intensitatea curentului nu poate depi 100 A astfel c puterea disipat rmne inferioar valorii de 3 W. Pentru evitarea nclzirii capilarului este preferabil plasarea lui ntr-un recipient termostatat.
Figura 7. Schema unei instalaii de electroforez capilar
Figura 8. Electroforegram
Semnalul obinut de la un detector plasat la distana l de extremitatea
superioar a capilarului, n apropierea catodului, st la baza obinerii electroforegramei (Figura 8) care conine informaiile despre compoziia probei cercetate. Sunt detectate numai speciile care se orienteaz spre catod. Moduri de detecie utilizate:
a) Detecia UV / VIS se msoar intensitatea luminii care traverseaz capilarul ntr-o zon unde acoperirea total a fost eliminat, utiliznd o lungime de und 200 -230 nm. Msurtorile sunt dificile datorit matricelor care sunt n general absorbante. Pentru ionii anorganici care absorb puin se alege un electrolit care conine cromat sau ftalat ce determin creterea absorbanei. n aceste condiii cnd un ion din prob ajunge la
-
10
nivelul detectorului se produce o diminuare a absorbiei, obinndu-se picuri negative (detecie invers).
b) Detecia prin fluorescen este foarte sensibil i utilizeaz o surs laser foarte intens, fiind adesea asociat cu un procedeu de pre- sau post-derivare a analiilor pentru a deveni fluoresceni.
c) Cuplarea cu un spectrometru de mas este un procedeu de detecie larg utilizat. Debitul slab din capilar permite ionizarea la presiune atmosferic ceea ce face posibil studiul componenilor biologici.
d) Detectare electrochimic const n introducerea unor microelectrozi n capilar. Se poate lucra poteniometric sau conductometric. Electroforegrama este similar cromatogramei din tehnica HPLC, iar
interpretarea ei se face identic (vezi capitolul V de curs). Electroforegrama este format dintr-o sum de picuri electroforetice, fiecare pic corespunznd unui singur compus, iar aria lui este direct proporional cu concentraia.
Related Documents