24‐11‐2015 1 CORROSÃO E PROTEÇÃO DE METAIS Química 12 – Marília Peres (adaptado de Texto Editores) Os metais podem sofrer corrosão. A corrosão de metais corresponde a oxidação (indesejável) associada simultaneamente a uma redução Corrosão 2 (indesejável), associada, simultaneamente, a uma redução. Quando uma gota de água entra em contacto com um pedaço de ferro, que reacções ocorrem? Que fatores favorecem a corrosão dos metais? Todos os metais possuem igual propensão para se oxidarem? Todos os metais possuem igual propensão para se oxidarem? Como proteger um metal da corrosão? Poderá a oxidação de um metal ser útil?

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

24‐11‐2015
1
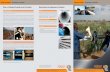
CORROSÃO E PROTEÇÃO DE METAIS
Química 12 – Marília Peres (adaptado de Texto Editores)
Os metais podem sofrer corrosão. A corrosão de metais corresponde a oxidação (indesejável) associada simultaneamente a uma redução
Corrosão2
(indesejável), associada, simultaneamente, a uma redução.
Quando uma gota de água entra em contacto com um pedaço de ferro, que reacções ocorrem?
Que fatores favorecem a corrosão dos metais?
Todos os metais possuem igual propensão para se oxidarem? Todos os metais possuem igual propensão para se oxidarem?
Como proteger um metal da corrosão?
Poderá a oxidação de um metal ser útil?

24‐11‐2015
2
OXIDAÇÃO DO FERROQuando uma gota de água entra em contacto com um pedaço de
3
Corrosão
Quando uma gota de água entra em contacto com um pedaço de ferro, ocorrem várias reacções.
4
Corrosão / Oxidação do Ferro
O que se passa? Onde? Designação
O ferro é oxidado a ferro (II)Fe (s) Fe2+ (aq) + 2e-
e passa para a solução (gota de água)
O oxigénio é reduzido2e- + ½ O2 (aq) + H2O (l) 2OH- (aq)e passa para a solução (gota de água)
Forma-se Fe(OH)2: Fe2+ + 2OH- Fe(OH)2 com subsequente formação de Fe2O3xH2O Fe(OH)2xH2O (ferrugem)
O2 (aq)
Na superfície do metal
Sobretudo à superfícieda gota e junto
ao metal
No interior da gota
Semi-reacçãode oxidação
Semi-reacçãode redução

24‐11‐2015
3
Corrosão5
Adaptado de Rosa Pais
Que fatores favorecem a corrosão do ferro?
6
Corrosão
1. Meio ácido
2. SO2
3. Iões
M i á id
1. 2e- + ½ O2 (aq) + H2O (l) 2OH- (aq)
Meio ácido
2. Formação de Sulfuretos
3. A existência de iões favorece a condutibilidade, logo as reações redox.
Fonte: Texto Editores

24‐11‐2015
4
7
Proteção dos Metais contra a Corrosão
8
Proteção dos Metais contra a Corrosão
COMO COMBATER A CORROSÃO:
1- Aplicar uma camada protetora , como a pintura ou plastificação ;
2- Provocar a formação de um filme protetor de óxidos ( anodização ) ;
3- Recobrir o metal com uma fina camada de outro metal (galvanoplastia);
4 P ã ódi4- Proteção catódica .

24‐11‐2015
5
9
Proteção dos Metais contra a Corrosão
10
Proteção dos Metais contra a Corrosão

24‐11‐2015
6
11
Proteção dos Metais contra a Corrosão
ANODIZAÇÃO DO ALUMÍNIO:
Esquema de anodização(fonte: Santillana)
12
Proteção dos Metais contra a Corrosão
Adaptado de Rosa Pais

24‐11‐2015
7
13
Proteção dos Metais contra a Corrosão
GALVANOPLASTIA
14
Proteção dos Metais contra a Corrosão
Fonte: Rosa Pais

24‐11‐2015
8
15
Proteção dos Metais contra a Corrosão
16
Proteção dos Metais contra a Corrosão
4 4 –– PROTEÇÃO CATÓDICAPROTEÇÃO CATÓDICA

24‐11‐2015
9
17
Proteção dos Metais contra a Corrosão
18
Proteção dos Metais contra a Corrosão

24‐11‐2015
10
Reciclagem de Metais19
Fonte: http://www.dreamstime.com/
Related Documents