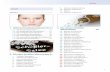
Anhang A: Zeichnungen von Laborgeräten Uhrglas Bechergläser mit Graduierung in breiter und hoher Form Reagenzglas Kochbecher für z. B. den Sodaauszug Halbmikrorührstab 1 1,5 2 Zentrifugenglas © Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018 M. Herbig und J. Wagler, Qualitative Anorganische Analyse, https://doi.org/10.1007/978-3-662-57850-6 125

Welcome message from author
This document is posted to help you gain knowledge. Please leave a comment to let me know what you think about it! Share it to your friends and learn new things together.
Transcript

AnhangA: ZeichnungenvonLaborgeräten
Uhrglas
Bechergläser mit Graduierung
in breiter und hoher Form
ReagenzglasKochbecher für
z. B. den
Sodaauszug
Halbmikrorührstab
1
1,5
2
Zentrifugenglas
© Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018M. Herbig und J. Wagler, Qualitative Anorganische Analyse,https://doi.org/10.1007/978-3-662-57850-6
125

126 Anhang A: Zeichnungen von Laborgeräten
Mörser mit PistillPorzellanschale mit
rundem Boden Abdampfschale
Reagenzienflasche mit
Schliff oder mit
Schraubverschluss
Tondreieck
Tropfer (Pasteur-Pipetten), = Glasröhrchen mit kurz- und langausgezogener
Spitze (ersteres mit einem Gummisauger abgebildet). Letzteres kann, ohne
Gummisauger, als Gaseinleitungsröhrchen dienen
Reagenzglashalter aus Holz (oben) und Metall (unten)
Tiegelzange aus Metall

Anhang A: Zeichnungen von Laborgeräten 127
Spatel (oben) und Löffelspatel (unten)
Objektträger mit Probe und Deckgläschen Glasring, der für die
Mikrogaskammer
benötigt wird
Porzellantiegel mit
DeckelNickeltiegel mit Deckel
Bleitiegel mit Deckel
Bunsenbrenner mit
teilweise geöffneter
Luftzufuhr
Teclubrenner mit
teilweise geöffneter
Luftzufuhr Kipp’scher Gasentwickler

128 Anhang A: Zeichnungen von Laborgeräten
Wasserbadeinsatz mit Stellplätzen für
Kochbecher und
Halbmikroreagenzgläser Spritzflasche
Tüpfelplatte mit unterschiedlich großen Vertiefungen
Dreifuß Vierfuß Ionenaustauscherrohr
mit Halterung

AnhangB: Reagenzienanhang
Inhaltsverzeichnis
B.1 Säuren . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 129B.2 Laugen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 130B.3 Organische Lösungsmittel . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 130B.4 Anorganische Reagenzlösungen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 130B.5 Organische Reagenzlösungen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 133
Die erwähnten Reagenzien haben folgende Konzentrationen bzw. Gehalte.
B.1 Säuren
Essigsäure (H3CCOOH)2N verd. 120ml 96 – 100%ige H3CCOOH auf 1 l verdünnen96% konz. auch 100% möglich
Perchlorsäure (HClO4)30% 43ml konz. HClO4 mit Wasser auf 100ml verdünnen70% konz.
Phosphorsäure (H3PO4)85% konz.
Salpetersäure (HNO3)2N verd. 140ml 65%ige HNO3 auf 1 l verdünnen65% konz.
Salzsäure (HCl)2N verd. 165ml 35%ige HCl auf 1 l verdünnen35% konz.
Schwefelsäure (H2SO4)2N verd. 56ml 96%ige H2SO4 auf 1 l verdünnen96% konz.
© Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018M. Herbig und J. Wagler, Qualitative Anorganische Analyse,https://doi.org/10.1007/978-3-662-57850-6
129

130 Anhang B: Reagenzienanhang
B.2 Laugen
Ammoniak (NH3)2N verd. 150ml 25%ige NH3-Lösung auf 1 l verdünnen25% konz.
Kalilauge (KOH)2N verd. 11,2g KOH in 100ml Wasser lösen
Natronlauge (NaOH)2N verd. 80g NaOH in 1 l Wasser lösen40% konz. 65g in 100ml Wasser lösen
B.3 Organische Lösungsmittel
• Diethylether • Methanol• Glycerol (Glycerin) • Pentanol (Amylalkohol)• Ethanol • Trichlormethan (Chloroform)
B.4 Anorganische Reagenzlösungen
Einige Lösungen müssen stets frisch bereitet werden und sind nicht lagerfähig. Fol-gende Lösungen können einige Zeit gelagert werden. Gesättigte Lösungen müssenzum Lösen ggf. erwärmt und nach der Herstellung kalt filtriert werden. Die Gehalts-und Konzentrationsangaben sind ungefähre Angaben.
Ammoniumcarbonat ((NH4)2CO3)
ges. 32g in 100ml Wasser lösen
Ammoniummolybdat ((NH4)2MoO4)
0,25M 5g (NH4)6Mo7O24 · 4H2O in 100ml Wasser lösen und in 35ml 6,5N HNO3
eingießen
Ammoniumoxalat ((NH4)2C2O4)
ges. 22g (NH4)2C2O4 · H2O in 500ml Wasser lösen
Ammoniumpolysul f id ((NH4)2Sx )var. 150ml konz. NH3 in der Kälte mit H2S sättigen und mit 250ml konz. NH3 ver-
dünnen; darin 10g Schwefel lösen und mit Wasser auf 1 l verdünnen
Ammoniumsul f id((NH4)2S)
var. 200ml konz. NH3 in der Kälte mit H2S sättigen und mit 200ml konz. NH3 ver-dünnen; anschließend auf 1 l mit Wasser auffüllen
Ammonium-tetrathiocyanatomercurat (I I ) ((NH4)2 [Hg(SCN )4])1M 30g HgCl2 und 33g NH4SCN in 100ml H2O lösen und ggf. filtrieren
Ammoniumthiocyanat (NH4SCN )
10% 10g NH4SCN in 90ml Wasser lösen

Anhang B: Reagenzienanhang 131
Bariumchlorid (BaCl2)5% 5,8g BaCl2 · 2H2O in 95ml Wasser lösen
Bariumhydroxid (Ba(OH)2)
ges. 36g Ba(OH)2 · 8H2O in 500ml Wasser lösen
Bleiacetat (Pb(OOCCH3)2)
10%ig 11,66g Pb(OOCCH3)2 · 3H2O in 90ml Wasser lösenBromwasser
ges. 3,5g Br2 auf 1 l Wasser verdünnen
Calciumchlorid (CaCl2)5M 55,5g CaCl2 (wasserfrei) in 100ml Wasser lösen
Calciumsul f at (CaSO4)
ges. 2g CaSO4 cot 2H2O in 1 l Wasser lösen
Chlorwasservar. Wasser mit Cl2-Gas sättigen (nicht sehr lange haltbar)
Cobalt (I I )-chlorid (CoCl2)0,1mM 0,125g CoCl2 · 6H2O in 500ml Wasser lösen
Cobalt (I I )-nitrat (Co(NO3)2)
verd. ca. 0,1g Co(NO3)2 · 6H2O in 100ml Wasser lösen
Kup f er(I I )-sul f at (CuSO4)
4mM 0,1g CuSO4 · 5H2O in 100ml Wasser lösen
Eisen(I I I )-chlorid (FeCl3)0,3M 9g FeCl3 · 6H2O in 1ml konz. HCl lösen und auf 100ml mit Wasser auffüllen
I od-Kaliumiodid („K I3)“3,2g I2 in einer Lösung von 25g KI in 250ml Wasser lösen
Kaliumchromat (K2CrO4)
10% 10g K2CrO4 in 90ml Wasser lösen
Kaliumcyanid (KCN )
1M 1,6g KCN in 25ml Wasser lösen
Kaliumhexacyanof errat (I I ) (K4 [Fe(CN )6)])0,1M 21,1g K4[Fe(CN)6] · 3H2O in 500ml Wasser lösen
Kaliumhexacyanof errat (I I I ) (K3 [Fe(CN )6)])0,1M 16,45g K3[Fe(CN)6] in 500ml Wasser lösen
Kaliumiodid (KI )0,5M 41,5g KI in 500ml Wasser lösen
Kaliumpermanganat (KMnO4)
0,025M 1g KMnO4 in 250ml Wasser lösen
Kaliumthiocyanat (KSCN)1M 9,7g KSCN in 100ml Wasser lösen
Kup f er(I I )-sul f at (CuSO4)
4mM 0,1g CuSO4 · 5H2O in 100ml Wasser lösen

132 Anhang B: Reagenzienanhang
Magnesia-Mixtur100g MgCl2 · 6H2O mit 100g NH4Cl in 500ml H2O lösen und mit 50ml konz.NH3 versetzen; auf 1 l mit Wasser auffüllen
Magnesium-Uranylacetat (Mg(OOCCH3)2 · (UO2)(OOCCH3)2)
var. a) 10g (UO2)(OOCCH3)2 · 2H2O in 100ml Wasser und 6ml konz. Essigsäurelösenb) 33g Mg(OOCCH3)2 in 100ml Wasser und 10ml konz. Essigsäure lösena und b mischen und ggf. nach 24 h filtrieren, Lösung nicht zu lange haltbar
Mangan(I I )-sul f at (MnSO4)
0,02M 4,5g MnSO4 · 4H2O in 2N H2SO4 auf 1 l lösen
Natriumacetat (NaOOCCH3)
2M 27,2g NaOOCCH3 · 3H2O in 100ml Wasser lösen
Natriumcarbonat (Na2CO3)
ges. 21,2g wasserfreies Na2CO3 in 100ml Wasser lösen oder 57,2g Na2CO3 · 10H2Overwenden
Natrium f luorid (NaF)
0,1M 0,42g NaF in 100ml Wasser lösen
Natriumthiosul f at (Na2S2O3)
1M 24,8g Na2S2O3 · 5H2O in 100ml Wasser lösen
NeßlersReagenz (K2HgI4)var. käuflich erwerben (enthält KOH)
Quecksilber(I I )-chlorid (HgCl2)0,1M 2,7g HgCl2 in 100ml Wasser lösen
Quecksilber(I I )-nitrat (Hg(NO3)2)
0,5M 16,3g Hg(NO3)2 in 100ml 0,5M HNO3 lösen
Silberni trat (AgNO3)
5% 53g AgNO3 in 1 l Wasser lösen
Strontiumnitrat (Sr(NO3)2)
ges. 66g Sr(NO3)2 in 100ml Wasser lösen
Strontiumsul f at (Sr SO4)
ges. 0,11g SrSO4 in 1 l Wasser lösen
Wassersto f f peroxid (H2O2)
verd. 3% = 9ml konz. H2O2 mit 81ml Wasser verdünnenkonz. 30%
Zink(I I )-nitrat (Zn(NO3)2)
ges. 180g Zn(NO3)2 · 6H2O in 100ml Wasser lösen
Zink(I I )-sul f at (ZnSO4)
0,1M 2,9g ZnSO4 · 7H2O in 100ml Wasser lösen
Zinn(I I )-chlorid (SnCl2)0,25M 5,65gSnCl2 ·2H2O in 20ml konz.HCl lösen und auf 100mlmitWasser verdünnen.
Zur Lagerung eine Zinn-Granalie zugeben.

Anhang B: Reagenzienanhang 133
B.5 Organische Reagenzlösungen
Ali zarin S1% 1g Alizarin S in 99ml Wasser lösen
α-Naphthylamin0,3% 0,4g α-Naphthylamin in 125ml 30%iger Essigsäure lösen
Bromthymolblau0,6mM 0,4g Bromthymolblau in 1 l Wasser lösen
Diacetyldioxim (DADO)
1% 5g DADO in 500ml Ethanol lösen
essigsaure Sul f anilsaure0,02M 0,5g Sulfanilsäure in 150ml 10%iger Essigsäure lösen
Methylviolett5mM 2g Kristallviolett in 1 l Wasser lösen
Morin1,25% 1g Morin in 100ml Methanol lösen
Natrium-5-sul f osalicylat0,25M 6,5g Natrium-5-sulfosalicylat in 100ml Wasser lösen
Rhodamin B0,01% 0,01g Rhodamin B mit 2g KCl in 100ml 2N HCl lösen
Thioacetamid1M 15g Thioacetamid in 200ml Wasser lösen (nicht allzu lange haltbar)
T itangelb0,05% 0,05g Titangelb in 100ml Wasser lösen

AnhangC: TheoretischeEmissionsspektren
Inhaltsverzeichnis
C.1 Der physikalische Farbkreis . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 135C.2 Intensivste Linien ohne Berücksichtigung der relativen Intensitäten . . . . . . . . . . . . . . . . 136C.3 Intensivste Linien mit Berücksichtigung der relativen Intensitäten . . . . . . . . . . . . . . . . . . 137
C.1 Der physikalische Farbkreis
© Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018M. Herbig und J. Wagler, Qualitative Anorganische Analyse,https://doi.org/10.1007/978-3-662-57850-6
135

136 Anhang C: Theoretische Emissionsspektren
C.2 Intensivste Linien ohne Berücksichtigung der relativenIntensitäten [6]

Anhang C: Theoretische Emissionsspektren 137
C.3 Intensivste Linienmit Berücksichtigung der relativenIntensitäten [6]

AnhangD: Kristallbilder
Blei(II)-iodid
nicht aus Blei(II)-acetat herstellen, sonst ändert sich die Kristallform deutlich
Blei(II)-nitrat-Thioharnstoff
nicht aus Blei(II)-acetat herstellen, sonst ändert sich die Kristallform deutlich
© Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018M. Herbig und J. Wagler, Qualitative Anorganische Analyse,https://doi.org/10.1007/978-3-662-57850-6
139

140 Anhang D: Kristallbilder
Cadmium-Harnstoff-Reineckat
Kupfer(II)-tetrathiocyanatomercurat(II)
hochkonzentrierte Lösung
Zink(II)-tetrathiocyanatomercurat(II)
hochkonzentrierte Lösung
Cobalt(II)-tetrathiocyanatomercurat(II)

Anhang D: Kristallbilder 141
Strontiumchromat
Calciumsulfat-dihydrat
Ammoniummagnesiumphosphat-hexahydrat
hochkonzentrierte Lösung
Kaliumperchlorat
umkristallisiert im Wasserbad

142 Anhang D: Kristallbilder
Natriummagnesiumuranylacetat-nonahydrat
Die dreieckigen Kristalle sind Natriumuranylacetat.

Literatur
1. Ackermann, G. (1966). Einführung in die qualitative anorganische Halbmikroanalyse (4., über-arb. Aufl., S. 170). Leipzig: Dt. Verl. für Grundstoffind.
2. Schweda, E. (2016). Package: Jander/Blasius, Anorganische Chemie 1+2 (Bd. 2 18., völlig neubearb. Aufl., S. 577 X). Stuttgart: Hirzel S. Verlag.
3. Gerdes, E. (2001). Qualitative anorganische Analyse : ein Begleiter für Theorie und Praxis (2.,korr. und überarb. Aufl. 1998, Nachdr.). Berlin: Springer.
4. Autorenkollektiv, Standard elektrode Potential. https://en.wikipedia.org/wiki/Standard_electrode_potential_(data_page).
5. Jagner, S., Ljungström, E., & Tullberg, A. (1980). The structure of sodium pentacyanosulphito-ferrate(II) 10.5-water. Acta Crystallographica Section B Structural Crystallography and CrystalChemistry, 36, 2213–2217.
6. Kramida, A., Ralchenko, Y., Reader, J., & NIST ASD Team, NIST Atomic Spectra Database(ver. 5.5.2) [2018, January 11]. Gaithersburg: National Institute of Standards and Technology.
© Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018M. Herbig und J. Wagler, Qualitative Anorganische Analyse,https://doi.org/10.1007/978-3-662-57850-6
143

Sachverzeichnis
AAbdampfschale, 21, 31Aluminiumals Nachweisreagenz, 80Nachweise, 93Vorprobe, 47
Ammoniakgruppe, 90Ammoniumals Nachweisreagenz, 68, 75, 108Nachweise, 107
Ammoniumcarbonatgruppe, 100Arbeitsschema, 102
Ammoniumsulfidgruppe, 96Arbeitsschema, 97
Anionen, 51Gruppenreaktionen, 51Nachweise, 56
AntimonNachweise, 81Vorprobe, 46
ArsenNachweise, 79Vorprobe, 46
Arsengruppe, 77Aufschluss, 34basischer, 35Freiberger, 35Oxidationsschmelze, 36saurer, 34Silberhalogenide, 36
BBariumals Fällungsmittel, 53als Nachweisreagenz, 64, 65, 69, 71Nachweise, 104Vorprobe, 43
Becherglas, 22Bismut (Nachweise), 88Bleials Nachweisreagenz, 62Nachweise, 74
Bleitiegel, 24Borat (Nachweis), 71Boraxperle, 44Brenner, 24Verwendung, 31
Bromat (Nachweis), 60BromidNachweis, 58Vorprobe, 45
CCadmiumNachweise, 86Vorprobe, 49
Calciumals Fällungsmittel, 52als Nachweisreagenz, 103Nachweise, 101Vorprobe, 43
Carbonat (Nachweis), 69Chlorat (Nachweis), 60
© Springer-Verlag GmbH Deutschland, ein Teil von Springer Nature 2018M. Herbig und J. Wagler, Qualitative Anorganische Analyse,https://doi.org/10.1007/978-3-662-57850-6
145

146 Sachverzeichnis
Chlorid (Nachweis), 57Chromals Nachweisreagenz, 74, 103, 104Nachweise, 95Vorprobe, 44, 48
Cobaltals Nachweisreagenz, 107Nachweise, 99Vorprobe, 44, 47
DDeckgläschen, 22Drei- oder Vierfuß, 24
EEisenals Nachweisreagenz, 56, 58, 63, 67, 72Nachweise, 91Vorprobe, 44
Entnahme von Feststoffen, 27Erhitzen, 31
FFällung, 29, 32Kristalle, 29
Filtration, 32Flammenfärbung, 43Fluoridals Nachweisreagenz, 93Nachweis, 56
GGasnachweisdurch Verbrennen, 38mit Mikrogaskammer, 38
Gruppe, lösliche, 105
HHalbmikrorührstab, 22Handspektroskop, 25Heiz- und Rührwerk, 25Hexacyanidoferrat(II)als Nachweisreagenz, 85, 91, 96Nachweis, 72
Hexacyanidoferrat(III)als Nachweisreagenz, 91, 98Nachweis, 72
Hexafluoridosilicat, 71
IIodat (Nachweis), 60
Iodidals Nachweisreagenz, 53, 74, 84, 88Nachweis, 58Vorprobe, 45
Ionenaustauscherrohr, 22
KKaliumals Nachweisreagenz, 61Nachweise, 106Vorprobe, 43
Kipp’scher Gasentwickler, 22Verwendung, 37
Kochbecher, 22Kupferals Nachweisreagenz, 59Nachweise, 85Vorprobe, 43, 44
Kupfergruppe, 78
LLösung (Arbeiten mit), 28
MMagnesiastäbchen und -rinnen, 25Magnesiumals Nachweisreagenz, 68, 106Nachweise, 108
Manganals Nachweisreagenz, 53, 60, 64, 65Nachweise, 98Vorprobe, 44, 48
Mikrogaskammer, 22Abbildung, 39Verwendung, 38
Mikroskop, 25Verwendung, 29
Mörser, 23Verwendung, 27
NNatriumNachweise, 106Vorprobe, 43
Natriumnitroprussid als Nachweisreagenz,62, 65
NickelNachweise, 100Vorprobe, 44
Nickeltiegel, 24Nitrat

Sachverzeichnis 147
Nachweis, 66Vorprobe, 45
Nitrit (Nachweis), 66
OObjektträger, 22
PPerchloratals Nachweisreagenz, 106Nachweis, 61
pH-Wert, 29Phosphatals Nachweisreagenz, 108Nachweis, 68
Pinzette, 25Porzellanschale, 23Porzellantiegel, 23
QQuecksilberals Nachweisreagenz, 83, 86, 98, 100, 107Quecksilber(I)-Nachweise, 75Quecksilber(II)-Nachweise, 84Vorprobe, 50
RReagenzglas, 23Reagenzglasgestell, 25Reagenzglashalter, 25Reagenzienflaschen, 23Reinecke-Salz, 84, 85, 87Reinheit (Feststoffe), 28
SSalzsäuregruppe, 73Arbeitsschema, 73
SchwefelwasserstoffgruppeArbeitsschema, 77, 78
Siedestein, 25Silberals Fällungsmittel, 52als Nachweisreagenz, 57, 60, 63, 79–81,
95Nachweise, 76Vorprobe, 50
Silicat (Nachweis), 70Sodaauszug, 51Spatel, 24Spritzflasche, 25Strontium
als Nachweisreagenz, 105Nachweise, 103Vorprobe, 43
Sulfat (Nachweis), 65Sulfid (Nachweis), 62Sulfit (Nachweis), 64
TThiocyanatals Nachweisreagenz, 56, 91, 99Nachweis, 58
Thiosulfat (Nachweis), 63TiegelBlei, 24Nickel, 24Porzellan, 23Verwendung, 31
Tiegelzange, 24Tondreieck, 25Verwendung, 31
TrennungsgangAmmoniakgruppe, 90Ammoniumcarbonatgruppe, 100Ammoniumsulfidgruppe, 96Arsengruppe, 77halogenhaltige Säuren, 54Kupfergruppe, 78lösliche Gruppe, 105Salzsäuregruppe, 73Schwefelverbindungen, 55Schwefelwasserstoffgruppe, 76
Trichter, 26Tropfer, 23Verwendung, 28
Tüpfelplatte, 26Verwendung, 29
Tüpfelreaktionen, 29
UUhrglasschale, 23Umfüllen von Flüssigkeiten, 28
VVorproben, 43
WWasserbad, 31Wasserbadeinsatz, 26
ZZentrifuge, 26

148 Sachverzeichnis
Verwendung, 32Zentrifugenglas, 26Zinkals Nachweisreagenz, 62, 67, 79Nachweise, 96
Vorprobe, 47Zinnals Nachweisreagenz, 80, 88Nachweise, 83Vorprobe, 49
Related Documents